Активатор транскрипции — это белок ( фактор транскрипции ), который увеличивает транскрипцию гена или набора генов. [1] Считается, что активаторы положительно контролируют экспрессию генов, поскольку они способствуют транскрипции генов и, в некоторых случаях, необходимы для возникновения транскрипции генов. [1] [2] [3] [4] Большинство активаторов представляют собой ДНК-связывающие белки , которые связываются с энхансерами или проксимальными элементами промотора . [1] Сайт ДНК, связанный с активатором, называется «сайтом связывания активатора». [3] Часть активатора, которая осуществляет белок-белковые взаимодействия с общим механизмом транскрипции, называется «активирующей областью» или «доменом активации». [1]
Большинство активаторов действуют путем специфичного связывания последовательности с регуляторным участком ДНК, расположенным рядом с промотором, и осуществляя белок-белковые взаимодействия с общим механизмом транскрипции ( РНК-полимеразой и общими факторами транскрипции ), тем самым облегчая связывание общего механизма транскрипции с промотором. [1] [2] [3] [4] Другие активаторы способствуют транскрипции генов, заставляя РНК-полимеразу высвобождаться из промотора и продвигаться по ДНК. [2] Иногда РНК-полимераза может приостанавливать работу вскоре после выхода из промотора; Активаторы также позволяют этим «остановившимся» РНК-полимеразам продолжать транскрипцию. [1] [2]
Активность активаторов можно регулировать. Некоторые активаторы имеют аллостерический сайт и могут функционировать только тогда, когда определенная молекула связывается с этим сайтом, по сути, включая активатор. [4] Посттрансляционные модификации активаторов также могут регулировать активность, увеличивая или уменьшая активность в зависимости от типа модификации и модифицируемого активатора. [1]
В некоторых клетках, обычно эукариотах, с сайтом связывания могут связываться несколько активаторов; эти активаторы имеют тенденцию связываться кооперативно и взаимодействовать синергически. [1] [2]
Белки-активаторы состоят из двух основных доменов : ДНК-связывающего домена , который связывается с последовательностью ДНК, специфичной для активатора, и домена активации , который действует для увеличения транскрипции генов путем взаимодействия с другими молекулами. [1] ДНК-связывающие домены активатора имеют различные конформации, в том числе спираль-поворот-спираль , цинковый палец и лейциновую застежку-молнию . [1] [2] [3] Эти ДНК-связывающие домены специфичны для определенной последовательности ДНК, что позволяет активаторам включать только определенные гены. [1] [2] [3] Активационные домены также бывают различных типов, которые классифицируются на основе аминокислотной последовательности домена, включая богатые аланином , богатые глутамином и кислотные домены. [1] Эти домены не столь специфичны и имеют тенденцию взаимодействовать с различными целевыми молекулами. [1]
Активаторы также могут иметь аллостерические сайты , отвечающие за включение и выключение самих активаторов. [4]
В бороздках двойной спирали ДНК обнажены функциональные группы пар оснований. [2] Таким образом, последовательность ДНК создает уникальный рисунок поверхностных особенностей, включая области возможных водородных связей , ионных связей , а также гидрофобных взаимодействий . [2] Активаторы также имеют уникальные последовательности аминокислот с боковыми цепями, которые способны взаимодействовать с функциональными группами ДНК. [2] [3] Таким образом, структура боковых цепей аминокислот, составляющих белок-активатор, будет комплементарна поверхностным особенностям специфической регуляторной последовательности ДНК, с которой он был разработан, чтобы связываться. [1] [2] [3] Комплементарные взаимодействия между аминокислотами белка-активатора и функциональными группами ДНК создают «точную» специфичность между активатором и его регуляторной последовательностью ДНК. [2]
Большинство активаторов связываются с основными бороздками двойной спирали, поскольку эти области имеют тенденцию быть шире, но есть некоторые, которые связываются с второстепенными бороздками. [1] [2] [3]
Сайты связывания активатора могут располагаться очень близко к промотору или на расстоянии многих пар оснований. [2] [3] Если регуляторная последовательность расположена далеко, ДНК образует петлю (зацикливание ДНК), чтобы связанный активатор мог взаимодействовать с механизмом транскрипции в промоторном сайте. [2] [3]
У прокариот несколько генов могут транскрибироваться вместе ( оперон ) и, таким образом, контролируются одной и той же регуляторной последовательностью. [2] У эукариот гены, как правило, транскрибируются индивидуально, и каждый ген контролируется своими собственными регуляторными последовательностями. [2] Регуляторные последовательности, с которыми связываются активаторы, обычно находятся выше промотора, но их также можно найти ниже или даже внутри интронов у эукариот. [1] [2] [3]
Связывание активатора с его регуляторной последовательностью способствует транскрипции гена, обеспечивая активность РНК-полимеразы. [1] [2] [3] [4] Это осуществляется с помощью различных механизмов, таких как привлечение транскрипционного аппарата к промотору и запуск РНК-полимеразы для продолжения элонгации. [1] [2] [3] [4]
Гены, контролируемые активаторами, требуют связывания активаторов с регуляторными сайтами, чтобы рекрутировать необходимый транскрипционный аппарат в область промотора. [1] [2] [3]
Взаимодействия активатора с РНК-полимеразой преимущественно прямые у прокариот и непрямые у эукариот. [2] У прокариот активаторы имеют тенденцию напрямую контактировать с РНК-полимеразой, чтобы помочь связать ее с промотором. [2] У эукариот активаторы в основном взаимодействуют с другими белками, и именно эти белки затем будут взаимодействовать с РНК-полимеразой. [2]
У прокариот гены, контролируемые активаторами, имеют промоторы, которые сами по себе не способны прочно связываться с РНК-полимеразой. [2] [3] Таким образом, белки-активаторы способствуют связыванию РНК-полимеразы с промотором. [2] [3] Это делается с помощью различных механизмов. Активаторы могут изгибать ДНК, чтобы лучше обнажить промотор, чтобы РНК-полимераза могла связываться более эффективно. [3] Активаторы могут вступать в прямой контакт с РНК-полимеразой и закреплять ее на промоторе. [2] [3] [4]
У эукариот активаторы имеют множество различных молекул-мишеней, которые они могут рекрутировать для стимулирования транскрипции генов. [1] [2] Они могут рекрутировать другие факторы транскрипции и кофакторы , которые необходимы для инициации транскрипции. [1] [2]
Активаторы могут рекрутировать молекулы, известные как коактиваторы . [1] [2] Эти молекулы-коактиваторы затем могут выполнять функции, необходимые для начала транскрипции, вместо самих активаторов, например, модификации хроматина. [1] [2]
ДНК у эукариот гораздо более конденсирована; таким образом, активаторы имеют тенденцию рекрутировать белки, которые способны реструктурировать хроматин, чтобы промотор стал более доступным для транскрипционного аппарата. [1] [2] Некоторые белки меняют расположение нуклеосом вдоль ДНК, чтобы обнажить сайт промотора ( АТФ-зависимые комплексы ремоделирования хроматина ). [1] [2] Другие белки влияют на связывание между гистонами и ДНК посредством посттрансляционных модификаций гистонов , позволяя ДНК, плотно завернутой в нуклеосомы, ослабнуть. [1] [2]
Все эти привлеченные молекулы работают вместе, чтобы в конечном итоге привлечь РНК-полимеразу к промоторному сайту. [1] [2]
Активаторы могут способствовать транскрипции генов, сигнализируя РНК-полимеразе о необходимости выйти за пределы промотора и продолжить движение вдоль ДНК, инициируя начало транскрипции. [2] Иногда РНК-полимераза может приостанавливать работу вскоре после начала транскрипции, и для высвобождения РНК-полимеразы из этого «остановленного» состояния требуются активаторы. [1] [2] Существует множество механизмов высвобождения этих «остановившихся» РНК-полимераз. Активаторы могут действовать просто как сигнал, запускающий дальнейшее движение РНК-полимеразы. [2] Если ДНК слишком конденсирована, чтобы позволить РНК-полимеразе продолжить транскрипцию, активаторы могут рекрутировать белки, которые могут реструктурировать ДНК, чтобы удалить любые блоки. [1] [2] Активаторы также могут способствовать привлечению факторов элонгации, которые необходимы РНК-полимеразе для продолжения транскрипции. [1] [2]
Существуют разные способы регулирования активности самих активаторов, чтобы гарантировать, что активаторы стимулируют транскрипцию генов в подходящее время и на соответствующих уровнях. [1] Активность активатора может увеличиваться или уменьшаться в ответ на раздражители окружающей среды или другие внутриклеточные сигналы. [1]
Активаторы часто необходимо «включить», прежде чем они смогут способствовать транскрипции генов. [2] [3] [4] Активность активаторов контролируется способностью активатора связываться со своим регуляторным участком на ДНК. [2] [3] [4] ДНК-связывающий домен активатора имеет активную и неактивную форму, которые контролируются связыванием молекул, известных как аллостерические эффекторы , с аллостерическим сайтом активатора. [4]
Активаторы в своей неактивной форме не связаны с какими-либо аллостерическими эффекторами. [4] В неактивном состоянии активатор не способен связываться со своей специфической регуляторной последовательностью в ДНК и, таким образом, не оказывает регулирующего воздействия на транскрипцию генов. [4]
Когда аллостерический эффектор связывается с аллостерическим сайтом активатора, происходит конформационное изменение ДНК-связывающего домена, что позволяет белку связываться с ДНК и увеличивать транскрипцию гена. [2] [4]
Некоторые активаторы способны претерпевать посттрансляционные модификации , которые влияют на их активность внутри клетки. [1] Было замечено, что такие процессы, как фосфорилирование , ацетилирование и убиквитинирование , среди прочих, регулируют активность активаторов. [1] В зависимости от добавляемой химической группы, а также природы самого активатора, посттрансляционные модификации могут либо увеличивать, либо уменьшать активность активатора. [1] Например, было замечено, что ацетилирование увеличивает активность некоторых активаторов за счет таких механизмов, как увеличение аффинности связывания ДНК. [1] С другой стороны, убиквитинирование снижает активность активаторов, поскольку убиквитин маркирует белки для деградации после того, как они выполнили свои соответствующие функции. [1]
У прокариот одинокий белок-активатор способен стимулировать транскрипцию. [2] [3] У эукариотов в месте связывания обычно собирается более одного активатора, образуя комплекс, который способствует транскрипции. [1] [2] Эти активаторы кооперативно связываются в сайте связывания, а это означает, что связывание одного активатора увеличивает аффинность сайта к связыванию другого активатора (или, в некоторых случаях, другого регулятора транскрипции), что облегчает взаимодействие нескольких активаторов. привязать на сайте. [1] [2] В этих случаях активаторы взаимодействуют друг с другом синергетически , а это означает, что скорость транскрипции, достигаемая за счет совместной работы нескольких активаторов, намного выше, чем аддитивный эффект активаторов, если бы они работали индивидуально. [1] [2]
Расщепление мальтозы в Escherichia coli контролируется активацией генов. [3] Гены, кодирующие ферменты, ответственные за катаболизм мальтозы, могут транскрибироваться только в присутствии активатора. [3] Активатор, который контролирует транскрипцию ферментов мальтозы, «выключен» в отсутствие мальтозы. [3] В неактивной форме активатор не способен связываться с ДНК и способствовать транскрипции генов мальтозы. [3] [4]
Когда мальтоза присутствует в клетке, она связывается с аллостерическим сайтом белка-активатора, вызывая конформационные изменения в ДНК-связывающем домене активатора. [3] [4] Это конформационное изменение «включает» активатор, позволяя ему связываться со своей специфической регуляторной последовательностью ДНК. [3] [4] Связывание активатора с его регуляторным участком способствует связыванию РНК-полимеразы с промотором и, следовательно, транскрипции, вырабатывая ферменты, необходимые для расщепления мальтозы, попавшей в клетку. [3]
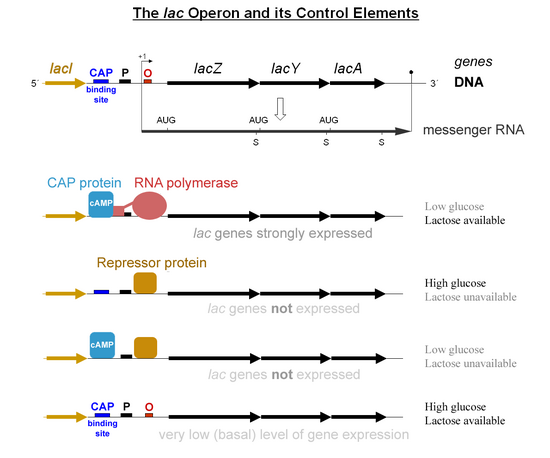
Белок -активатор катаболита (CAP), также известный как белок рецептора цАМФ (CRP), активирует транскрипцию lac- оперона бактерии Escherichia coli . [5] Циклический аденозинмонофосфат (цАМФ) вырабатывается во время глюкозного голодания; эта молекула действует как аллостерический эффектор, который связывается с CAP и вызывает конформационные изменения, которые позволяют CAP связываться с участком ДНК, расположенным рядом с промотором lac. [5] Затем CAP осуществляет прямое белок-белковое взаимодействие с РНК-полимеразой, которая рекрутирует РНК-полимеразу на lac-промотор. [5]