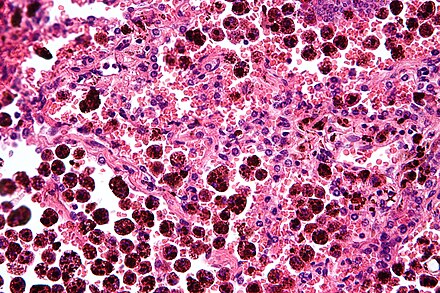
Альвеолярный макрофаг , легочный макрофаг (или пылевая клетка ) — разновидность макрофага , профессионального фагоцита , обнаруживаемого в дыхательных путях и на уровне альвеол в легких , но отделенного от их стенок. [1]
Активность альвеолярных макрофагов сравнительно высока, поскольку они расположены на одной из важнейших границ между организмом и внешним миром. Они отвечают за удаление частиц, таких как пыль или микроорганизмы, с поверхностей дыхательных путей.
Альвеолярные макрофаги часто содержат гранулы экзогенного материала, такого как частицы углерода , которые они улавливают с поверхностей дыхательных путей. Такие черные гранулы могут особенно часто встречаться в легких курильщиков или постоянных городских жителей.
Альвеолярные макрофаги — третий тип клеток альвеолы; остальные представляют собой пневмоциты типа I и типа II .



Альвеолярные макрофаги — это фагоциты, которые играют решающую роль в гомеостазе , защите хозяина и ремоделировании тканей. [7] Плотность населения имеет решающее значение для многих процессов. Они обладают высокой адаптивностью и могут выделять множество секретов для взаимодействия с другими клетками и молекулами, используя несколько поверхностных рецепторов . Альвеолярные макрофаги также участвуют в фагоцитозе апоптотических и некротических клеток. [8] Им необходимо избирательно выбирать материал, который фагоцитируется, чтобы защитить нормальные клетки и структуры. [8] Для борьбы с инфекцией фагоциты облегчают работу многих рецепторов распознавания образов (PRR), помогая распознавать молекулярные узоры, связанные с патогенами (PAMP), на поверхности патогенных микроорганизмов. [9] Все PAMP имеют общие черты: они уникальны для группы патогенов , но инвариантны в своей базовой структуре; и необходимы для патогенности (способности организма вызывать инфекционное заболевание в другом организме). [9] Белки, участвующие в распознавании микробных образов, включают рецептор маннозы, рецепторы комплемента, DC-SIGN, Toll-подобные рецепторы (TLR), рецептор-поглотитель, CD14 и Mac-1. [9] [10] PRR можно разделить на три класса:
Распознавание и уничтожение вторгшихся микроорганизмов происходит как опсонин-зависимыми, так и опсонин-независимыми путями. Молекулярные механизмы, облегчающие опсонин-зависимый фагоцитоз, различны для конкретных пар опсонин/рецептор. Например, фагоцитоз IgG-опсонизированных патогенов происходит через рецепторы Fcγ (FcγR) и включает расширение фагоцитов вокруг микроба, что приводит к выработке провоспалительных медиаторов. И наоборот, поглощение патогенов, опосредованное рецептором комплемента, происходит без заметного расширения мембраны (частицы просто погружаются в клетку) и обычно не приводит к реакции медиатора воспаления.
После интернализации микроб заключен в везикулярную фагосому, которая затем сливается с первичными или вторичными лизосомами , образуя фаголизосому. [9] Существуют различные механизмы, которые приводят к внутриклеточному уничтожению; существуют окислительные процессы и другие, независимые от окислительного метаболизма. Первый включает активацию мембранных ферментных систем, которые приводят к стимуляции поглощения кислорода (известному как дыхательный взрыв) и его восстановлению до промежуточных продуктов активного кислорода (ROI), молекулярных разновидностей, которые высокотоксичны для микроорганизмов. [9] Фермент, ответственный за возникновение дыхательного взрыва, известен как никотинамидадениндинуклеотидфосфат (НАДФН)-оксидаза, которая состоит из пяти субъединиц. [9] Одним из компонентов является мембранный цитохром, состоящий из двух белковых субъединиц, gp91phox и p22phox; остальные три компонента представляют собой белки цитозольного происхождения: p40phox, p47phox и p67phox. [9] НАДФН-оксидаза существует в цитозоле АМ, когда он находится в состоянии покоя; но после активации два его цитозольных компонента, p47phox и p67phox, фосфорилируют остатки тирозина и серина, которые затем способны опосредовать транслокацию NADPHox в цитохромный компонент gp91phox/p22phox на плазматической мембране через элементы цитоскелета. [11]
По сравнению с другими фагоцитами дыхательный взрыв при АМ имеет большую величину. [9] Кислороднезависимые микробицидные механизмы основаны на продукции кислоты, секреции лизоцимов, железосвязывающих белках и синтезе токсичных катионных полипептидов. [9] Макрофаги обладают набором антимикробных молекул, упакованных в их гранулы и лизосомы. [9] Эти органеллы содержат множество деградирующих ферментов и антимикробных пептидов, которые высвобождаются в фаголизосомы, таких как протеазы, нуклеазы, фосфатазы, эстеразы, липазы и высокоосновные пептиды. [9] Более того, макрофаги обладают рядом механизмов лишения питательных веществ, которые используются для лишения фагоцитируемых патогенов необходимых микроэлементов. [9] Некоторые микроорганизмы разработали контрмеры, которые позволяют им избежать уничтожения фагоцитами. Хотя деградация, опосредованная лизосомами, является эффективным средством нейтрализации инфекции и предотвращения колонизации, некоторые патогены паразитируют на макрофагах, используя их в качестве клеток-хозяев для роста, поддержания и репликации. [9] Паразиты, такие как Toxoplasma gondii и микобактерии, способны предотвращать слияние фагосом с лизосомами, избегая таким образом вредного действия лизосомальных гидролаз. Другие избегают лизосом, покидая фагоцитарную вакуоль и достигая цитозольного матрикса, где их развитие беспрепятственно. В этих случаях макрофаги могут активно уничтожать фагоцитированные микроорганизмы, производя ряд высокотоксичных молекул и запуская депривационный механизм, вызывающий их голодание. [9] Наконец, у некоторых микробов есть ферменты для детоксикации метаболитов кислорода, образующихся во время респираторного взрыва. [9]
Когда альвеолярные макрофаги недостаточны для отражения угрозы, они могут выделять провоспалительные цитокины и хемокины, вызывая высокоразвитую сеть защитных фагоцитарных клеток, ответственных за адаптивный иммунный ответ.
Легкие особенно чувствительны и склонны к повреждениям, поэтому, чтобы избежать сопутствующего повреждения пневмоцитов типа I и типа II, альвеолярные макрофаги поддерживаются в состоянии покоя, продуцируя мало воспалительных цитокинов и проявляя небольшую фагоцитарную активность, о чем свидетельствует сниженная экспрессия фагоцитарной активности. рецептор антиген макрофага 1 (Mac-1). [7] [12] АМ активно подавляют индукцию двух иммунных систем организма: адаптивного иммунитета и гуморального иммунитета. Адаптивный иммунитет подавляется за счет воздействия АМ на интерстициальные дендритные клетки, В-клетки и Т-клетки, поскольку эти клетки менее избирательны в отношении того, что они разрушают, и часто наносят ненужный ущерб нормальным клеткам. Для предотвращения неконтролируемого воспаления в нижних дыхательных путях альвеолярные макрофаги секретируют оксид азота, простагландины , интерлейкины-4 и -10 (IL-4, IL-10) и трансформирующий фактор роста -β (TGF-β). [12] [13] [14] [15]
Оксид азота (NO) является основным источником иммуномодуляции у грызунов и вырабатывается ферментом синтетазой оксида азота типа 2 (NOS2) в альвеолярных макрофагах. [14] NO ингибирует фосфорилирование тирозина киназ, участвующих в выработке рецептора интерлейкина-2 (IL-2), экспрессия которого имеет фундаментальное значение для пролиферации Т-клеток. [13] Однако у людей активность NOS2 проверить сложно. [14]
Существует два объяснения отсутствия реакции промотора индуцибельной синтетазы оксида азота человека (iNOS) на активацию NO липополисахаридами ( ЛПС) + интерфероном гамма (IFNγ). [14] Во-первых, существуют различные вариации инактивирующих нуклеотидов в человеческом аналоге энхансерного элемента, который регулирует индуцированную LPS/IFNγ экспрессию мышиного гена NOS2. Во-вторых, это связано с отсутствием в макрофагах человека ядерного фактора, необходимого для оптимальной экспрессии гена NOS2 (комплекс ЛПС-индуцируемый ядерный фактор-каппа B/Rel). [14] Предполагается, что сложность проверки NOS2 связана с гораздо более строго контролируемой экспрессией АМ человека по сравнению с таковой у АМ грызунов. [14] NOS2 является частью петли обратной связи ауторегуляции, в которой аллерген или провокатор стимулирует выработку воспалительных цитокинов, которые, в свою очередь, стимулируют выработку NO, а NO подавляет выработку цитокинов. [14] У крыс NO ингибирует опосредованное гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF) созревание дендритных клеток, а у людей он ингибирует опосредованное TNF-альфа созревание дендритных клеток человека посредством циклического GMP-зависимого механизмы. [14] NO продлевает способность дендритных клеток человека интернализировать антигены в местах воспаления, тем самым модулируя начальные этапы, ведущие к антигенспецифическим иммунным ответам. [14]
Производство NO имеет отношение к патологии астмы. У людей, страдающих астмой, наблюдается повышенная экспрессия iNOS в эпителиальных клетках дыхательных путей и повышенный уровень оксида азота в выдыхаемом воздухе. [14]
Выделено множество других иммуномодулирующих факторов, важнейшими из которых являются простагландины и цитокины. PGE2 был первым иммуномодулятором, полученным из макрофагов и описанным. [14] PGE2 участвует в усилении транскрипции IL-10 лимфоцитов периферической крови и выработке белка; а также в дезактивации макрофагов и Т-клеток. [14] PGE2 представляет собой иммуномодулирующий эйкозаноид, полученный из компонента клеточной мембраны, арахидоновой кислоты , и обрабатывается в каскаде арахидоновой кислоты: последовательная оксигенация и изомеризация арахидоновой кислоты ферментами циклооксигеназой и синтазой PGE2. [16] Регуляция клеток-мишеней с помощью PGE2 происходит посредством передачи сигналов через четыре связанных с клеточной мембраной, связанных с G-белком, E-простаноидных (EP) рецепторов, называемых EP1, EP2, EP3 и EP4. [16] PGE2 ингибирует уничтожение бактерий и продукцию ROI с помощью AM, нарушая Fcγ-опосредованный фагоцитоз благодаря его способности стимулировать выработку внутриклеточных эффекторов циклического аденозинмонофосфата (цАМФ) через передачу сигналов рецепторов EP2 и EP4. [11] [16] Рецепторы EP2 и EP4 передают сигнал в первую очередь через стимулирующий G-белок (Gs), увеличивая активность аденилатциклазы (AC) и последующее образование цАМФ. [11] цАМФ является вторичным мессенджером, который влияет на множество клеточных функций посредством активации двух нижестоящих эффекторных молекул, протеинкиназы А (PKA) и обменных белков, непосредственно активируемых цАМФ (Epac-1 и -2). [11] Epac-1 и PKA являются важными факторами, участвующими в ингибировании уничтожения бактерий AM. [11] Эффекты PKA обусловлены ее способностью фосфорилировать остатки серина и треонина на многих клеточных белках, особенно на белке, связывающем ответный элемент фактора транскрипции цАМФ (CREB). Ось цАМФ/ПКА/CREB опосредует ингибирование высвобождения TNF-альфа. [11] Уничтожение фагоцитированных бактерий АМ зависит от нескольких различных микробицидных механизмов, таких как снижение опосредованного НАДФН-оксидазой высвобождения ROI. [9] [11] Генерация ROI с помощью НАДФН-оксидазы является важным бактерицидным механизмом после FcR-опосредованного фагоцитоза. [11] PGE2 активирует как Gs-связанные рецепторы EP2, так и EP4 путем лигирования, стимулируя выработку цАМФ и последующую активацию нижестоящих эффекторов цАМФ, PKA и Epac-1; оба из них, в свою очередь, нарушают фосфорилирование и транслокацию в фагосомальную мембрану компонента НАДФН-оксидазы, p47phox, тем самым ингибируя респираторный взрыв. [11]
IL-4 представляет собой плейотропный цитокин, который играет ключевую роль в развитии Т-хелперных клеток 2-го типа (Th2). IL-4 важен для дифференцировки наивных клеток CD4-T в зрелые клетки типа Th2; а также при переключении класса иммуноглобулинов (Ig) на IgE и IgG4 при развитии иммунных ответов. [17] [18] Ig — это класс антител, обнаруженных только у млекопитающих, который играет важную роль в аллергической реакции и защите от многих видов патогенов, защищая организм от них путем активации комплемента, опсонизации для фагоцитоза и нейтрализации их токсинов. . [18]
Было показано, что IL-4 и IL-10 снижают выработку металлопротеиназ (эндопептидаз, которые расщепляют коллаген и другие внеклеточные белки) АМ человека. [14] [15] IL-4 оказывает двойное воздействие на биологическую функцию макрофагов, которое может быть либо стимулирующим, либо ингибирующим. [15] Он усиливает экспрессию антигена MHC класса II (внеклеточный белковый комплекс, который взаимодействует исключительно с CD4-T-клетками как часть экзогенного пути) и Mac-1 (поверхностный рецептор как часть врожденной системы комплемента), тем самым способствуя фагоцитозу. [15] Также было показано, что IL-4 ингибирует выработку PGE2 за счет снижения экспрессии фермента простагландин H-синтазы-2 (PGHS-2), который имеет решающее значение в выработке PGE2. [14] Однако IL-4 ингибирует выработку TNF-альфа, IL-1 и -6, которые являются важными цитокинами в провоспалительной реакции). [15]
IL-10 ингибирует секрецию провоспалительных цитокинов TNF-альфа и INF-гамма, подавляя тем самым пролиферацию Т-клеток, NK-клеток и АМ. [14] IL-10 имеет схожие с TGF-β механизмы иммуномодулирования. [14] Считается, что оба цитокина снижают скорость апоптоза в альвеолярных макрофагах человека, тем самым косвенно усиливая опосредованное альвеолярными макрофагами ингибирование пролиферации Т-клеток. [14] Наблюдается значительное увеличение базальной скорости апоптоза при активации бактериальными продуктами. Апоптоз в частности регулируется присутствием цитокинов: IFNγ увеличивает скорость апоптоза, тогда как IL-10 и TGF-β снижают ее. [14] Однако IL-10 оказывает контрпродуктивное воздействие на иммунную систему и, как было показано, фактически способствует заражению чужеродными патогенами. Роль IL-10 в бактериальных и паразитарных инфекциях была обнаружена как стратегия уклонения от иммунной системы хозяина. [19] Существуют бактерии, которые паразитируют на АМ, проникая через их мембраны, и процветают за счет роста и размножения внутри них, используя АМ в качестве клеток-хозяев. В норме эту инфекцию можно устранить с помощью Т-клеток, которые активируют ферменты альвеолярных макрофагов, уничтожающие бактерии; но было показано, что эти бактерии изменяют сигнальную сеть цитокинов в свою пользу. Как ингибирующий цитокин, IL-10 облегчает инфицирование альвеолярных макрофагов и моноцитов человека, полностью обращая защитный эффект IFNγ против внутриклеточной репликации Legionella pneumophila. [19] Также было показано, что Yersinia enterocolitica высвобождает вирулентный антиген LcrV, который индуцирует IL-10 через Toll-подобный рецептор-2 и CD14 (вспомогательный поверхностный белок TLR4-опосредованной передачи сигналов LPS), что приводит к подавлению IFNγ и Подавление ФНО-альфа. [19]
В нормальных условиях альвеолярные макрофаги тесно прикрепляются к альвеолярным эпителиальным клеткам, индуцируя тем самым экспрессию интегрина αvβ6. Интегрины представляют собой димерные рецепторы клеточной поверхности, состоящие из альфа- и бета-субъединиц, которые активируют TGF-β.< [20] [21] TGF-β представляет собой многофункциональный цитокин, который модулирует различные биологические процессы, такие как рост клеток, апоптоз, внеклеточный матрикс. синтез, воспаление и иммунные реакции. [22] TGF-β жестко регулирует противовоспалительную активность, подавляя выработку провоспалительных цитокинов, тем самым ингибируя функцию Т-лимфоцитов. [23] Интегрины avβ6 и avβ8 секвестрируют латентный TGF-β на поверхности клетки, где активация может быть тесно связана с клеточными реакциями на стресс окружающей среды при поддержании гомеостаза; интегрины также локализуют активированный TGFβ вблизи макрофагов. [24] В норме зрелый TGFβ секретируется в виде латентного комплекса с его N-концевым фрагментом, латентно-ассоциированным пептидом (LAP), который ингибирует его активность. [22] Латентный комплекс ковалентно связан с внеклеточным матриксом путем связывания со латентными TGF-β-связывающими белками. [20] TGF-β активируется в легких различными механизмами, в конечном итоге включающими либо протеолиз, либо конформационные изменения LAP. [24] Интегрин αvβ6 способен опосредовать активацию TGF-β путем связывания с LAP TGF-β1, который служит сайтом связывания лиганда для интегрина и является важным компонентом аппарата активации TGF-β. [22] [25] После активации TGFβ приводит к подавлению функциональности макрофагов (выработка цитокинов и фагоцитоз). [22] Связывание активированного TGF-β с его рецепторами, экспрессируемыми на альвеолярных макрофагах, индуцирует нижестоящий сигнальный каскад, включая фосфорилирование гомологов 2 и 3, регулируемых рецепторами Small Mothers Against Decapentaplegic (R-SMAD). [ 7] [22] [23 ] ] Фосфорилированные SMAD-2 и -3 затем образуют гетеромерные комплексы с общим медиатором SMAD 4 (со-SMAD-4). После сборки комплексы транслоцируются в ядро через ядерную пору с помощью импортинов альфа/бета. Попадая в ядро, эти комплексы накапливаются и в конечном итоге действуют как факторы транскрипции, регулируя экспрессию генов-мишеней TGF-β. [23] Таким образом, передача сигналов TGF-β включает прямой путь от рецепторов на поверхности клетки к ядру.
Toll-подобные рецепторы (TLR) представляют собой сигнальные PRR , способные распознавать различные бактериальные белки. [10] Хотя бактерии разработали способы уклонения от защитных механизмов хозяина, они экспрессируют PAMP, такие как липогликаны и липопротеины, которые распознаются клетками врожденной иммунной системы через TLR. [10] При связывании PAMP с TLR TLR запускает воспалительные и защитные реакции в клетке-хозяине, индуцируя полимеризацию актина в альвеолярных макрофагах (важнейший компонент эндоцитоза и подвижности). [22] Полимеризация актина в альвеолярных макрофагах вызывает подавление экспрессии интегрина, что, в свою очередь, вызывает дезактивацию TGF-β и снижение уровня базального фосфорилирования SMAD 2/3; что впоследствии приводит к активации и отслоению альвеолярных макрофагов от альвеолярных эпителиальных клеток [22] [15]. После активации макрофаги готовятся к фагоцитозу и начинают секретировать провоспалительные цитокины (TNF-α и IL-6). [22]
Праймирование макрофагов включает усиление активности респираторного взрыва под действием IFN-γ и TNF-α. [9] IFNγ индуцирует как повышенное сродство НАДФН-оксидазы к НАДФН в макрофагах, так и повышенную скорость транскрипции гена и экспрессии сообщения для белка gp91phox. [9] TNF-α действует как аутокринный стимул, увеличивая экспрессию транскриптов p47phox и p67phox. ROI, образующиеся во время ответа на дыхательный взрыв, в свою очередь, усиливают выработку TNF-α макрофагами. [9]
Газообмен должен быть восстановлен как можно быстрее, чтобы избежать побочных повреждений, поэтому активированные лимфоциты секретируют IFNγ, чтобы стимулировать выработку макрофагами матриксной металлопротеиназы MMP-9. [22] Сообщалось, что AM продуцируют MMP-9 частично через PGE2-зависимые сигнальные пути PKA, которые являются путями, участвующими в ингибировании фагоцитоза. [26] MMP-9 активирует латентный TGF-β, усиливая экспрессию интегринов αvβ6 на альвеолярных эпителиальных клетках, тем самым возвращая альвеолярные макрофаги в состояние покоя. [7] [22] [26] Активация TGF-β также выгодна, поскольку его продукция стимулирует синтез коллагена в интерстициальных фибробластах, который необходим для восстановления архитектуры альвеолярных стенок. [22]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )