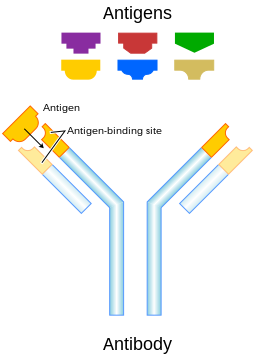
В иммунологии антиген ( Ag ) — это молекула , фрагмент , чужеродные частицы или аллерген , например пыльца , которые могут связываться со специфическим антителом или рецептором Т-клеток . [1] Присутствие антигенов в организме может вызвать иммунный ответ . [2]
Антигенами могут быть белки , пептиды (цепи аминокислот), полисахариды (цепи простых сахаров), липиды или нуклеиновые кислоты . [3] [4] Антигены существуют на нормальных клетках , раковых клетках , паразитах , вирусах , грибах и бактериях . [1] [3]
Антигены распознаются антигенными рецепторами, включая антитела и рецепторы Т-клеток. [3] Клетки иммунной системы производят разнообразные антигенные рецепторы, поэтому каждая клетка обладает специфичностью к одному антигену. [3] При воздействии антигена только лимфоциты, распознавшие этот антиген, активируются и размножаются. Этот процесс известен как клональная селекция . [4] В большинстве случаев антитела антигенспецифичны , что означает, что антитело может реагировать и связываться только с одним конкретным антигеном; однако в некоторых случаях антитела могут перекрестно реагировать , связываясь более чем с одним антигеном. Реакция между антигеном и антителом называется реакцией антиген-антитело .
Антиген может возникать либо изнутри организма (« собственный белок » или «собственные антигены»), либо из внешней среды («чужие»). [2] Иммунная система идентифицирует и атакует «чужие» внешние антигены. Антитела обычно не реагируют с аутоантигенами из-за отрицательной селекции Т -клеток в тимусе и В-клеток в костном мозге . [5] Заболевания, при которых антитела реагируют с собственными антигенами и повреждают собственные клетки организма, называются аутоиммунными заболеваниями . [6]
Вакцины являются примерами антигенов в иммуногенной форме, которые намеренно вводят реципиенту, чтобы индуцировать функцию памяти адаптивной иммунной системы в отношении антигенов патогена, проникшего в этого реципиента. Типичным примером является вакцина от сезонного гриппа . [7]
Пауль Эрлих ввел термин антитело ( нем . Antikörper ) в своей теории боковой цепи в конце 19 века. [8] В 1899 году Ладислас Дойч (Ласло Детре) назвал гипотетические вещества, находящиеся на полпути между бактериальными составляющими и антителами, «антигенными или иммуногенными веществами» ( фр . «вещества иммуногенные или антигенные »). Первоначально он полагал, что эти вещества являются предшественниками антител, точно так же, как зимоген является предшественником фермента . Но к 1903 году он понял, что антиген индуцирует выработку иммунных тел (антител), и написал, что слово «антиген» представляет собой сокращение слова «антисоматоген» ( Immunkörperbildner ). Оксфордский словарь английского языка указывает, что логическая конструкция должна быть «анти(тело)-ген». [9] Первоначально этот термин относился к веществу, которое действует как генератор антител. [10]
Антигенпрезентирующие клетки представляют антигены в виде пептидов на молекулах гистосовместимости . Т-клетки избирательно распознают антигены; в зависимости от антигена и типа молекулы гистосовместимости будут активированы разные типы Т-клеток. Для распознавания Т-клеточным рецептором (TCR) пептид должен быть процессирован на небольшие фрагменты внутри клетки и представлен главным комплексом гистосовместимости (MHC). [12] Антиген не может вызвать иммунный ответ без помощи иммунологического адъюванта . [13] Аналогичным образом, адъювантный компонент вакцин играет важную роль в активации врожденной иммунной системы. [14] [15]
Иммуноген — это антигенное вещество (или аддукт ), способное запускать гуморальный (врожденный) или клеточно-опосредованный иммунный ответ. [16] Сначала он инициирует врожденный иммунный ответ, который затем вызывает активацию адаптивного иммунного ответа. Антиген связывает высоковариабельные продукты иммунорецепторов (рецептор В-клеток или рецептор Т-клеток) после их образования. Иммуногены – это антигены, называемые иммуногенными , способные вызывать иммунный ответ. [17]
На молекулярном уровне антиген можно охарактеризовать по его способности связываться с паратопами антитела . Различные антитела способны различать специфические эпитопы, присутствующие на поверхности антигена. Гаптен — это небольшая молекула , которая может вызвать иммунный ответ только при присоединении к более крупной молекуле-переносчику, такой как белок . Антигенами могут быть белки, полисахариды, липиды , нуклеиновые кислоты или другие биомолекулы. [4] Сюда входят части (оболочки, капсулы, клеточные стенки, жгутики, фимбрии и токсины) бактерий , вирусов и других микроорганизмов . Немикробные несобственные антигены могут включать пыльцу, яичный белок и белки из трансплантированных тканей и органов или на поверхности перелитых клеток крови.
Антигены можно классифицировать в зависимости от их источника.
Экзогенные антигены — это антигены, попавшие в организм извне, например, при вдыхании , проглатывании или инъекции . Реакция иммунной системы на экзогенные антигены часто носит субклинический характер. Путем эндоцитоза или фагоцитоза экзогенные антигены попадают в антигенпрезентирующие клетки (АПК) и расщепляются на фрагменты. Затем APC представляют фрагменты Т-хелперным клеткам ( CD4 + ) с помощью молекул гистосовместимости класса II на их поверхности. Некоторые Т-клетки специфичны для комплекса пептид:MHC. Они активируются и начинают секретировать цитокины, вещества, которые активируют цитотоксические Т-лимфоциты (CTL), В-клетки, секретирующие антитела , макрофаги и другие частицы.
Некоторые антигены изначально экзогенны, а затем становятся эндогенными (например, внутриклеточные вирусы). Внутриклеточные антигены могут быть возвращены в кровообращение после разрушения инфицированной клетки.
Эндогенные антигены образуются внутри нормальных клеток в результате нормального клеточного метаболизма или вследствие вирусной или внутриклеточной бактериальной инфекции . Затем фрагменты презентируются на поверхности клетки в комплексе с молекулами MHC класса I. Если активированные цитотоксические CD8 + Т-клетки распознают их, Т-клетки выделяют различные токсины , которые вызывают лизис или апоптоз инфицированной клетки. Чтобы не дать цитотоксическим клеткам убивать клетки только ради представления собственных белков , цитотоксические клетки (аутореактивные Т-клетки) удаляются в результате толерантности (негативной селекции). Эндогенные антигены включают ксеногенные (гетерологичные), аутологичные и идиотипические или аллогенные (гомологичные) антигены. Иногда антигены являются частью самого хозяина при аутоиммунном заболевании . [2]
Аутоантиген обычно представляет собой собственный белок или белковый комплекс (а иногда и ДНК или РНК), который распознается иммунной системой пациентов с конкретным аутоиммунным заболеванием . В нормальных условиях эти собственные белки не должны быть мишенью иммунной системы, но при аутоиммунных заболеваниях связанные с ними Т-клетки не удаляются, а вместо этого атакуют.
Неоантигены — это те, которые полностью отсутствуют в нормальном геноме человека. По сравнению с немутированными собственными белками неоантигены имеют значение для контроля опухоли, поскольку на качество пула Т-клеток, доступного для этих антигенов, не влияет центральная толерантность Т-клеток. Технология систематического анализа реактивности Т-клеток против неоантигенов стала доступной лишь недавно. [18] Неоантигены можно непосредственно обнаружить и количественно оценить. [19]
Для вирус-ассоциированных опухолей, таких как рак шейки матки и некоторые виды рака головы и шеи , эпитопы , полученные из вирусных открытых рамок считывания, вносят вклад в пул неоантигенов. [18]
Опухолевые антигены — это антигены, которые представлены молекулами MHC класса I или MHC класса II на поверхности опухолевых клеток . Антигены, обнаруженные только в таких клетках, называются опухолеспецифическими антигенами (TSA) и обычно возникают в результате опухолеспецифической мутации . Более распространены антигены, представленные опухолевыми и нормальными клетками, называемые опухолеассоциированными антигенами (ТАА). Цитотоксические Т-лимфоциты , распознающие эти антигены, могут разрушать опухолевые клетки. [18]
Опухолевые антигены могут появиться на поверхности опухоли в виде, например, мутировавшего рецептора, и в этом случае они распознаются В-клетками . [18]
Для опухолей человека невирусной этиологии новые пептиды (неоэпитопы) создаются путем опухолеспецифичных изменений ДНК. [18]
Большая часть опухолевых мутаций человека фактически специфична для пациента. Следовательно, неоантигены также могут быть основаны на отдельных опухолевых геномах. Технологии глубокого секвенирования могут выявить мутации в кодирующей белок части генома ( экзоме ) и предсказать потенциальные неоантигены. На моделях мышей для всех новых белковых последовательностей были предсказаны потенциальные MHC-связывающие пептиды. Полученный набор потенциальных неоантигенов использовали для оценки реактивности Т-клеток. Анализы на основе экзома использовались в клинических условиях для оценки реактивности у пациентов, получавших либо клеточную терапию инфильтрирующих опухоль лимфоцитов (TIL), либо блокаду контрольных точек. Идентификация неоантигена оказалась успешной для множества экспериментальных модельных систем и злокачественных опухолей человека. [18]
Частота ложноотрицательных результатов секвенирования ракового экзома низка, т.е. большинство неоантигенов встречаются в экзонной последовательности с достаточным покрытием. Однако подавляющее большинство мутаций в экспрессируемых генах не приводят к образованию неоантигенов, распознаваемых аутологичными Т-клетками. [18]
По состоянию на 2015 год разрешение масс-спектрометрии недостаточно, чтобы исключить многие ложноположительные результаты из пула пептидов, которые могут быть представлены молекулами MHC. Вместо этого используются алгоритмы для выявления наиболее вероятных кандидатов. Эти алгоритмы учитывают такие факторы, как вероятность протеасомного процессинга, транспорт в эндоплазматический ретикулум , сродство к соответствующим аллелям MHC класса I и уровни экспрессии генов или трансляции белков. [18]
Большинство неоантигенов человека, идентифицированных в ходе беспристрастного скрининга, демонстрируют высокую прогнозируемую аффинность связывания MHC. Минорные антигены гистосовместимости, концептуально схожий класс антигенов, также правильно идентифицируются алгоритмами связывания MHC. Другой потенциальный фильтр проверяет, улучшит ли мутация связывание MHC. Природа центральных TCR-экспонированных остатков MHC-связанных пептидов связана с иммуногенностью пептида. [18]
Нативный антиген – это антиген, который еще не расщеплен АПК на более мелкие части. Т-клетки не могут связывать нативные антигены, но требуют, чтобы они обрабатывались АПК, тогда как В-клетки могут быть активированы нативными антигенами.
Антигенная специфичность — это способность клеток-хозяев распознавать антиген как уникальную молекулярную единицу и отличать его от другого с исключительной точностью. Специфичность антигена обусловлена прежде всего конформациями боковой цепи антигена. Оно измеримо и не обязательно должно быть линейным или состоять из шага или уравнения с ограниченной скоростью. [2] [7] И Т-клетки , и В-клетки являются клеточными компонентами адаптивного иммунитета . [2] [4]