
Медьорганическая химия — это изучение физических свойств, реакций и синтеза медьорганических соединений , которые представляют собой металлоорганические соединения, содержащие химическую связь между углеродом и медью . [1] [2] [3] Это реагенты в органической химии .
Первое медьорганическое соединение, взрывчатый ацетилид меди(I) Cu 2 C 2 ( Cu-C≡C-Cu ), было синтезировано Рудольфом Кристианом Беттгером в 1859 году путем пропускания газообразного ацетилена через раствор хлорида меди(I) : [4 ] ]
Медьорганические соединения разнообразны по строению и реакционной способности, но почти все они основаны на меди со степенью окисления +1, иногда обозначаемой Cu(I) или Cu + . Имея 10 электронов в валентной оболочке , поведение связи Cu(I) аналогично Ni(0), но из-за более высокой степени окисления он участвует в меньшем количестве пи-связей . Органические производные меди с более высокими степенями окисления +2 и +3 иногда встречаются в качестве промежуточных продуктов реакции , но редко выделяются или даже наблюдаются.
Медьорганические соединения образуют комплексы с различными мягкими лигандами , такими как алкилфосфины ( R 3 P ), тиоэфиры ( R 2 S ) и цианид ( CN - ).
Благодаря сферической электронной оболочке Cu + комплексы меди(I) имеют симметричное строение — линейное, тригонально-планарное или тетраэдрическое , в зависимости от числа лигандов.
Давно известно, что соли меди(I) связывают CO, хотя и слабо. Представительным комплексом является полимерный комплекс CuCl(CO). В отличие от классических карбонилов металлов, пи-связь в этих соединениях не является прочной. [5]

Алкены связываются с медью(I), хотя опять же, как правило, слабо. Связывание этилена с Cu в белках имеет настолько широкое значение в биологии растений, что этилен классифицируется как растительный гормон . Его присутствие, обнаруживаемое Cu-белком, влияет на созревание и многие другие процессы. [6]
Хотя медь не образует металлоцена , можно получить полусэндвич-комплексы. Одним из таких производных является π-циклопентадиенил(триэтилфосфин)медь(I). [7]
Галогениды меди реагируют с литийорганическими реагентами с образованием медьорганических соединений. Первооткрывателем этой области был Генри Гилман , который сообщил о метилмеди в 1936 году. Таким образом, фенилмедь получается реакцией фениллития с бромидом меди (I) в диэтиловом эфире . Вместо литийорганических соединений можно использовать реактивы Гриньяра. Гилман также исследовал диалкилкупраты. Их получают путем объединения двух эквивалентов RLi с солями Cu(I). Альтернативно, эти купраты получают из олигомерных нейтральных медьорганических соединений путем обработки одним эквивалентом литийорганического реагента.
Соединения типа [CuR n ] ( n -1)- реакционноспособны по отношению к кислороду и воде, образуя оксид меди(I) . Они также имеют тенденцию быть термически нестабильными, что может быть полезно в некоторых реакциях сочетания. Несмотря на эти трудности или из-за них, медьорганические реагенты часто производятся и потребляются на месте , без попыток их выделения. Их используют в органическом синтезе в качестве алкилирующих реагентов, поскольку они проявляют большую толерантность к функциональным группам , чем соответствующие реагенты Гриньяра и литийорганические реагенты. Электроотрицательность меди намного выше , чем у ее ближайшего соседа по группе 12 элементов , цинка , что предполагает пониженную нуклеофильность ее углеродных лигандов.
Соли меди реагируют с концевыми алкинами с образованием ацетилидов .
Алкилгалогениды реагируют с медьорганическими соединениями с инверсией конфигурации. С другой стороны, реакции медьорганического соединения с алкенилгалогенидами протекают с сохранением конфигурации субстрата. [8]
Медьорганические соединения соединяются с арилгалогенидами (см. Конденсацию Ульмана и реакцию Ульмана ):
Алкильные и арильные комплексы меди агрегируют как в кристаллической форме, так и в растворе. Агрегация особенно очевидна для медьорганических соединений с нейтральным зарядом, т.е. соединений с эмпирической формулой (RCu), которые принимают циклические структуры. Поскольку для каждого медного центра требуется как минимум два лиганда, органическая группа является мостиковым лигандом . Этот эффект иллюстрируется структурой мезитилмеди, которая представляет собой пентамер. Циклическая структура также наблюдается у CuCH 2 SiMe 3 , где Me означает метильную группу CH 3 , первого медьорганического соединения с соотношением 1:1, которое было проанализировано методом рентгеновской кристаллографии (Lappert, 1972). Это соединение относительно стабильно, поскольку объемистые триметилсилильные группы обеспечивают стерическую защиту. Это тетрамер , образующий 8-членное кольцо с чередующимися связями Cu-C. Кроме того, четыре атома меди образуют плоское кольцо Cu 4 на основе трехцентровых двухэлектронных связей . Длина связи между медью составляет 242 пм по сравнению с 256 пм в массивной меди. В пентамезитилпентамеди образуется 5-членное медное кольцо, аналогичное (2,4,6-триметилфенил)золоту, а пентафторфенилмедь представляет собой тетрамер. [9]
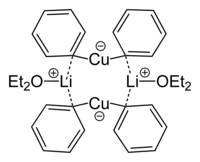
Диметилкупрат лития(I) представляет собой димер в диэтиловом эфире , образующий 8-членное кольцо с двумя атомами лития, соединяющими две метильные группы, (Li + [Cu(CH 3 ) 2 ] - ) 2 . Аналогичным образом дифенилкупрат лития (I) образует димерный эфират ([Li(O(CH 2 CH 3 ) 2 )] + [Cu Ph 2 ] - ) 2 в твердом состоянии. [10]
Участие редкой в других отношениях степени окисления Cu (III) было продемонстрировано при сопряженном присоединении реагента Гилмана к енону : [11] В так называемом эксперименте ЯМР с быстрым введением при -100 ° C реактив Гилмана Li + [Cu(CH 3 ) 2 ] − (стабилизированный иодидом лития ) вводили в циклогексенон ( 1 ), что позволило обнаружить медь-алкен пи-комплекс 2 . При последующем добавлении триметилсилилцианида образуется форма Cu(III) 3 (неопределенно стабильная при этой температуре), а при повышении температуры до -80 °C - продукт сопряженного присоединения 4 . Согласно сопутствующим экспериментам in silico [12] промежуточный продукт Cu(III) имеет квадратную плоскую молекулярную геометрию с цианогруппой в цис- ориентации по отношению к циклогексенилметиновой группе и антипараллельной метиновому протону. Это исследование предсказывает появление стабильных при комнатной температуре соединений Cu(III) с другими лигандами, кроме цианогруппы .
До разработки реакций кросс-сочетания , катализируемых палладием , медь была предпочтительным катализатором в течение почти столетия. Палладий обеспечивает более быструю и избирательную реакцию. Медные реагенты и катализаторы продолжают оставаться предметом инноваций. По сравнению с палладием медь дешевле, но обороты меди часто ниже, а условия реакции более энергичны. [13]
Реакции Li + [CuR 2 ] − с алкилгалогенидами R'−X дают продукт сочетания:
Механизм реакции включает окислительное присоединение (ОА) алкилгалогенида к Cu(I) с образованием планарного промежуточного соединения Cu(III) с последующим восстановительным элиминированием (RE). Нуклеофильная атака является стадией, определяющей скорость. При замещении йодида предложен одноэлектронный механизм переноса (см. рисунок).
В этой реакции участвуют многие электрофилы. Примерный порядок реакционной способности, начиная с наиболее реакционноспособной, следующий: хлорангидриды [14] > альдегиды > тозилаты ~ эпоксиды > йодиды > бромиды > хлориды > кетоны > сложные эфиры > нитрилы >> алкены.
В целом механизм OA-RE аналогичен механизму реакций кросс-сочетания, катализируемых палладием. Одно из различий между медью и палладием заключается в том, что медь может подвергаться процессам одноэлектронного переноса. [8]
Окислительная реакция — это реакция ацетилидов меди с сопряженными алкинами в реакции Глейзера (например, при синтезе циклооктадеканонаена ) или с арилгалогенидами в реакции Кастро-Стивенса .
Восстановительная реакция — это реакция сочетания арилгалогенидов со стехиометрическим эквивалентом металлической меди, которая происходит в реакции Ульмана . Родственная реакция, называемая декарбоксилативным кросс-сочетанием , одним из партнеров сочетания является карбоксилат. Cu(I) замещает карбоксил , образуя промежуточный арилмедь (ArCu). Одновременно палладиевый катализатор реагирует с арилбромидом с образованием палладиевого промежуточного соединения (Ar'PdB), которое подвергается переметаллированию с образованием ArPdAr', что, в свою очередь, восстановительно удаляет биарил . [15] [16]
Редокс-нейтральная реакция — это реакция концевых алкинов с галогеналкинами с солью меди (I) в реакции Кадио-Ходкевича . Также возможно термическое соединение двух медьорганических соединений.
Карбокупрация представляет собой нуклеофильное присоединение медьорганических реагентов ( R-Cu ) к ацетилену или концевым алкинам , приводящее к образованию алкенилмедного соединения ( R 2 C=C(R)-Cu ). [17] Это особый случай карбометаллирования , также называемый реакцией Норманта . [18] [19]
Гидриды меди являются специализированными восстановителями . Хорошо известный гидрид меди представляет собой реактив Страйкера с формулой [(PPh 3 )CuH] 6 . Он уменьшает алкеновую часть α,β-ненасыщенных карбонильных соединений . [21] В родственной, но каталитической реакции используется комплекс меди(I) NHC с гидридными эквивалентами, обеспечиваемыми гидросиланом . [22] [23]
Реакции алкилирования медьорганических реагентов, как правило, протекают через гамма -алкилирование. Цис - гамма- атака лучше происходит в циклогексилкарбамате из-за стерических свойств. Сообщается, что реакция протекает в эфирных растворителях. Этот метод оказался очень эффективным для окислительного сочетания аминов и алкилов, в том числе трет -бутила, и арилгалогенидов. [24]
Вицинальная функционализация с использованием последовательности альдольных реакций карбокупрата/Мукаиямы: [25]
Мюллер и его коллеги сообщили о вицинальной функционализации α,β-ацетиленовых эфиров с использованием последовательности реакции карбокупратион/альдоль Мукаямы (как показано на рисунке выше). Карбокупрат способствует образованию Z-альдола.