Дигидроксилирование — это процесс, при котором алкен превращается в вицинальный диол . Хотя существует множество способов осуществления этого окисления , в наиболее распространенных и прямых процессах используется переходный металл с высокой степенью окисления (обычно осмий или марганец). Металл часто используется в качестве катализатора в сочетании с другим стехиометрическим окислителем. [1] Кроме того, для катализа реакции были разработаны и использованы другие методы с переходными и непереходными металлами.


В механизме дигидроксилирования лиганд сначала координируется с металлическим катализатором (обозначенным как осмий), что определяет хиральную селективность олефина. Затем алкен координируется с металлом посредством (3+2)-циклоприсоединения, и лиганд диссоциирует от металлического катализатора. Затем гидролиз олефина дает вицинальный диол, а окисление катализатора стехиометрическим окислителем регенерирует металлический катализатор, повторяя цикл. [2] Концентрация олефина имеет решающее значение для энантиомерного избытка диола, поскольку более высокие концентрации алкена могут связываться с другим каталитическим центром с образованием другого энантиомера. [3]
Четырехокись осмия (OsO 4 ) является популярным окислителем, используемым при дигидроксилировании алкенов из-за его надежности и эффективности при получении син-диолов. Поскольку он дорог и токсичен, используют каталитические количества OsO 4 совместно со стехиометрическим окислителем. [2] [3] В реакциях гидроксилирования Миласа , дигидроксилирования Апджона и асимметричного дигидроксилирования Шарплесса в качестве катализатора используется осмий, а также различные вторичные окислители.
Дигидроксилирование по Миласу было введено в 1930 году, и в нем в качестве стехиометрического окислителя используется перекись водорода. [4] Хотя этот метод позволяет получать диолы, переокисление до дикарбонильного соединения привело к трудностям при выделении вицинального диола. [4] Таким образом, протокол Миласа был заменен асимметричным дигидроксилированием Апджона и Шарплесса.
О дигидроксилировании Апджона сообщалось в 1973 году, и в нем в качестве активного катализатора в процедуре дигидроксилирования используется OsO 4 . Он также использует N-оксид N-метилморфолина (NMO) в качестве стехиометрического окислителя для регенерации осмиевого катализатора, что позволяет использовать каталитические количества осмия. [2] [5] Протокол Апджона обеспечивает высокую конверсию вицинального диола и переносит многие субстраты. Однако протокол не может дигидроксилировать тетразамещенные алкены. [2] Условия Апджона можно использовать для синтеза антидиолов из аллильных спиртов, как продемонстрировали Киши и его коллеги. [6]
Асимметричное дигидроксилирование Шарплесса [7] было разработано К. Барри Шарплессом для использования каталитических количеств OsO 4 вместе со стехиометрическим окислителем K 3 [Fe(CN) 6 ]. [1] [2] [8] Реакцию проводят в присутствии хирального вспомогательного вещества. Выбор дигидрохинидина (DHQD) или дигидрохинина (DHQ) в качестве хирального вспомогательного средства диктует лицевую селективность олефина, поскольку абсолютная конфигурация лигандов противоположна. [2] [8] [9] Катализатор, окислитель и хиральное вспомогательное вещество можно приобрести предварительно смешанными для селективного дигидроксилирования. AD-mix-α содержит хиральный вспомогательный компонент (DHQ) 2 PHAL, который позиционирует OsO 4 на альфа-грани олефина; AD-mix-β содержит (DHQD) 2 PHAL и доставляет гидроксильные группы к бета-лицу. [1] [10] Асимметричное дигидроксилирование по Шарплессу имеет большие возможности для селективности субстрата за счет изменения хирального вспомогательного класса. [8]


Как упоминалось выше, возможность синтеза антидиолов из аллильных спиртов может быть достигнута при использовании NMO в качестве стехиометрического окислителя. [6] Использование тетраметилендиамина (TMEDA) в качестве лиганда привело к образованию син-диолов с благоприятным диастереомерным соотношением по сравнению с протоколом Киши; однако используется стехиометрический осмий. Син-селективность обусловлена донорной способностью аллилового спирта к донору водородных связей и акцепторной способностью диамина. [11] [12] [13] С тех пор это было применено к гомоаллильным системам. [14] [15]
Поскольку четырехокись осмия дорогая и токсичная, для получения вицинальных диолов из олефинов использовались другие металлы. Другим популярным металлом, используемым при дигидроксилировании, является рутений. Несмотря на высокую окислительную способность, рутений использовался из-за его короткого времени реакции и экономической эффективности. [16] Обычно четырехокись рутения создается на месте из трихлорида рутения, а вторичный окислитель NaIO 4 используется для регенерации катализатора. Стадией реакции, лимитирующей оборот, является стадия гидролиза; поэтому для увеличения скорости этой стадии добавляют серную кислоту. [16] [17]
Марганец также используется при дигидроксилировании, и его часто выбирают, когда методы с тетроксидом осмия дают плохие результаты. [17] Как и в случае с рутением, окислительный потенциал марганца высок, что приводит к чрезмерному окислению субстратов. Перманганат калия часто используется в качестве окислителя при дигидроксилировании; однако из-за его плохой растворимости в органическом растворителе также добавляют катализатор межфазного переноса (такой как хлорид бензилтриэтиламмония, TEBACl) для увеличения количества субстратов для дигидроксилирования. [17] Во избежание чрезмерного окисления необходимы мягкие условия. В частности, слишком теплый, кислый или концентрированный раствор приведет к расщеплению гликоля. [18]

В отличие от других описанных методов, в которых в качестве катализатора используются переходные металлы, в методах Прево и Вудворда используются йод и соль серебра. Однако добавление воды в реакцию направляет цис- и транс-присоединение гидроксильных групп. В реакции Прево обычно используется бензоат серебра для получения транс-диолов; В модификации Вудворда реакции Прево используется ацетат серебра для получения цис-диолов. И в реакциях Прево, и в реакциях Вудворда йод сначала добавляется к алкену, образуя циклический ион йода. Анион соответствующей соли серебра затем присоединяется путем нуклеофильного замещения к иону йода. [19]

В реакции Прево ион йода подвергается нуклеофильной атаке бензоат-аниона. Бензоат-анион снова действует как нуклеофил, замещая йодид посредством механизма участия соседних групп. Второй бензоат-анион реагирует с промежуточным соединением с образованием антизамещенного дибензоатного продукта, который затем может подвергаться гидролизу с образованием транс-диолов. [19]

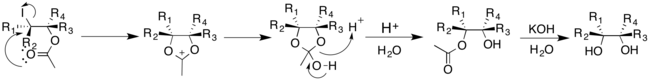
Модификация Вудворда реакции Прево дает цис-диолы. Ацетат-анион реагирует с циклическим ионом йода с образованием промежуточного иона оксония. Затем он может легко реагировать с водой с образованием моноацетата, который затем гидролизуется с образованием цис-диола [20].
Чтобы исключить необходимость в солях серебра, Судалай и его коллеги модифицировали реакцию Прево-Вудворда; реакция катализируется LiBr, а в качестве окислителей используются NaIO 4 и PhI(OAc) 2 . [21] LiBr реагирует с NaIO 4 и уксусной кислотой с образованием ацетата лития, который затем может протекать по реакции, как упоминалось ранее. Протокол дал высокий Dr для соответствующего диола, в зависимости от выбранного окислителя.

Синтез высокозамещенных и стереоспецифичных сахаров важен, поскольку полисахариды составляют большой класс соединений, встречающихся в природе. Одним из конкретных примеров является биологически активная молекула какелокелоза, которая, как было показано, обладает анти-ВИЧ-активностью. [22] Исследование, проведенное Harris et al. работали над энантиоспецифическим синтезом сахаров, относящихся к какелокелозе и другим сахарам, используя множество различных реакций дигидроксилирования с осмиевым катализатором. Винилфуран подвергали реакции в условиях Шарплесса с AD-mix-α с получением (R)-диола. Позже полученный дигидропиран подвергали реакции в условиях Апджона с получением сахара, маннозы (где R представляет собой либо H, либо защитную группу). [22]

Кроме того, талоза и гулоза также были синтезированы из другого дигидропирана. Поскольку соединение содержит аллильный спирт, условия Апджона и модификация Апджона с использованием TMEDA в качестве вторичного окислителя для создания полученных сахаров (где R представляет собой либо H, либо защитную группу). [22]

Другое применение методов дигидроксилирования - синтез стероидов. Брассиностероиды — это класс стероидов, которые, как было показано, регулируют рост растений и обладают сельскохозяйственной активностью в качестве инсектицида. Этот класс стероидов содержит стандартную структуру стероидов в дополнение к четырем вицинальным диолам, имеющим свою собственную стереохимию. [23] Броза установил гидроксильные группы в стероиде, используя оба условия Вудворда, чтобы получить цис-диол в кольце А стероида. Затем алкеновую цепь в кольце D дигидроксилировали с получением второго цис-диола, используя OsO 4 и NMO в качестве стехиометрического окислителя. [24]
