Газовая хроматография ( ГХ ) — это распространенный тип хроматографии, используемый в аналитической химии для разделения и анализа соединений, которые могут испаряться без разложения . Типичные применения ГХ включают проверку чистоты определенного вещества или разделение различных компонентов смеси. [1] В препаративной хроматографии ГХ может использоваться для получения чистых соединений из смеси. [2] [3]
Газовая хроматография также иногда известна как хроматография паровой фазы ( VPC ) или газожидкостная хроматография распределения ( GLPC ). Эти альтернативные названия, а также их соответствующие сокращения часто используются в научной литературе. [2]
Газовая хроматография — это процесс разделения соединений в смеси путем введения газообразного или жидкого образца в подвижную фазу, обычно называемую газом-носителем, и пропускания газа через неподвижную фазу. Подвижная фаза обычно представляет собой инертный газ или нереакционноспособный газ, такой как гелий , аргон , азот или водород . [1] Неподвижная фаза может быть твердой или жидкой, хотя большинство современных систем ГХ используют полимерную жидкую неподвижную фазу. [4] Неподвижная фаза содержится внутри разделительной колонки. Сегодня большинство колонок ГХ представляют собой капилляры из плавленого кварца с внутренним диаметром 100–320 микрометров (0,0039–0,0126 дюйма) и длиной 5–60 метров (16–197 футов). Колонка ГХ расположена внутри печи, где можно контролировать температуру газа, а выходящий из колонки поток контролируется соответствующим детектором. [1]
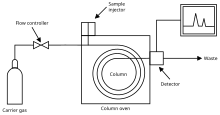
Газовый хроматограф состоит из узкой трубки, известной как колонка , через которую проходит испаренный образец, увлекаемый непрерывным потоком инертного или нереактивного газа. Компоненты образца проходят через колонку с разной скоростью, в зависимости от их химических и физических свойств и результирующего взаимодействия с футеровкой или наполнением колонки, называемым неподвижной фазой . Колонка обычно заключена в термостат с контролируемой температурой. Когда химикаты выходят из конца колонки, они обнаруживаются и идентифицируются электронным способом. [1]
_-_DPLA_-_6f678040232669661dcfb95308013cc0.jpg/440px-(Gas_chromatograph.)_-_DPLA_-_6f678040232669661dcfb95308013cc0.jpg)
Хроматография берет свое начало в 1903 году благодаря работе русского ученого Михаила Семеновича Цвета [5] , который разделил растительные пигменты с помощью жидкостной колоночной хроматографии.
Изобретение газовой хроматографии обычно приписывают Энтони Т. Джеймсу и Арчеру Дж. П. Мартину . [6] [7] Их газовый хроматограф использовал распределительную хроматографию в качестве принципа разделения, а не адсорбционную хроматографию . Популярность газовой хроматографии быстро возросла после разработки детектора пламенной ионизации. [8] Мартин и еще один их коллега, Ричард Синг , с которым он разделил Нобелевскую премию по химии 1952 года , отметили в более ранней статье [9], что хроматографию можно также использовать для разделения газов. Синг занимался другой работой, в то время как Мартин продолжал свою работу с Джеймсом.
Немецкий физик-химик Эрика Кремер в 1947 году вместе с австрийским аспирантом Фрицем Прайором разработали то, что можно было бы считать первым газовым хроматографом, который состоял из газа-носителя, колонки, заполненной силикагелем, и детектора теплопроводности. Они выставили хроматограф на выставке ACHEMA во Франкфурте, но никого он не заинтересовал. [10] NC Turner из Burrell Corporation представил в 1943 году массивный прибор, который использовал угольную колонку и пары ртути. Стиг Классон из Уппсальского университета опубликовал в 1946 году свою работу об угольной колонке, в которой также использовалась ртуть. [10] Герхард Гессе, будучи профессором в Университете Марбурга /Лана, решил проверить преобладающее среди немецких химиков мнение о том, что молекулы невозможно разделить в движущемся газовом потоке. Он установил простую стеклянную колонку, заполненную крахмалом, и успешно разделил бром и йод, используя азот в качестве газа-носителя. Затем он построил систему, которая пропускала инертный газ через стеклянный конденсатор, заполненный силикагелем, и собирала элюированные фракции. [10] Кортни С. Г. Филлипс из Оксфордского университета исследовал разделение в угольной колонке с использованием детектора теплопроводности. Он проконсультировался с Классоном и решил использовать вытеснение в качестве принципа разделения. Узнав о результатах Джеймса и Мартина, он переключился на распределительную хроматографию. [10]
Ранняя газовая хроматография использовала насадочные колонки, сделанные из блока длиной 1–5 м, диаметром 1–5 мм и заполненные частицами. Разрешение насадочных колонок было улучшено с изобретением капиллярной колонки, в которой неподвижная фаза нанесена на внутреннюю стенку капилляра. [6]
Автосэмплер обеспечивает возможность автоматического ввода образца во входные отверстия. Ручная вставка образца возможна, но больше не распространена. Автоматическая вставка обеспечивает лучшую воспроизводимость и оптимизацию времени .

Существуют различные виды автосамплеров. Автосамплеры можно классифицировать по емкости образца (автоинжекторы против автосамплеров, где автоинжекторы могут работать с небольшим количеством образцов), по роботизированным технологиям (робот XYZ [11] против вращающегося робота – наиболее распространенный) или по анализу:

Вход колонки (или инжектор) обеспечивает возможность введения образца в непрерывный поток газа-носителя. Вход представляет собой часть оборудования, прикрепленного к головке колонки.
Распространенные типы входных отверстий:
Выбор газа-носителя (подвижной фазы) важен. Водород имеет диапазон скоростей потока, которые сопоставимы с гелием по эффективности. Однако гелий может быть более эффективным и обеспечивать наилучшее разделение, если скорости потока оптимизированы. Гелий не воспламеняется и работает с большим количеством детекторов и более старыми приборами. Поэтому гелий является наиболее распространенным используемым газом-носителем. Однако цена гелия значительно выросла за последние годы, в результате чего все большее число хроматографистов переходят на водородный газ. Историческое использование, а не рациональные соображения, могут способствовать продолжению предпочтительного использования гелия.
Обычно используются детекторы пламенной ионизации (ПИД) и детектор теплопроводности (ДТП). Хотя ДТП выгодны тем, что они неразрушающие, их низкий предел обнаружения для большинства аналитов препятствует их широкому использованию. [1] ПИД чувствительны в первую очередь к углеводородам и более чувствительны к ним, чем ДТП. [4] ПИД не могут обнаруживать воду или углекислый газ, что делает их идеальными для анализа органических аналитов в окружающей среде. [1] ПИД в два-три раза более чувствителен к обнаружению аналитов, чем ДТП. [1]
ДТП основан на теплопроводности вещества, проходящего вокруг тонкой проволоки из вольфрам-рениевого сплава с проходящим по ней током. [4] В этой установке гелий или азот служат в качестве газа-носителя из-за их относительно высокой теплопроводности, которые поддерживают нить накала холодной и поддерживают равномерное удельное сопротивление и электрическую эффективность нити накала. [4] [13] Когда молекулы аналита вымываются из колонки, смешиваются с газом-носителем, теплопроводность уменьшается, в то время как температура нити накала и удельное сопротивление увеличиваются, что приводит к колебаниям напряжения, в конечном итоге вызывая отклик детектора. [4] [13] Чувствительность детектора пропорциональна току нити накала, в то время как она обратно пропорциональна непосредственной температуре окружающей среды этого детектора, а также скорости потока газа-носителя. [4]
В пламенно-ионизационном детекторе (ПИД) электроды размещаются рядом с пламенем, подпитываемым водородом/воздухом, вблизи выхода из колонки, и когда углеродсодержащие соединения выходят из колонки, они пиролизуются пламенем. [4] [13] Этот детектор работает только для органических/углеводородсодержащих соединений из-за способности углерода образовывать катионы и электроны при пиролизе, который генерирует ток между электродами. [4] [13] Увеличение тока транслируется и отображается в виде пика на хроматограмме. ПИД имеют низкие пределы обнаружения (несколько пикограмм в секунду), но они не способны генерировать ионы из карбонилов, содержащих углерод. [4] Совместимые с ПИД газы-носители включают гелий, водород, азот и аргон. [4] [13]
В FID иногда поток модифицируется перед поступлением в детектор. Метанизатор преобразует оксид углерода и диоксид углерода в метан, чтобы его можно было обнаружить. Другая технология — это polyarc от Activated Research Inc, которая преобразует все соединения в метан.
Щелочной пламенный детектор (AFD) или щелочной пламенно-ионизационный детектор (AFID) имеет высокую чувствительность к азоту и фосфору, подобно NPD. Однако ионы щелочного металла поставляются с водородным газом, а не с шариком над пламенем. По этой причине AFD не страдает от «усталости» NPD, но обеспечивает постоянную чувствительность в течение длительного периода времени. Кроме того, когда щелочные ионы не добавляются в пламя, AFD работает как стандартный FID. Каталитический детектор сгорания (CCD) измеряет горючие углеводороды и водород. Разрядно-ионизационный детектор (DID) использует высоковольтный электрический разряд для получения ионов.
Пламенный фотометрический детектор (ПФД) использует фотоумножительную трубку для обнаружения спектральных линий соединений, когда они сжигаются в пламени. Соединения, элюирующие из колонки, переносятся в водородное пламя, которое возбуждает определенные элементы в молекулах, а возбужденные элементы (P, S, галогены, некоторые металлы) излучают свет определенных характерных длин волн. [13] Излучаемый свет фильтруется и обнаруживается фотоумножительной трубкой. [4] [13] В частности, эмиссия фосфора составляет около 510–536 нм, а эмиссия серы — 394 нм. [4] [13] С помощью атомно-эмиссионного детектора (АЭД) образец, элюирующий из колонки, попадает в камеру, которая возбуждается микроволнами, которые вызывают плазму. [13] Плазма заставляет образец анализируемого вещества разлагаться, и определенные элементы генерируют спектры атомной эмиссии. [13] Спектр атомной эмиссии дифрагируется дифракционной решеткой и обнаруживается серией фотоумножительных трубок или фотодиодов. [13]
Детектор электронного захвата (ДЭЗ) использует источник радиоактивных бета-частиц (электронов) для измерения степени захвата электронов. ДЭЗ используются для обнаружения молекул, содержащих электроотрицательные / акцепторные элементы и функциональные группы, такие как галогены, карбонил, нитрилы, нитрогруппы и металлоорганические соединения. [4] [13] В этом типе детектора в качестве газа-носителя подвижной фазы используется азот или 5% метан в аргоне. [4] [13] Газ-носитель проходит между двумя электродами, размещенными в конце колонки, а рядом с катодом (отрицательным электродом) находится радиоактивная фольга, такая как 63Ni. [4] [13] Радиоактивная фольга испускает бета-частицу (электрон), которая сталкивается с газом-носителем и ионизирует его, генерируя больше ионов, что приводит к возникновению тока. [4] [13] Когда молекулы аналита с электроотрицательными / акцепторными элементами или функциональными группами захватываются электроны, что приводит к уменьшению тока, вызывающего отклик детектора. [4] [13]
Азотно-фосфорный детектор (NPD) — разновидность термоионного детектора, в котором азот и фосфор изменяют работу выхода на специально покрытом шарике, и измеряется результирующий ток.
Детектор сухой электролитической проводимости (DELCD) использует воздушную фазу и высокую температуру (v. Coulsen) для измерения хлорированных соединений.
Масс-спектрометр (МС), также называемый ГХ-МС ; высокоэффективен и чувствителен, даже при небольшом количестве образца. Этот детектор может использоваться для идентификации аналитов в хроматограммах по их масс-спектру. [14] Некоторые ГХ-МС подключены к ЯМР-спектрометру, который действует как резервный детектор. Эта комбинация известна как ГХ-МС-ЯМР. [ необходима цитата ] Некоторые ГХ-МС-ЯМР подключены к инфракрасному спектрофотометру , который действует как резервный детектор. Эта комбинация известна как ГХ-МС-ЯМР-ИК. Однако следует подчеркнуть, что это встречается очень редко, поскольку большинство необходимых анализов можно выполнить исключительно с помощью ГХ-МС. [ необходима цитата ]
Вакуумный ультрафиолет (ВУФ) представляет собой новейшую разработку в области детекторов газовой хроматографии. Большинство химических видов поглощают и имеют уникальные сечения поглощения газовой фазы в контролируемом диапазоне длин волн ВУФ приблизительно 120–240 нм. Если сечения поглощения известны для аналитов, детектор ВУФ способен к абсолютному определению (без калибровки) количества молекул, присутствующих в проточной ячейке при отсутствии химических помех. [15]
Ольфактометрический детектор , также называемый GC-O, использует человека-оценщика для анализа активности запаха соединений. С помощью порта запаха или порта для нюханья можно оценить качество запаха, интенсивность запаха и продолжительность активности запаха соединения.
Другие детекторы включают в себя детектор электролитической проводимости Холла (ElCD), детектор ионизации гелия (HID), инфракрасный детектор (IRD), фотоионизационный детектор (PID), детектор ионизации импульсного разряда (PDD) и термоионизационный детектор (TID). [16]
Метод — это набор условий, в которых ГХ работает для данного анализа. Разработка метода — это процесс определения того, какие условия являются адекватными и/или идеальными для требуемого анализа.
Условия, которые можно изменять для обеспечения требуемого анализа, включают температуру на входе, температуру детектора, температуру колонки и температурную программу, газ-носитель и скорость потока газа-носителя, неподвижную фазу колонки, диаметр и длину, тип и скорость потока на входе, размер образца и метод ввода. В зависимости от детектора(ов) (см. ниже), установленных на ГХ, может быть ряд условий детектора, которые также можно изменять. Некоторые ГХ также включают клапаны, которые могут изменять маршрут потока образца и носителя. Время открытия и закрытия этих клапанов может быть важным для разработки метода.
Типичные газы-носители включают гелий , азот , аргон и водород . [4] [1] Какой газ использовать, обычно определяется используемым детектором, например, DID требует гелий в качестве газа-носителя. [1] При анализе газовых образцов носитель также выбирается на основе матрицы образца, например, при анализе смеси в аргоне носитель аргона предпочтителен, поскольку аргон в образце не отображается на хроматограмме. Безопасность и доступность также могут влиять на выбор носителя.
Чистота газа-носителя также часто определяется детектором, хотя необходимый уровень чувствительности также может играть значительную роль. Обычно используются степени чистоты 99,995% и выше. Наиболее распространенные степени чистоты, требуемые современными приборами для большинства чувствительности, — это степени 5,0 или чистота 99,999%, что означает, что в газе-носителе содержится в общей сложности 10 ppm примесей, которые могут повлиять на результаты. Наиболее высокие степени чистоты, которые обычно используются, — это степени 6,0, но необходимость обнаружения на очень низких уровнях в некоторых судебно-медицинских и экологических приложениях обусловила потребность в газах-носителях степени чистоты 7,0, и теперь они доступны в продаже. Торговые наименования типичных степеней чистоты включают «нулевой класс», «сверхвысокий класс чистоты (UHP)», «класс 4,5» и «класс 5,0».
Линейная скорость газа-носителя влияет на анализ так же, как и температура (см. выше). Чем выше линейная скорость, тем быстрее анализ, но тем ниже разделение между аналитами. Выбор линейной скорости, таким образом, является тем же компромиссом между уровнем разделения и продолжительностью анализа, что и выбор температуры колонки. Линейная скорость будет реализована посредством расхода газа-носителя с учетом внутреннего диаметра колонки.
В газовых хроматографах, выпущенных до 1990-х годов, скорость потока носителя контролировалась косвенно, путем управления входным давлением носителя или «давлением головки колонки». Фактическая скорость потока измерялась на выходе из колонки или детектора с помощью электронного расходомера или пузырькового расходомера и могла быть сложным, трудоемким и утомительным процессом. Было невозможно изменять настройку давления во время цикла, и, таким образом, поток был по существу постоянным во время анализа. Соотношение между скоростью потока и входным давлением рассчитывается с помощью уравнения Пуазейля для сжимаемых жидкостей .
Однако многие современные ГХ измеряют скорость потока электронным способом и контролируют давление газа-носителя, чтобы задать скорость потока. Следовательно, давление и скорость потока можно регулировать во время работы, создавая программы давления/потока, аналогичные программам температуры.
Полярность растворенного вещества имеет решающее значение для выбора неподвижного соединения, которое в оптимальном случае будет иметь такую же полярность, как и растворенное вещество. Обычными неподвижными фазами в открытых трубчатых колонках являются цианопропилфенилдиметилполисилоксан, карбовакс полиэтиленгликоль, бисцианопропилцианопропилфенилполисилоксан и дифенилдиметилполисилоксан. Для насадочных колонок доступны дополнительные варианты. [ 4]
Выбор типа впуска и метода ввода зависит от того, находится ли образец в жидкой, газообразной, адсорбированной или твердой форме, а также от того, присутствует ли матрица растворителя, которую необходимо испарить. Растворенные образцы можно вводить непосредственно в колонку через инжектор COC, если условия хорошо известны; если матрицу растворителя необходимо испарить и частично удалить, используется инжектор S/SL (наиболее распространенный метод ввода); газообразные образцы (например, воздушные баллоны) обычно вводятся с использованием системы клапанов переключения газа; адсорбированные образцы (например, на адсорбционных трубках) вводятся с использованием либо внешнего (онлайн или оффлайн) десорбционного аппарата, такого как система продувки и улавливания, либо десорбируются в инжекторе (приложения SPME).

Настоящий хроматографический анализ начинается с введения образца в колонку. Развитие капиллярной газовой хроматографии привело к появлению множества практических проблем с техникой ввода. Техника ввода в колонку, часто используемая с насадочными колонками, обычно невозможна с капиллярными колонками. В системе ввода в капиллярном газовом хроматографе вводимое количество не должно перегружать колонку, а ширина вводимой пробки должна быть небольшой по сравнению с распространением из-за хроматографического процесса. Несоблюдение этого последнего требования снизит разделительную способность колонки. Как правило, вводимый объем, V inj , и объем ячейки детектора, V det , должны составлять около 1/10 объема, занимаемого частью образца, содержащей интересующие молекулы (аналиты) при выходе из колонки.
Некоторые общие требования, которым должна соответствовать хорошая методика ввода, заключаются в том, что она должна обеспечивать оптимальную эффективность разделения колонки, обеспечивать точные и воспроизводимые вводы небольших количеств репрезентативных образцов, не вызывать изменений в составе образца, не демонстрировать дискриминации на основе различий в температуре кипения, полярности, концентрации или термической/каталитической стабильности и быть применимой как для анализа следов, так и для неразбавленных образцов.
Однако существует ряд проблем, присущих использованию шприцев для инъекций. Даже самые лучшие шприцы заявляют о точности всего 3%, а в неумелых руках ошибки гораздо больше. Игла может отрезать небольшие кусочки резины от мембраны, когда вводит через нее образец. Они могут заблокировать иглу и помешать заполнению шприца при следующем использовании. Может быть неочевидно, что это произошло. Часть образца может застрять в резине и высвободиться во время последующих инъекций. Это может привести к появлению ложных пиков на хроматограмме. Может иметь место избирательная потеря более летучих компонентов образца путем испарения с кончика иглы. [17]
Выбор колонки зависит от образца и измеряемого активного вещества. Основным химическим атрибутом, который учитывается при выборе колонки, является полярность смеси , но функциональные группы могут играть большую роль в выборе колонки. Полярность образца должна точно соответствовать полярности неподвижной фазы колонки для повышения разрешения и разделения при сокращении времени работы. Разделение и время работы также зависят от толщины пленки (неподвижной фазы), диаметра колонки и ее длины.

Колонка(и) в ГХ находятся в печи, температура которой точно контролируется электроникой. (Когда аналитик обсуждает «температуру колонки», он технически имеет в виду температуру печи колонки. Однако это различие не имеет значения и не будет впоследствии проводиться в этой статье.)
Скорость прохождения образца через колонку прямо пропорциональна температуре колонки. Чем выше температура колонки, тем быстрее образец проходит через колонку. Однако чем быстрее образец проходит через колонку, тем меньше он взаимодействует с неподвижной фазой и тем меньше аналитов разделяется.
Как правило, температура колонки выбирается с учетом компромисса между продолжительностью анализа и уровнем разделения.
Метод, который поддерживает колонку при одной и той же температуре в течение всего анализа, называется «изотермическим». Однако большинство методов повышают температуру колонки во время анализа, начальная температура, скорость повышения температуры (температурный «рамп») и конечная температура называются температурной программой.
Температурная программа позволяет адекватно разделять аналиты, элюирующиеся в начале анализа, и одновременно сокращать время, необходимое для прохождения аналитов, элюирующихся в конце анализа, через колонку.
Обычно хроматографические данные представляются в виде графика отклика детектора (ось Y) против времени удерживания (ось X), который называется хроматограммой. Это обеспечивает спектр пиков для образца, представляющих аналиты, присутствующие в образце, элюирующие из колонки в разное время. Время удерживания может быть использовано для идентификации аналитов, если условия метода постоянны. Кроме того, картина пиков будет постоянной для образца при постоянных условиях и может идентифицировать сложные смеси аналитов. Однако в большинстве современных приложений ГХ подключен к масс-спектрометру или аналогичному детектору, который способен идентифицировать аналиты, представленные пиками.
Площадь под пиком пропорциональна количеству аналита, присутствующего в хроматограмме. Вычислив площадь пика с использованием математической функции интегрирования , можно определить концентрацию аналита в исходном образце. Концентрацию можно рассчитать с помощью калибровочной кривой, созданной путем нахождения отклика для ряда концентраций аналита, или путем определения относительного фактора отклика аналита. Относительный фактор отклика представляет собой ожидаемое отношение аналита к внутреннему стандарту (или внешнему стандарту) и рассчитывается путем нахождения отклика известного количества аналита и постоянного количества внутреннего стандарта (химического вещества, добавленного к образцу при постоянной концентрации, с определенным временем удерживания аналита).
В большинстве современных систем ГХ-МС для построения и интегрирования пиков, а также сопоставления спектров МС с библиотечными спектрами используется компьютерное программное обеспечение .
В общем, вещества, которые испаряются ниже 300 °C (и, следовательно, стабильны до этой температуры), могут быть измерены количественно. Образцы также должны быть бессолевыми ; они не должны содержать ионов . Можно измерить очень малые количества вещества, но часто требуется, чтобы образец измерялся в сравнении с образцом, содержащим чистое, предполагаемое вещество, известное как эталонный стандарт .
Чтобы сделать показания более содержательными, можно использовать различные температурные программы, например, чтобы различать вещества, которые ведут себя одинаково в процессе ГХ.
Профессионалы, работающие с ГХ, анализируют содержание химического продукта, например, для обеспечения качества продукции в химической промышленности; или измеряют химические вещества в почве, воздухе или воде, например, почвенные газы . [18] ГХ очень точна при правильном использовании и может измерять пикомоли вещества в образце жидкости объемом 1 мл или концентрации частей на миллиард в газообразных образцах.
На практических курсах в колледжах студенты иногда знакомятся с ГХ, изучая состав лавандового масла или измеряя этилен , который выделяется растениями Nicotiana benthamiana после искусственного повреждения их листьев. Эти ГХ анализируют углеводороды (C2-C40+). В типичном эксперименте насадочная колонка используется для разделения легких газов, которые затем обнаруживаются с помощью ДТП . Углеводороды разделяются с помощью капиллярной колонки и обнаруживаются с помощью ПИД . Сложность с анализами легких газов, которые включают H2 , заключается в том, что He, который является наиболее распространенным и наиболее чувствительным инертным носителем (чувствительность пропорциональна молекулярной массе), имеет почти такую же теплопроводность, как и водород (именно разница в теплопроводности между двумя отдельными нитями в конструкции типа моста Уитстона показывает, когда компонент был элюирован). По этой причине распространены двойные приборы ДТП, используемые с отдельным каналом для водорода, который использует азот в качестве носителя. Аргон часто используется при анализе реакций газовой фазы химии, таких как синтез FT, так что можно использовать один газ-носитель вместо двух отдельных. Чувствительность снижается, но это компромисс ради простоты подачи газа.
Газовая хроматография широко используется в судебной экспертизе . Такие разнообразные дисциплины, как идентификация и количественная оценка твердых доз наркотиков (форма до употребления), расследование поджогов, анализ остатков краски и токсикологические дела, используют ГХ для идентификации и количественной оценки различных биологических образцов и улик с места преступления.
![]() Медиа, связанные с Газовая хроматография на Wikimedia Commons
Медиа, связанные с Газовая хроматография на Wikimedia Commons