


Гибридизация in situ (ISH) — это тип гибридизации , при котором используется меченая комплементарная ДНК , РНК или цепь модифицированных нуклеиновых кислот (т. е. зонд ) для локализации определенной последовательности ДНК или РНК в части или участке ткани ( in situ ) или, если ткань достаточно мала (например, семена растений, эмбрионы дрозофилы ), во всей ткани (целый препарат ISH), в клетках и в циркулирующих опухолевых клетках (ЦОК). Это отличается от иммуногистохимии , которая обычно локализует белки в срезах ткани.
Гибридизация in situ используется для выявления местоположения определенных последовательностей нуклеиновых кислот на хромосомах или в тканях, что является важным шагом для понимания организации, регуляции и функции генов. Ключевые методы, используемые в настоящее время, включают гибридизацию in situ с мРНК с олигонуклеотидными и РНК-зондами (как радиоактивно-меченными, так и гаптен-меченными), анализ с помощью светового и электронного микроскопов, гибридизацию in situ целиком , двойное обнаружение РНК и РНК плюс белок, и флуоресцентная гибридизация in situ для обнаружения хромосомных последовательностей. ДНК ISH можно использовать для определения структуры хромосом. Флуоресцентная ДНК ISH (FISH) может, например, использоваться в медицинской диагностике для оценки целостности хромосом. РНК ISH (гибридизация РНК in situ ) используется для измерения и локализации РНК (мРНК, днРНК и микроРНК) в срезах тканей, клетках, целых препаратах и циркулирующих опухолевых клетках (ЦОК). Гибридизацию in situ изобрели американские биологи Мэри-Лу Пардью и Джозеф Г. Галл . [1] [2] [3]
Гибридизация in situ — мощный метод идентификации конкретных видов мРНК внутри отдельных клеток в срезах тканей, позволяющий лучше понять физиологические процессы и патогенез заболеваний. Однако гибридизация in situ требует выполнения множества шагов с точной оптимизацией для каждой исследуемой ткани и каждого используемого зонда. Чтобы сохранить целевую мРНК в тканях, часто требуется использовать сшивающие фиксаторы (например, формальдегид ). [4]
Кроме того, гибридизация in-situ на срезах ткани требует, чтобы срезы ткани были очень тонкими, обычно толщиной от 3 до 7 мкм. Обычные методы подготовки срезов тканей для гибридизации in-situ включают разрезание образцов с помощью криостата или слайсера ткани Compresstome . Криостат берет свежую или фиксированную ткань и погружает ее в жидкий азот для мгновенного замораживания . Затем ткань помещают в замораживающую среду, называемую ОКТ, и делают тонкие срезы. К препятствиям относятся появление на тканях артефактов замораживания, которые могут помешать правильному окрашиванию мРНК. Compresstome разрезает ткань на тонкие ломтики без процесса замораживания; Свободно плавающие срезы вырезают после помещения в агарозу для стабильности. Этот метод позволяет избежать замораживания тканей и, следовательно, связанных с ним артефактов замораживания. После завершения процесс является постоянным и необратимым. [5]
Для гибридизационной гистохимии образцы клеток и тканей обычно обрабатывают, чтобы зафиксировать целевые транскрипты на месте и улучшить доступ зонда. Как отмечалось выше, зонд представляет собой либо меченую комплементарную ДНК , либо, что сейчас чаще всего, комплементарную РНК ( рибозонд ). Зонд гибридизуется с целевой последовательностью при повышенной температуре, а затем избыток зонда смывается (после предварительного гидролиза с использованием РНКазы в случае негибридизированного зонда с избытком РНК). Параметры раствора, такие как температура, соль и/или концентрация детергента, можно манипулировать для устранения любых неидентичных взаимодействий (т. е. только точные совпадения последовательностей останутся связанными). Затем зонд, который был помечен радио-, флуоресцентно- или антиген-мечеными основаниями (например, дигоксигенином ), локализуется и количественно определяется в ткани с помощью авторадиографии , флуоресцентной микроскопии или иммуногистохимии соответственно. ISH также может использовать два или более зондов, помеченных радиоактивностью или другими нерадиоактивными метками, для одновременного обнаружения двух или более транскриптов.
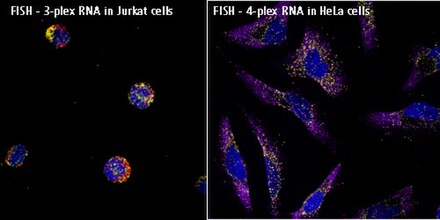
Альтернативная технология, анализ разветвленной ДНК , может быть использована для анализа РНК (мРНК, днРНК и микроРНК) in situ в анализах гибридизации с чувствительностью к одной молекуле без использования радиоактивности. Этот подход (например, анализы ViewRNA) можно использовать для визуализации до четырех мишеней в одном анализе, и он использует запатентованную конструкцию зонда и амплификацию сигнала бДНК для генерации чувствительных и специфичных сигналов. Образцы (клетки, ткани и ЦОК) фиксируются, затем обрабатываются, чтобы обеспечить доступность мишени РНК (демаскировка РНК). Целенаправленные зонды гибридизуются с каждой целевой РНК. Последующая амплификация сигнала основана на специфической гибридизации соседних зондов (отдельных олигонуклеотидов [олиго], которые бок о бок связываются с мишенями РНК). Типичный зонд, специфичный для мишени, будет содержать 40 олигонуклеотидов, в результате чего образуется 20 пар олигонуклеотидов, которые бок о бок связываются с мишенью для обнаружения мРНК и днРНК, а также 2 олигонуклеотида или одна пара для обнаружения микроРНК. Усиление сигнала достигается посредством серии последовательных этапов гибридизации. Молекула предварительного усилителя гибридизуется с каждой парой олигонуклеотидов на целевой РНК, затем несколько молекул усилителя гибридизуются с каждым предусилителем. Затем олигонуклеотиды с несколькими метками-зондами (конъюгированные с щелочной фосфатазой или непосредственно с флуорофорами) гибридизуются с каждой молекулой усилителя. Полностью собранная структура усиления сигнала «Дерево» имеет 400 мест связывания для зондов-меток. Когда все мишене-специфичные зонды связываются с целевым транскриптом мРНК, для этого одного транскрипта происходит 8000-кратная амплификация сигнала. Отдельные, но совместимые системы усиления сигнала позволяют проводить мультиплексные анализы. Сигнал можно визуализировать с помощью флуоресцентного или светлопольного микроскопа.
Протокол занимает около 2–3 дней и требует некоторого времени для настройки. Некоторые компании продают роботов для автоматизации процесса (например, CEM InsituPro). В результате в лабораториях были проведены масштабные проверки тысяч генов. Доступ к результатам обычно можно получить через веб-сайты (см. внешние ссылки). [6]