ДНК-лигаза — это тип фермента, который облегчает соединение цепей ДНК , катализируя образование фосфодиэфирной связи . Он играет роль в восстановлении одноцепочечных разрывов дуплексной ДНК в живых организмах, но некоторые формы (например, ДНК-лигаза IV ) могут специфически восстанавливать двухцепочечные разрывы (т.е. разрыв обеих комплементарных цепей ДНК). Однонитевые разрывы восстанавливаются с помощью ДНК-лигазы, используя комплементарную цепь двойной спирали в качестве матрицы [1] , при этом ДНК-лигаза создает конечную фосфодиэфирную связь для полного восстановления ДНК.
ДНК-лигаза используется как для репарации ДНК , так и для репликации ДНК (см. Лигазы млекопитающих ). Кроме того, ДНК-лигаза широко используется в лабораториях молекулярной биологии для экспериментов по рекомбинантной ДНК (см. «Исследовательские применения »). Очищенная ДНК-лигаза используется при клонировании генов для соединения молекул ДНК с образованием рекомбинантной ДНК .
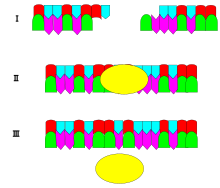
Механизм ДНК-лигазы заключается в образовании двух ковалентных фосфодиэфирных связей между 3'-гидроксильными концами одного нуклеотида («акцептор») и 5'-фосфатным концом другого («донор»). На каждую образовавшуюся фосфодиэфирную связь расходуются две молекулы АТФ. [ нужна цитация ] AMP необходим для лигазной реакции, которая протекает в четыре этапа:
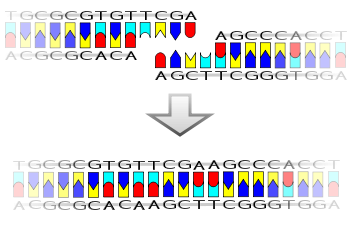
Лигаза также будет работать с тупыми концами , хотя требуются более высокие концентрации фермента и другие условия реакции.
ДНК -лигаза E. coli кодируется геном lig . ДНК-лигаза в E. coli , как и у большинства прокариот, использует энергию, полученную при расщеплении никотинамидадениндинуклеотида (НАД), для создания фосфодиэфирной связи. [3] Он не лигирует ДНК с тупыми концами, за исключением условий молекулярной скученности полиэтиленгликолем , и не может эффективно соединять РНК с ДНК. [ нужна цитата ]
Активность ДНК-лигазы E. coli может быть усилена ДНК-полимеразой в правильных концентрациях. Усиление работает только тогда, когда концентрации ДНК-полимеразы 1 намного ниже, чем концентрации фрагментов ДНК, подлежащих лигированию. Повышение концентрации ДНК-полимераз Pol I оказывает неблагоприятное воздействие на ДНК-лигазу E. coli [4].
ДНК-лигаза бактериофага Т4 ( бактериофага , инфицирующего бактерии Escherichia coli ). Лигаза Т4 наиболее часто используется в лабораторных исследованиях. [5] Он может лигировать как слипшиеся, так и тупые концы ДНК, олигонуклеотиды, а также гибриды РНК и РНК-ДНК, но не одноцепочечные нуклеиновые кислоты. Он также может лигировать ДНК с тупыми концами с гораздо большей эффективностью, чем ДНК-лигаза E. coli . В отличие от ДНК-лигазы E. coli , ДНК-лигаза Т4 не может использовать НАД и абсолютно необходима АТФ в качестве кофактора. Были проведены некоторые инженерные разработки для улучшения активности ДНК-лигазы Т4 in vitro ; один успешный подход, например, протестировал ДНК-лигазу Т4, слитую с несколькими альтернативными ДНК-связывающими белками, и обнаружил, что конструкции с p50 или NF-kB в качестве партнеров слияния были более чем на 160% более активны при лигировании тупых концов для целей клонирования, чем конструкции дикого типа. ДНК-лигаза Т4. [6] В типичной реакции вставки фрагмента в плазмидный вектор используется от 0,01 (липкие концы) до 1 (тупые концы) единицы лигазы. Оптимальная температура инкубации ДНК-лигазы Т4 составляет 16 °С. [ нужна цитата ]
Мутанты лигазы бактериофага Т4 обладают повышенной чувствительностью как к УФ- облучению [7] [8], так и к алкилирующему агенту метилметансульфонату [9] , что указывает на то, что ДНК-лигаза используется для восстановления повреждений ДНК , вызванных этими агентами.
У млекопитающих существует четыре конкретных типа лигазы.
ДНК-лигаза эукариот и некоторых микробов использует аденозинтрифосфат (АТФ), а не НАД. [3]
Полученный из термофильной бактерии, фермент стабилен и активен при гораздо более высоких температурах, чем обычные ДНК-лигазы. Период его полураспада составляет 48 часов при 65°С и более 1 часа при 95°С. Было показано, что амплигаза ДНК-лигаза активна в течение как минимум 500 термических циклов (94 °C/80 °C) или 16 часов езды на велосипеде. 10 Эта исключительная термостабильность обеспечивает чрезвычайно высокую строгость гибридизации и специфичность лигирования. [11]
Для измерения активности ДНК-лигазы используются как минимум три различных единицы: [12]
ДНК-лигазы стали незаменимыми инструментами в современных молекулярно-биологических исследованиях для создания рекомбинантных последовательностей ДНК. Например, ДНК-лигазы используются с ферментами рестрикции для вставки фрагментов ДНК, часто генов , в плазмиды .
Контроль оптимальной температуры является жизненно важным аспектом проведения эффективных экспериментов по рекомбинации, включающих лигирование фрагментов со слипшимися концами. В большинстве экспериментов используется ДНК-лигаза Т4 (выделенная из бактериофага Т4 ), которая наиболее активна при 37 °C. [13] Однако для оптимальной эффективности лигирования фрагментов со слипшимися концами («липкие концы») оптимальная температура фермента должна быть сбалансирована с температурой плавления T m лигируемых липких концов, [14] гомологичным спариванием липкие концы не будут стабильными, поскольку высокая температура разрушает водородные связи . Реакция лигирования наиболее эффективна, когда липкие концы уже стабильно отожжены, и поэтому разрушение отжигаемых концов может привести к низкой эффективности лигирования. Чем короче свес , тем ниже T m .
Поскольку фрагменты ДНК с тупыми концами не имеют сцепленных концов, которые можно было бы отжигать, температура плавления не является фактором, который следует учитывать в нормальном температурном диапазоне реакции лигирования. Ограничивающим фактором при лигировании тупых концов является не активность лигазы, а количество происходящих выравниваний между концами фрагментов ДНК. Таким образом, наиболее эффективной температурой лигирования ДНК с тупыми концами будет температура, при которой может произойти наибольшее количество выравниваний. Большинство перевязок с тупыми концами проводят при температуре 14–25 °C в течение ночи. Отсутствие стабильно отожженных концов также означает, что эффективность лигирования снижается, что требует использования более высокой концентрации лигазы. [14]
Новое применение ДНК-лигазы можно увидеть в области нанохимии, особенно в ДНК-оригами. Принципы самосборки, основанные на ДНК, оказались полезными для организации наноразмерных объектов, таких как биомолекулы, наномашины, наноэлектронные и фотонные компоненты. Сборка такой наноструктуры требует создания сложной сети молекул ДНК. Хотя самосборка ДНК возможна без какой-либо внешней помощи с использованием различных субстратов, таких как кататоническая поверхность алюминиевой фольги, ДНК-лигаза может оказать ферментативную помощь, необходимую для создания решетчатой структуры ДНК из остатков ДНК. [15]
Первая ДНК-лигаза была очищена и охарактеризована в 1967 году лабораториями Геллерта, Лемана, Ричардсона и Гурвица. [16] Впервые он был очищен и охарактеризован Вайсом и Ричардсоном с использованием шестиэтапного процесса хроматографического фракционирования, начинающегося с удаления клеточного мусора и добавления стрептомицина, за которым следовали несколько промывок колонки с диэтиламиноэтил (DEAE)-целлюлозой и окончательное фракционирование фосфоцеллюлозы. Конечный экстракт содержал 10% активности, первоначально зафиксированной в среде E. coli ; В ходе процесса было обнаружено, что АТФ и Mg++ необходимы для оптимизации реакции. Обычные коммерчески доступные ДНК-лигазы были первоначально обнаружены в бактериофаге Т4 , E.coli и других бактериях . [17]
Генетические дефициты ДНК-лигаз человека связаны с клиническими синдромами, характеризующимися иммунодефицитом, чувствительностью к радиации и аномалиями развития. [16] Синдром LIG4 (синдром лигазы IV) представляет собой редкое заболевание, связанное с мутациями ДНК-лигазы 4 и препятствующее разрыву дцДНК. ремонтные механизмы. Синдром лигазы IV вызывает у людей иммунодефицит и обычно связан с микроцефалией и гипоплазией костного мозга. [18] Список распространенных заболеваний, вызванных отсутствием или нарушением работы ДНК-лигазы, выглядит следующим образом.
Пигментная ксеродерма, широко известная как XP, представляет собой наследственное заболевание, характеризующееся крайней чувствительностью к ультрафиолетовым (УФ) лучам солнечного света. Это заболевание чаще всего поражает глаза и участки кожи, подвергающиеся воздействию солнца. У некоторых пострадавших также наблюдаются проблемы с нервной системой. [19]
Мутации в гене ATM вызывают атаксию-телеангиэктазию . Ген ATM дает инструкции по созданию белка, который помогает контролировать деление клеток и участвует в восстановлении ДНК. Этот белок играет важную роль в нормальном развитии и деятельности ряда систем организма, включая нервную и иммунную системы. Белок АТМ помогает клеткам распознавать поврежденные или сломанные цепи ДНК и координирует восстановление ДНК, активируя ферменты, которые восстанавливают сломанные цепи. Эффективное восстановление поврежденных цепей ДНК помогает поддерживать стабильность генетической информации клетки. У больных детей обычно возникают трудности при ходьбе, проблемы с равновесием и координацией рук, непроизвольные подергивания (хорея), мышечные подергивания (миоклонус) и нарушения функции нервов (нейропатия). Проблемы с передвижением обычно приводят к тому, что в подростковом возрасте людям требуется помощь инвалидной коляски. Люди с этим расстройством также имеют невнятную речь и проблемы с перемещением глаз, чтобы посмотреть из стороны в сторону (глазодвигательная апраксия). [20]
Анемия Фанкони (АФ) — редкое наследственное заболевание крови, приводящее к недостаточности костного мозга. FA не позволяет костному мозгу производить достаточно новых клеток крови, чтобы организм мог нормально работать. FA также может привести к тому, что костный мозг выработает много дефектных клеток крови. Это может привести к серьезным проблемам со здоровьем, например, лейкемии . [21]
Синдром Блума приводит к тому, что кожа становится чувствительной к воздействию солнечных лучей, и обычно к появлению пятен покрасневшей кожи в форме бабочки на носу и щеках. Кожная сыпь может также появиться на других участках, которые обычно подвергаются воздействию солнца, например, на тыльной стороне кистей и предплечьях. В сыпи часто появляются небольшие скопления расширенных кровеносных сосудов (телеангиэктазии); телеангиэктазии также могут возникать в глазах. Другие особенности кожи включают участки кожи, которые светлее или темнее окружающих участков (гипопигментация или гиперпигментация соответственно). Эти пятна появляются на участках кожи, не подвергающихся воздействию солнца, и их развитие не связано с высыпаниями.
В недавних исследованиях ДНК-лигаза I человека использовалась в компьютерной разработке лекарств для идентификации ингибиторов ДНК-лигазы в качестве возможных терапевтических средств для лечения рака. [22] Поскольку чрезмерный рост клеток является признаком развития рака, таргетная химиотерапия, которая нарушает функционирование ДНК-лигазы, может препятствовать адъювантным формам рака. Кроме того, было показано, что ДНК-лигазы можно разделить на две категории, а именно АТФ- и НАД + -зависимые. Предыдущие исследования показали, что, хотя НАД + -зависимые ДНК-лигазы были обнаружены в спорадических клеточных или вирусных нишах за пределами бактериальной области жизни, не существует ни одного случая, когда НАД + -зависимая лигаза присутствовала бы в эукариотическом организме. Наличие исключительно у неэукариотических организмов, уникальная субстратная специфичность и отличительная доменная структура НАД+-зависимых по сравнению с АТФ-зависимыми ДНК-лигаз человека в совокупности делают НАД + -зависимые лигазы идеальными мишенями для разработки новых антибактериальных препаратов. [16]