

Пиретроид — органическое соединение , подобное природным пиретринам , которые вырабатываются цветками пиретрумов ( Chrysanthemum cinerariaefolium и C. coccineum ). Пиретроиды используются в качестве коммерческих и бытовых инсектицидов . [1]
В домашних условиях пиретроиды обычно безвредны для человека. [1] Однако пиретроиды токсичны для таких насекомых, как пчелы , стрекозы , подёнки , оводы и некоторые другие беспозвоночные , в том числе те, которые составляют основу водных и наземных пищевых сетей . [2] Пиретроиды токсичны для водных организмов , особенно рыб. [3] Было доказано, что они являются эффективной мерой борьбы со вспышками малярии при использовании внутри помещений. [4]
Пиретроиды эксайтотоксичны для аксонов . Они действуют, предотвращая закрытие потенциалзависимых натриевых каналов в аксональных мембранах . Натриевый канал представляет собой мембранный белок с гидрофильной внутренней частью. Эта внутренняя часть имеет такую форму, которая позволяет ионам натрия проходить через мембрану, проникать в аксон и распространять потенциал действия . Когда токсин удерживает каналы в открытом состоянии, нервы не могут реполяризоваться , оставляя аксональную мембрану навсегда деполяризованной , тем самым парализуя организм. [5] Пиретроиды можно комбинировать с синергистом пиперонилбутоксидом , известным ингибитором микросомальных ферментов P450 , которые играют важную роль в метаболизме пиретроида. Таким образом, эффективность (летальность) пиретроида увеличивается. [6] Вероятно, существуют и другие механизмы интоксикации. [7] Считается, что нарушение нейроэндокринной активности способствует их необратимому воздействию на насекомых, что указывает на действие пиретроидов на потенциал-управляемые кальциевые каналы (и, возможно, на другие потенциал-управляемые каналы в более широком смысле). [7]
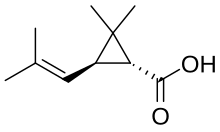
Пиретроиды классифицируются по механизму биологического действия, поскольку они не имеют общей химической структуры. Многие из них представляют собой производные 2,2-диметилциклопропанкарбоновой кислоты, такие как хризантемовая кислота , этерифицированные спиртом . Однако циклопропильное кольцо встречается не во всех пиретроидах. Фенвалерат , разработанный в 1972 году, является одним из таких примеров и первым коммерческим пиретроидом без этой группы.
Пиретроиды, у которых отсутствует α-цианогруппа, часто классифицируются как пиретроиды типа I , а те, у которых она есть, называются пиретроидами типа II . Пиретроиды, общее название которых начинается с «cy», содержат цианогруппу и относятся к типу II. Фенвалерат также содержит α- цианогруппу .
Некоторые пиретроиды, такие как этофенпрокс , также не имеют эфирной связи, присутствующей в большинстве других пиретроидов, и вместо нее имеют эфирную связь. Силафлуофен также классифицируется как пиретроид и имеет атом кремния вместо сложного эфира. Пиретроиды часто имеют хиральные центры , и только некоторые стереоизомеры эффективно действуют как инсектициды . [8]
Пиретроиды токсичны для таких насекомых, как пчелы , стрекозы , подёнки , оводы и некоторых других беспозвоночных , в том числе тех, которые составляют основу водных и наземных пищевых сетей . [2] Они токсичны для водных организмов, включая рыбу. [3]
Пиретроиды обычно распадаются под действием солнечного света и атмосферы за один или два дня, однако, когда они связаны с отложениями, они могут сохраняться в течение некоторого времени. [9]
На пиретроиды не влияют обычные системы вторичной очистки городских очистных сооружений. Они появляются в сточных водах, обычно в количествах, смертельных для беспозвоночных. [10]
Абсорбция пиретроида может происходить через кожу, при вдыхании или проглатывании. [11] Пиретроиды часто неэффективно связываются с натриевыми каналами млекопитающих . [12] Они также плохо всасываются через кожу, а печень человека часто способна метаболизировать их относительно эффективно. Таким образом, пиретроиды гораздо менее токсичны для человека, чем для насекомых. [13]
Не совсем точно установлено, является ли хроническое воздействие небольших количеств пиретроидов опасным или нет. [14] Однако большие дозы могут вызвать острое отравление, которое редко представляет угрозу для жизни. Типичные симптомы включают парестезию лица , зуд, жжение, головокружение, тошноту, рвоту и более тяжелые случаи подергивания мышц. Тяжелое отравление часто вызывается приемом пиретроидов и может привести к различным симптомам, таким как судороги, кома , кровотечение или отек легких . [11] Существует связь пиретроидов с более плохим ранним социально-эмоциональным и языковым развитием. [4]
Пиретроиды очень токсичны для кошек , но не для собак . Отравление у кошек может привести к судорогам, лихорадке, атаксии и даже смерти. Отравление может возникнуть при применении на кошках пиретроидсодержащих средств от блох , предназначенных для собак. Печень кошек хуже детоксицирует пиретроиды посредством глюкуронидации , чем собаки, что и является причиной такого различия. [15] За исключением кошек, пиретроиды обычно не токсичны для млекопитающих и птиц . [16] Они часто токсичны для рыб , рептилий и амфибий . [17]
Использование пиретроидов в качестве инсектицидов привело к развитию широко распространенной устойчивости к ним среди некоторых популяций насекомых, особенно комаров. [18] Хотя в Северной Америке клопы были практически уничтожены благодаря использованию ДДТ и органофосфатов , появились популяции клопов, устойчивых к обоим препаратам. Использование ДДТ для этой цели было запрещено, а его повторное внедрение не могло решить проблему клопов из-за резистентности. [19] Пиретроиды стали более широко использоваться против клопов, но теперь к ним также появились устойчивые популяции. [20] [21] [22] [23] Популяции бабочек Diamondback также часто развивают устойчивость к пиретроидам [24] [ нужен лучший источник ] – в том числе в штатах США Северная Дакота [25] и Висконсин [26], хотя пиретроиды все еще используются рекомендуется в Калифорнии . [27] Было обнаружено, что различные популяции комаров обладают высоким уровнем устойчивости, в том числе Anopheles gambiae sl в Западной Африке (Chandre et al 1999) по Pwalia et al 2019, A. arabiensis в Судане (Ismail et al 2018) и в Гамбии (Opondo). и др., 2019 г., и Aedes aegypti в Юго-Восточной Азии, автор Амелия-Яп и др., 2018 г., Папуа-Новая Гвинея , автор Демок и др., 2019 г., и в различных других местах, автор Смит и др., 2016 г. [18]
Сопротивление нокдауну ( kdr ) — один из самых сильных видов сопротивления. [28] Мутации kdr придают сайту-мишени устойчивость к ДДТ и пиретроидам, а также перекрестную устойчивость к ДДТ. [28] Большинство мутаций kdr находятся внутри или вблизи двух генов натриевых каналов членистоногих . [28]
Пиретроиды были введены группой ученых Rothamsted Research в 1960-х и 1970-х годах после выяснения структур пиретрина I и II Германом Штаудингером и Леопольдом Ружичкой в 1920-х годах. [29] Пиретроиды представляли собой важное достижение в химии, позволившее синтезировать аналог природной версии, обнаруженной в пиретруме . Его инсектицидная активность имеет относительно низкую токсичность для млекопитающих и необычайно быстрое биоразложение. Их разработка совпала с выявлением проблем с использованием ДДТ . Их работа заключалась, во-первых, в выявлении наиболее активных компонентов пиретрума , извлеченного из цветков восточноафриканской хризантемы и давно известного своими инсектицидными свойствами. Пиретрум быстро уничтожает летающих насекомых, но обладает незначительной стойкостью, что полезно для окружающей среды, но дает низкую эффективность при применении в полевых условиях. Пиретроиды по существу представляют собой химически стабилизированные формы природного пиретрума и относятся к группе IRAC MoA 3 (они препятствуют транспорту натрия в нервных клетках насекомых). [30]
Пиретроиды первого поколения , разработанные в 1960-х годах, включают биоаллетрин , тетраметрин , ресметрин и биоресметрин. Они более активны, чем природный пиретрум, но нестабильны на солнечном свете. После пересмотра 91/414/EEC [31] многие соединения 1-го поколения не были включены в Приложение 1, вероятно, потому, что рынок недостаточно велик, чтобы оправдать затраты на перерегистрацию (а не какие-либо особые опасения по поводу безопасности). .
К 1974 году команда Ротамстеда открыла второе поколение более стойких соединений, а именно: перметрин , циперметрин и дельтаметрин . Они значительно более устойчивы к разложению под действием света и воздуха, что делает их пригодными для использования в сельском хозяйстве , но они обладают значительно более высокой токсичностью для млекопитающих. В последующие десятилетия за этими производными последовали другие запатентованные соединения, такие как фенвалерат , лямбда-цигалотрин и бета- цифлутрин . Срок действия большинства патентов уже истек, что делает эти соединения дешевыми и, следовательно, популярными (хотя перметрин и фенвалерат не были перерегистрированы в соответствии с процессом 91/414/EEC).