
Мутация со сдвигом рамки считывания (также называемая ошибкой кадрирования или сдвигом рамки считывания ) — это генетическая мутация, вызванная инделами ( вставками или делециями ) ряда нуклеотидов в последовательности ДНК, которая не делится на три. Из-за триплетной природы экспрессии генов кодонами вставка или делеция может изменить рамку считывания (группировку кодонов), что приведет к совершенно иной трансляции по сравнению с оригиналом. Чем раньше в последовательности происходит делеция или вставка, тем больше изменяется белок. [1] Мутация со сдвигом рамки считывания — это не то же самое, что полиморфизм одного нуклеотида , при котором нуклеотид заменяется, а не вставляется или удаляется. Мутация со сдвигом рамки считывания в целом приведет к тому, что считывание кодонов после мутации будет кодировать разные аминокислоты. Мутация со сдвигом рамки считывания также изменит первый стоп-кодон («UAA», «UGA» или «UAG»), встречающийся в последовательности. Создаваемый полипептид может быть аномально коротким или аномально длинным и, скорее всего, не будет функциональным. [2]
Мутации со сдвигом рамки считывания очевидны при тяжелых генетических заболеваниях, таких как болезнь Тея-Сакса ; они повышают восприимчивость к определенным видам рака и классам семейной гиперхолестеринемии ; в 1997 году [3] мутация со сдвигом рамки считывания была связана с устойчивостью к инфицированию ретровирусом ВИЧ. Мутации со сдвигом рамки считывания были предложены в качестве источника биологической новизны, как и в случае с предполагаемым созданием нейлоназы , однако эта интерпретация является спорной. Исследование Негоро и др. (2006) [4] показало, что мутация со сдвигом рамки считывания вряд ли была причиной, и что скорее замена двух аминокислот в активном центре предковой эстеразы привела к нейлоназе.
Информация, содержащаяся в ДНК, определяет функцию белка в клетках всех организмов. Транскрипция и трансляция позволяют передавать эту информацию для создания белков. Однако ошибка в прочтении этой информации может привести к неправильной функции белка и в конечном итоге вызвать заболевание, даже если клетка применяет различные корректирующие меры. Генетическая информация передается ДНК для синтеза белка в клетках. Неправильная интерпретация может привести к неправильной функции и заболеванию, несмотря на клеточные механизмы коррекции.
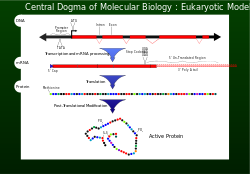
В 1956 году Фрэнсис Крик описал поток генетической информации от ДНК к определенному расположению аминокислот для создания белка как центральную догму. [1] Для того, чтобы клетка правильно функционировала, белки должны быть произведены точно для структурной и каталитической активности. Неправильно созданный белок может иметь пагубные последствия для жизнеспособности клетки и в большинстве случаев привести к тому, что высший организм станет нездоровым из-за ненормальных клеточных функций. Чтобы гарантировать, что геном успешно передает информацию, в репликацию ДНК включены механизмы корректуры , такие как экзонуклеазы и системы исправления несоответствий . [1]

После репликации ДНК считывание выбранного раздела генетической информации осуществляется путем транскрипции . [1] Нуклеотиды, содержащие генетическую информацию, теперь находятся на одноцепочечной матрице-мессенджере, называемой мРНК . мРНК включена в субъединицу рибосомы и взаимодействует с рРНК . Генетическая информация, содержащаяся в кодонах мРНК, теперь считывается (декодируется) антикодонами тРНК. По мере считывания каждого кодона (триплета) аминокислоты соединяются до тех пор, пока не будет достигнут стоп-кодон (UAG, UGA или UAA). В этот момент полипептид (белок) синтезируется и высвобождается. [1] На каждые 1000 аминокислот, включенных в белок, не более одной является неправильной. Такая точность распознавания кодонов, сохраняющая важность правильной рамки считывания, достигается за счет правильного спаривания оснований на участке рибосомы А, активности гидролиза ГТФ EF-Tu (формы кинетической стабильности) и механизма корректуры при высвобождении EF-Tu. [1]
Сдвиг рамки может также происходить во время профазы трансляции, производя различные белки из перекрывающихся открытых рамок считывания, таких как ретровирусные белки gag-pol-env . Это довольно распространено у вирусов , а также встречается у бактерий и дрожжей (Farabaugh, 1996). Обратная транскриптаза , в отличие от РНК-полимеразы II , считается более сильной причиной возникновения мутаций со сдвигом рамки. В экспериментах только 3–13% всех мутаций со сдвигом рамки произошли из-за РНК-полимеразы II. У прокариот частота ошибок, вызывающих мутации со сдвигом рамки, находится всего лишь где-то в диапазоне от 0,0001 до 0,00001. [5]
Существует несколько биологических процессов, которые помогают предотвратить мутации со сдвигом рамки. Происходят обратные мутации, которые изменяют мутированную последовательность обратно к исходной последовательности дикого типа . Другая возможность исправления мутации — использование супрессорной мутации . Это компенсирует эффект исходной мутации, создавая вторичную мутацию, сдвигая последовательность, чтобы позволить считывать правильные аминокислоты. Направляющая РНК также может использоваться для вставки или удаления уридина в мРНК после транскрипции, это позволяет получить правильную рамку считывания. [1]

Кодон — это набор из трех нуклеотидов , триплет, который кодирует определенную аминокислоту . Первый кодон устанавливает рамку считывания, посредством которой начинается новый кодон. Последовательность аминокислотной основы белка определяется смежными триплетами. [6] Кодоны играют ключевую роль в трансляции генетической информации для синтеза белков. Рамка считывания устанавливается, когда начинается трансляция мРНК, и сохраняется по мере считывания одного триплета к другому. Чтение генетического кода подчиняется трем правилам, которые отслеживают кодоны в мРНК. Во-первых, кодоны считываются в направлении от 5' к 3'. Во-вторых, кодоны не перекрываются, и сообщение не имеет пробелов. Последнее правило, как указано выше, заключается в том, что сообщение транслируется в фиксированной рамке считывания. [1]

Мутации со сдвигом рамки считывания могут возникать случайно или быть вызваны внешним стимулом. Обнаружение мутаций со сдвигом рамки считывания может происходить несколькими различными методами. Сдвиги рамки считывания — это всего лишь один тип мутаций, который может привести к неполным или неправильным белкам, но они составляют значительный процент ошибок в ДНК. В неизмененном гене кодоны (триплеты нуклеотидов) последовательно интерпретируются, причем каждый кодон кодирует определенную аминокислоту. Это известно как стандартная рамка считывания. Однако в случаях мутаций со сдвигом рамки считывания в последовательность ДНК вставляется дополнительный нуклеотид (или больше), нарушая типичную рамку считывания и вызывая сдвиг в последовательности.
Эта вставка вызывает сдвиг в рамке считывания из-за триплетной природы генетического кода. Например, добавление дополнительной «A» приводит к сдвигу последовательности, запуская считывание совершенно другого набора кодонов. Это отклонение в генетической информации заставляет рибосому, которая считывает мРНК для синтеза белка, неправильно интерпретировать генетические данные. Следовательно, генерируется совершенно другой ряд аминокислот, что приводит к генерации измененной последовательности белка. В большинстве случаев новая рамка считывания приводит к ранней встрече со стоп-кодоном, что приводит к образованию укороченного и обычно неактивного белка. Эта форма мутации называется ранним стоп-кодоном или бессмысленной мутацией.
Это генетическая мутация на уровне нуклеотидных оснований. Почему и как происходят мутации со сдвигом рамки считывания, постоянно ищут. Было проведено экологическое исследование, в частности, производство мутаций со сдвигом рамки считывания, вызванных УФ- излучением, ДНК-полимеразами с дефицитом 3′ → 5′ экзонуклеазной активности. Нормальная последовательность 5′ GTC GTT TTA CAA 3′ была изменена на GTC GTT T TTA CAA (MIDT) из GTC GTT C TTA CAA (MIDC) для изучения сдвигов рамки считывания. Мутантные ферменты ДНК-полимеразы E. coli pol I Kf и T7 , лишенные 3′ → 5′ экзонуклеазной активности, производят ревертанты, вызванные УФ-излучением, с более высокой частотой, чем их аналоги, обладающие экзонуклеазной активностью. Данные показывают, что потеря корректурной активности увеличивает частоту сдвигов рамки считывания, вызванных УФ-излучением. [7]
Эффекты соседних оснований и вторичной структуры для обнаружения частоты мутаций сдвига рамки были подробно исследованы с использованием флуоресценции . Флуоресцентно маркированная ДНК с помощью аналогов оснований позволяет изучать локальные изменения последовательности ДНК. [8] Исследования эффектов длины цепи праймера показывают, что равновесная смесь четырех конформаций гибридизации наблюдалась, когда основания шаблона вытягивались в виде выпуклости, т. е. структуры, фланкированной с обеих сторон дуплексной ДНК. Напротив, двухпетлевая структура с необычной неуложенной конформацией ДНК на ее нисходящем крае наблюдалась, когда выдвинутые основания располагались на стыке праймера и шаблона, показывая, что несоответствия могут быть изменены соседней вторичной структурой ДНК. [9]
.jpg/440px-Frameshift_deletion_(13062713935).jpg)
Секвенирование по Сэнгеру и пиросеквенирование — два метода, которые использовались для обнаружения мутаций со сдвигом рамки считывания, однако, вероятно, что полученные данные не будут самого высокого качества. Тем не менее, 1,96 миллиона инделей были идентифицированы с помощью секвенирования по Сэнгеру, которые не пересекаются с другими базами данных. Когда наблюдается мутация со сдвигом рамки считывания, ее сравнивают с Базой данных мутаций генома человека (HGMD), чтобы определить, оказывает ли мутация повреждающее воздействие. Это делается путем рассмотрения четырех характеристик. Во-первых, соотношения между затронутой и сохраненной ДНК, во-вторых, местоположения мутации относительно транскрипта, в-третьих, соотношения сохраненных и затронутых аминокислот и, наконец, расстояния от инделя до конца экзона . [ 10]
Массовое параллельное секвенирование — это новый метод, который можно использовать для обнаружения мутаций. Используя этот метод, можно секвенировать до 17 гигабаз одновременно, в отличие от ограниченных диапазонов для секвенирования по Сэнгеру, которые составляют всего около 1 килобазы. Для выполнения этого теста доступно несколько технологий, и его рассматривают для использования в клинических приложениях. [11] При тестировании на различные карциномы современные методы позволяют просматривать только один ген за раз. Массовое параллельное секвенирование может одновременно тестировать на различные мутации, вызывающие рак, в отличие от нескольких конкретных тестов. [12] Эксперимент по определению точности этого нового метода секвенирования протестировал 21 ген и не дал ложноположительных результатов для мутаций со сдвигом рамки считывания. [13]
Патент США (5,958,684) от 1999 года, выданный Leeuwen, подробно описывает методы и реагенты для диагностики заболеваний, вызванных или связанных с геном, имеющим соматическую мутацию, приводящую к мутации со сдвигом рамки. Методы включают предоставление образца ткани или жидкости и проведение генного анализа на мутацию со сдвигом рамки или белка из этого типа мутации. Нуклеотидная последовательность подозреваемого гена предоставляется из опубликованных последовательностей генов или из клонирования и секвенирования подозреваемого гена. Затем предсказывается аминокислотная последовательность, кодируемая геном. [14] Секвенирование NA: секвенирование по Сэнгеру или секвенирование следующего поколения (NGS) можно использовать для прямого секвенирования ДНК и выявления вставок или делеций. Полимеразная цепная реакция (ПЦР): ПЦР можно использовать для амплификации определенной области, содержащей мутацию, для последующего анализа. Мультиплексная лигированно-зависимая амплификация зонда (MLPA): MLPA — это метод, используемый для обнаружения вариаций числа копий и небольших вставок или делеций. Сравнительная геномная гибридизация (CGH): CGH используется для обнаружения хромосомных дисбалансов, которые могут включать крупные вставки или делеции.
Несмотря на правила, которые управляют генетическим кодом и различными механизмами, присутствующими в клетке для обеспечения правильной передачи генетической информации в процессе репликации ДНК, а также во время трансляции, мутации все же происходят; мутация со сдвигом рамки считывания — не единственный тип. Существует по крайней мере два других типа распознаваемых точечных мутаций, в частности, миссенс-мутация и нонсенс-мутация . [1] Мутация со сдвигом рамки считывания может радикально изменить кодирующую способность (генетическую информацию) сообщения. [1] Небольшие вставки или делеции (менее 20 пар оснований) составляют 24% мутаций, которые проявляются в распознаваемых в настоящее время генетических заболеваниях. [10]
Мутации со сдвигом рамки считывания, как оказалось, чаще встречаются в повторяющихся областях ДНК. Причиной этого является проскальзывание фермента полимеразы в повторяющихся областях, что позволяет мутациям проникать в последовательность . [15] Эксперименты могут быть проведены для определения частоты мутации со сдвигом рамки считывания путем добавления или удаления заранее заданного количества нуклеотидов. Эксперименты проводились путем добавления четырех пар оснований, называемых экспериментами +4, но группа из Университета Эмори рассмотрела разницу в частоте мутации как путем добавления, так и путем удаления пары оснований. Было показано, что не было никакой разницы в частоте между добавлением и удалением пары оснований. Однако есть разница в результате белка. [15]
Болезнь Хантингтона является одним из девяти нарушений повторения кодонов, вызванных мутациями полиглутаминовой экспансии, которые включают спино-церебеллярную атаксию (SCA) 1, 2, 6, 7 и 3, спинобульбарную мышечную атрофию и дентаторубально-паллидолуизианотрофию. Может существовать связь между заболеваниями, вызванными мутациями полиглутамина и полиаланина, как сдвиг рамки исходного продукта гена SCA3, кодирующего CAG/полиглутамины, на GCA/полиаланины. Рибосомное проскальзывание во время трансляции белка SCA3 было предложено как механизм, приводящий к сдвигу с рамки, кодирующей полиглутамин, на рамку, кодирующую полиаланин. Делеция динуклеотида или вставка одного нуклеотида в полиглутаминовый тракт экзона 1 хантингтина сместит CAG, кодирующую рамку полиглутамина, на +1 (сдвиг рамки +1) к GCA, кодирующей рамку полиаланина, и введет новый эпитоп в C-конец экзона 1 Htt (APAAAPAATRPGCG). [16]
Несколько заболеваний имеют мутации со сдвигом рамки считывания как по крайней мере часть причины. Знание распространенных мутаций также может помочь в диагностике заболевания. В настоящее время предпринимаются попытки использовать мутации со сдвигом рамки считывания с пользой для лечения заболеваний, изменяя рамку считывания аминокислот.


Известно, что мутации со сдвигом рамки являются фактором колоректального рака, а также других видов рака с нестабильностью микросателлитов . Как было сказано ранее, мутации со сдвигом рамки чаще возникают в области повторяющейся последовательности. Когда репарация несоответствий ДНК не фиксирует добавление или удаление оснований, эти мутации с большей вероятностью будут патогенными. Это может быть отчасти связано с тем, что опухоль не получает команду прекратить рост. Эксперименты на дрожжах и бактериях помогают выявить характеристики микросателлитов, которые могут способствовать дефектному репарированию несоответствий ДНК. К ним относятся длина микросателлита , состав генетического материала и чистота повторов. Согласно экспериментальным результатам, более длинные микросателлиты имеют более высокую частоту мутаций со сдвигом рамки. Фланговая ДНК также может способствовать мутациям со сдвигом рамки. [17] При раке предстательной железы мутация со сдвигом рамки изменяет открытую рамку считывания (ORF) и предотвращает возникновение апоптоза . Это приводит к нерегулируемому росту опухоли . Хотя существуют факторы окружающей среды, которые способствуют прогрессированию рака простаты , есть также и генетический компонент. Во время тестирования кодирующих областей для выявления мутаций было обнаружено 116 генетических вариантов, включая 61 мутацию со сдвигом рамки считывания. [18] Существует более 500 мутаций на хромосоме 17, которые, по-видимому, играют роль в развитии рака груди и яичников в гене BRCA1, многие из которых являются мутациями со сдвигом рамки считывания. [19]
Болезнь Крона связана с геном NOD2. Мутация представляет собой вставку цитозина в положение 3020. Это приводит к преждевременному стоп-кодону, укорачивая белок, который должен транскрибироваться. Когда белок способен нормально формироваться, он реагирует на бактериальные липосахариды, где мутация 3020insC не позволяет белку реагировать. [20]
Муковисцидоз (МВ) — это заболевание, в основе которого лежат мутации в гене регулятора трансмембранной проводимости МВ (CFTR). Выявлено более 1500 мутаций, но не все они вызывают заболевание. [21] Большинство случаев муковисцидоза являются результатом мутации ∆F508, которая удаляет всю аминокислоту. Две мутации со сдвигом рамки считывания представляют интерес для диагностики МВ: CF1213delT и CF1154-insTC. Обе эти мутации обычно встречаются в тандеме по крайней мере с одной другой мутацией. Они обе приводят к небольшому снижению функции легких и встречаются примерно у 1% обследованных пациентов. Эти мутации были идентифицированы с помощью секвенирования по Сэнгеру. [22]
CCR5 является одним из сопутствующих факторов проникновения в клетку, связанных с ВИЧ, чаще всего вовлеченным в несинцитий-индуцирующие штаммы, наиболее очевиден у пациентов с ВИЧ, в отличие от пациентов со СПИДом. Делеция 32 пар оснований в CCR5 была идентифицирована как мутация, которая сводит на нет вероятность заражения ВИЧ. Этот регион на открытой рамке считывания ORF содержит мутацию сдвига рамки, приводящую к преждевременному стоп-кодону. Это приводит к потере функции корецептора ВИЧ in vitro. CCR5-1 считается диким типом, а CCR5-2 считается мутантным аллелем. Те, у кого была гетерозиготная мутация для CCR5, были менее восприимчивы к развитию ВИЧ. В исследовании, несмотря на высокую подверженность вирусу ВИЧ, не было ни одного гомозиготного по мутации CCR5, который дал бы положительный результат на ВИЧ. [3]
Болезнь Тея-Сакса — это смертельное заболевание, поражающее центральную нервную систему. Чаще всего встречается у младенцев и маленьких детей. Прогрессирование заболевания начинается в утробе матери, но симптомы не проявляются до возраста примерно 6 месяцев. Лечения этой болезни не существует. [23] Известно, что мутации в гене β-гексозаминидазы A (Hex A) влияют на начало болезни Тея-Сакса, описано 78 мутаций различных типов, 67 из которых, как известно, вызывают заболевание. Большинство наблюдаемых мутаций (65/78) представляют собой замены одного основания или SNP, 11 делеций, 1 большую и 10 малых, и 2 вставки. 8 из наблюдаемых мутаций представляют собой сдвиг рамки считывания, 6 делеций и 2 вставки. Вставка 4 пар оснований в экзоне 11 наблюдается в 80% случаев болезни Тея-Сакса среди еврейской популяции ашкенази . Мутации сдвига рамки считывания приводят к раннему стоп-кодону, который, как известно, играет роль в заболевании у младенцев. Задержка начала заболевания, по-видимому, вызвана 4 различными мутациями, одна из которых представляет собой делецию 3 пар оснований. [24]
Синдром Смита-Магениса (СМС) — сложный синдром , включающий в себя интеллектуальные нарушения, нарушение сна, поведенческие проблемы и различные черепно-лицевые, скелетные и висцеральные аномалии. Большинство случаев СМС имеют общую делецию размером ~3,5 Мб, которая охватывает ген, индуцированный ретиноевой кислотой-1 ( RAI1 ). Другие случаи иллюстрируют изменчивость фенотипа СМС , ранее не показанную для мутации RAI1, включая потерю слуха, отсутствие самооскорбительного поведения и легкие глобальные задержки. Секвенирование RAI1 выявило мутацию гептамерного C-тракта (CCSC) в экзоне 3, что приводит к мутациям со сдвигом рамки считывания. Из семи зарегистрированных мутаций со сдвигом рамки считывания, происходящих в поли C-трактах в RAI1, четыре случая (~57%) происходят в этом гептамерном C-тракте. Результаты показывают, что этот гептамерный С-тракт представляет собой предпочтительный участок рекомбинации с вставками/делециями (SNindels) и, следовательно, является основной целью для анализа у пациентов с подозрением на мутации в RAI1. [25]
Гипертрофическая кардиомиопатия является наиболее распространенной причиной внезапной смерти у молодых людей, включая тренированных спортсменов, и вызывается мутациями в генах, кодирующих белки сердечного саркомера. Мутации в гене тропонина C ( TNNC1 ) являются редкой генетической причиной гипертрофической кардиомиопатии. Недавнее исследование показало, что мутация со сдвигом рамки считывания (c.363dupG или p.Gln122AlafsX30) в тропонине C стала причиной гипертрофической кардиомиопатии (и внезапной сердечной смерти) у 19-летнего мужчины. [26]
Найти лекарство от болезней, вызванных мутациями со сдвигом рамки, удается редко. Исследования в этой области продолжаются. Одним из примеров является первичный иммунодефицит (ПИД), наследственное состояние, которое может привести к увеличению числа инфекций. Существует 120 генов и 150 мутаций, которые играют роль в первичных иммунодефицитах. Стандартным лечением в настоящее время является генная терапия , но это очень рискованное лечение и часто может приводить к другим заболеваниям, таким как лейкемия. Процедуры генной терапии включают модификацию белка слияния нуклеазы цинковой каймы, расщепление обоих концов мутации, что, в свою очередь, удаляет ее из последовательности. Пропуск экзона , опосредованный антисмысловыми олигонуклеотидами, является еще одной возможностью для мышечной дистрофии Дюшенна . Этот процесс позволяет обойти мутацию, так что остальная часть последовательности остается в рамке, а функция белка остается нетронутой. Однако это не излечивает болезнь, а только лечит симптомы и имеет смысл только в структурных белках или других повторяющихся генах. Третья форма репарации — ревертантный мозаицизм , который естественным образом происходит путем создания обратной мутации или мутации на втором сайте, которая корректирует рамку считывания. Эта реверсия может произойти посредством внутригенной рекомбинации , митотической генной конверсии, проскальзывания ДНК на втором сайте или сайт-специфической реверсии. Это возможно при нескольких заболеваниях, таких как тяжелый комбинированный иммунодефицит, сцепленный с Х-хромосомой (SCID), синдром Вискотта-Олдрича и синдром Блума . Не существует лекарств или других фармакогеномных методов, которые помогают при ПИД. [27]
Европейский патент (EP1369126A1) 2003 года, выданный Bork, описывает метод, используемый для профилактики рака и для радикального лечения рака и предраковых заболеваний, таких как спорадические опухоли с дефицитом репарации несоответствий ДНК (MMR) и опухоли, ассоциированные с HNPCC. Идея заключается в использовании иммунотерапии с комбинаторными смесями пептидов, полученных из мутаций сдвига рамки считывания, специфичных для опухоли, для вызова цитотоксического ответа Т-клеток, направленного конкретно против опухолевых клеток. [28]