В органической химии реакция Михаэля или присоединение Михаэля 1,4 представляет собой реакцию между донором Михаэля ( енолятом или другим нуклеофилом ) и акцептором Михаэля (обычно α,β-ненасыщенный карбонил ) с образованием аддукта Михаэля путем создания углеродного атома. -углеродная связь у β-углерода акцептора . [1] [2] Он принадлежит к более широкому классу сопряженных присоединений и широко используется для мягкого образования углерод-углеродных связей. [3]

Присоединение Михаэля является важным атомосберегающим методом диастереоселективного и энантиоселективного образования связей C–C, и существует множество асимметричных вариантов [4] [5] [6]
В этой общей схеме присоединения Михаэля один или оба из R и R' на нуклеофиле (доноре Михаэля) представляют собой электроноакцепторные заместители, такие как ацильные , циано , нитро или сульфоновые группы, которые делают соседний метиленовый водород достаточно кислым для образования карбанион при реакции с основанием , B: . Для алкена (акцептора Михаэля) заместителем R" обычно является карбонил , что делает соединение α,β-ненасыщенным карбонильным соединением (еноном или еналем ) , или R" может быть любой электроноакцепторной группой.
Как первоначально определил Артур Майкл [7] [8] , реакция представляет собой присоединение енолята кетона или альдегида к α,β-ненасыщенному карбонильному соединению по β-углероду. Текущее определение реакции Михаэля расширилось и теперь включает нуклеофилы, отличные от енолятов . [9] Некоторые примеры нуклеофилов включают углеродные нуклеофилы с двойной стабилизацией, такие как бета-кетоэфиры, малонаты и бета-цианоэфиры. Полученный продукт содержит очень полезный 1,5-диоксигенированный образец. Неуглеродные нуклеофилы, такие как вода, спирты , амины и енамины, также могут реагировать с α,β-ненасыщенным карбонилом по 1,4-присоединению. [10]
Некоторые авторы расширили определение присоединения Михаэля, чтобы по существу относиться к любой реакции 1,4-присоединения α,β-ненасыщенных карбонильных соединений. Другие, однако, настаивают на том, что такое использование является злоупотреблением терминологией, и ограничивают присоединение Михаэля образованием углерод-углеродных связей за счет добавления углеродных нуклеофилов. Термины окса-реакция Михаэля и аза-реакция Михаэля [2] использовались для обозначения 1,4-присоединения кислородных и азотных нуклеофилов соответственно. Реакция Михаэля также связана с реакциями 1,6-присоединения. [11]
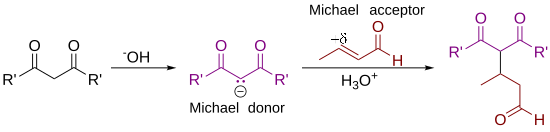
В механизме реакции нуклеофилом является 1 : [3]
Депротонирование 1 основанием приводит к карбаниону 2, стабилизированному электроноакцепторными группами . Структуры 2a–2c представляют собой три резонансные структуры , которые можно нарисовать для этого вида, две из которых содержат енолят- ионы. Этот нуклеофил реагирует с электрофильным алкеном 3 с образованием 4 в реакции сопряженного присоединения . Наконец, енолят 4 отрывает протон от протонированного основания (или растворителя) с образованием 5 .
В реакции преобладают орбитальные, а не электростатические соображения. ВЗМО стабилизированных енолятов имеет большой коэффициент при центральном атоме углерода, в то время как НСМО многих альфа-, бета-ненасыщенных карбонильных соединений имеет большой коэффициент при бета-углероде. Таким образом, оба реагента можно считать мягкими . Эти поляризованные граничные орбитали имеют одинаковую энергию и эффективно реагируют с образованием новой связи углерод-углерод. [12]
Как и альдольное присоединение , реакция Михаэля может протекать через енол , силиленоловый эфир при присоединении Мукаямы-Майкла или, что чаще, через енолятный нуклеофил. В последнем случае стабилизированное карбонильное соединение депротонируется сильным основанием (жесткая енолизация) или кислотой Льюиса и слабым основанием (мягкая енолизация). Образующийся енолят атакует активированный олефин с 1,4- региоселективностью , образуя углерод-углеродную связь. При этом енолят также передается электрофилу . Поскольку электрофил гораздо менее кислый, чем нуклеофил, быстрый перенос протона обычно передает енолят обратно нуклеофилу, если продукт поддается енолизу; однако можно воспользоваться преимуществами нового локуса нуклеофильности, если имеется подходящий электрофил. В зависимости от относительной кислотности нуклеофила и продукта реакция может быть каталитической по основанию. В большинстве случаев реакция необратима при низкой температуре.
Исследование, проведенное Артуром Майклом в 1887 году в Университете Тафтса, было вызвано публикацией Конрада и Кутцейта в 1884 году о реакции этил-2,3-дибромпропионата с диэтил-натрийомалонатом с образованием производного циклопропана [13] (теперь признано, что это включает две последовательные реакции замещения). ).
Майкл смог получить тот же продукт, заменив пропионат этиловым эфиром 2-бромакриловой кислоты , и понял, что эта реакция может работать, только если предположить реакцию присоединения к двойной связи акриловой кислоты . Затем он подтвердил это предположение, проведя реакцию диэтилмалоната и этилового эфира коричной кислоты , образовав первый аддукт Михаэля: [14]
В том же году Райнер Людвиг Клайзен заявил о приоритете изобретения. [15] Он и Т. Комненос наблюдали продукты присоединения к двойным связям в качестве побочных продуктов ранее в 1883 году при исследовании реакций конденсации малоновой кислоты с альдегидами . [16] Однако, по мнению биографа Такаси Токороямы, это утверждение необоснованно. [14]
Исследователи расширили сферу применения добавок Майкла, включив в него элементы хиральности посредством асимметричных версий реакции. Наиболее распространенные методы включают хиральный катализ фазового переноса , такой как четвертичные аммониевые соли , полученные из алкалоидов хинного дерева ; или органокатализ , который активируется енамином или иминием с помощью хиральных вторичных аминов, обычно полученных из пролина . [17]
В реакции между циклогексаноном и β-нитростиролом, изображенной ниже, основной пролин превращается в производное и работает в сочетании с протонной кислотой, такой как п -толуолсульфоновая кислота : [18]
Син-присоединение предпочтительно при 99% ее . В переходном состоянии, которое, как полагают, отвечает за эту селективность, енамин (образующийся между азотом пролина и циклокетоном) и β-нитростирол находятся на одной стороне с нитрогруппой , связанной водородом с протонированным амином в боковой группе пролина.
Хорошо известной реакцией Михаэля является синтез варфарина из 4-гидроксикумарина и бензилиденацетона , о котором впервые сообщил Линк в 1944 году: [19]
Существует несколько асимметричных версий этой реакции с использованием хиральных катализаторов. [20] [21] [22] [23] [24] [25]
Классическими примерами реакции Михаэля являются реакции между диэтилмалонатом (донор Михаэля) и диэтилфумаратом (акцептор Михаэля), [26] реакция диэтилмалоната и мезитилоксида (с образованием димедона ), [27] реакция диэтилмалоната и метилкротоната, [28] 2-нитропропана и метилакрилата , [ 29] этилфенилцианоацетата и акрилонитрила [30] и нитропропана и метилвинилкетона . [31]
Классической тандемной последовательностью присоединения Михаэля и альдолов является кольцеобразование Робинсона .
В реакции присоединения Мукаямы-Майкла нуклеофилом является простой эфир силилинола , а катализатором обычно является тетрахлорид титана : [32] [33]

Реакция 1,6-Майкла протекает через нуклеофильную атаку 𝛿 углерода α,β- , 𝛿 -диненасыщенного акцептора Михаэля. [34] [35] Механизм присоединения 1,6 аналогичен механизму присоединения 1,4, за одним исключением является нуклеофильная атака, происходящая по углероду 𝛿 акцептора Михаэля. [35] Однако исследования показывают, что органокатализ часто благоприятствует 1,4-присоединению. [34] Во многих синтезах, где предпочтение отдавалось 1,6-присоединению, субстрат содержал определенные структурные особенности. [35] Исследования показали, что катализаторы также могут влиять на региоселективность и энантиоселективность реакции 1,6-присоединения. [35]
Например, на изображении ниже показано присоединение этилмагнийбромида к этилсорбату 1 с использованием медного катализатора с обратным йозифосным ( R,S )-(–)-3-лигандом. [35] Эта реакция привела к образованию продукта 1,6-присоединения 2 с выходом 0%, продукта 1,6-присоединения 3 с выходом примерно 99% и продукта 1,4-присоединения 4 с выходом менее 2%. Этот конкретный катализатор и набор условий реакции привели к преимущественно региоселективному и энантиоселективному присоединению 1,6-Майкла этилсорбата 1 к продукту 3 .

Реакция Михаэля используется в качестве механистического этапа во многих препаратах- ингибиторах ковалентной связи . Противораковые препараты , такие как ибрутиниб, осимертиниб и рокилетиниб, имеют функциональную группу акриламида в качестве акцептора Михаэля. Акцептор Михаэля в препарате реагирует с акцептором Михаэля в активном центре фермента . Это жизнеспособное лечение рака, поскольку целевой фермент ингибируется в результате реакции Михаэля. [36]
Все реакции полимеризации имеют три основные стадии: инициирование, распространение и прекращение. Стадией инициирования является присоединение нуклеофила к мономеру по Михаэлю . Полученная разновидность подвергается присоединению по Михаэлю с другим мономером, причем последний действует как акцептор. Это удлиняет цепь за счет образования еще одной нуклеофильной разновидности, которая будет выступать в качестве донора для следующего добавления. Этот процесс повторяется до тех пор, пока реакция не завершится обрывом цепи. [37] Первоначальный донор Михаэля может быть нейтральным донором, таким как амины , тиолы и алкоксиды или алкиллиганды, связанные с металлом. [38]

Полимеризация с линейным ступенчатым ростом - одно из первых применений реакции Михаэля в полимеризации. Для синтеза широкого спектра полимеров использовалось множество доноров и акцепторов Михаэля. Примеры таких полимеров включают поли(амидоамин), поли(аминоэфир), поли(имидосульфид ) , поли( эфирсульфид ), поли(аспартамид), поли(имидоэфир ) , поли(аминохинон ) , поли(енонсульфид). ) и поли(енаминкетон ) .
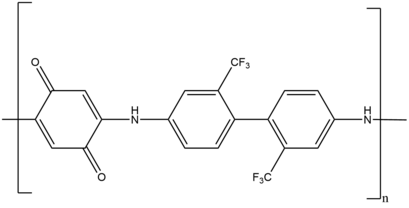
Например, в результате линейно-ступенчатой ростовой полимеризации образуется окислительно-восстановительный поли(аминохинон), который служит антикоррозионным покрытием на различных металлических поверхностях. [39] Другой пример включает сетчатые полимеры , которые используются для доставки лекарств, высокоэффективные композиты и покрытия. Эти сетчатые полимеры синтезируются с использованием системы присоединения Михаэля с двойным ростом цепи, фотоиндуцированного радикала и ступенчатого роста.

{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )