В химии и термодинамике стандартная энтальпия образования или стандартная теплота образования соединения — изменение энтальпии при образовании 1 моля вещества из составляющих его элементов в исходном состоянии при всех веществах в стандартном состоянии . Стандартное значение давления p ⦵ = 10 5 Па (= 100 кПа = 1 бар ) рекомендовано ИЮПАК , хотя до 1982 года использовалось значение 1,00 атм (101,325 кПа). [1] Стандартной температуры не существует. Его символ — Δ f H ⦵ . Надстрочный индекс Plimsoll на этом символе указывает на то, что процесс протекал в стандартных условиях при указанной температуре (обычно 25 °C или 298,15 К).
Стандартные состояния определены для различных типов веществ. Для газа это гипотетическое состояние, которое он принял бы, если бы подчинялся уравнению идеального газа при давлении 1 бар. Для газообразного или твердого растворенного вещества , присутствующего в разбавленном идеальном растворе , стандартным состоянием является гипотетическое состояние концентрации растворенного вещества ровно один моль на литр (1 М ) при давлении 1 бар, экстраполированное из бесконечного разбавления. Для чистого вещества или растворителя в конденсированном состоянии (жидком или твердом) стандартным состоянием является чистая жидкость или твердое вещество под давлением 1 бар.
Для элементов, имеющих несколько аллотропов, эталонным состоянием обычно выбирается форма, в которой элемент наиболее стабилен при давлении 1 бар. Единственным исключением является фосфор , для которого наиболее стабильной формой при давлении 1 бар является черный фосфор , но белый фосфор выбран в качестве стандартного эталонного состояния при нулевой энтальпии образования. [2]
Например, стандартная энтальпия образования углекислого газа — это энтальпия следующей реакции в указанных выше условиях:
Все элементы записываются в свои стандартные состояния, и образуется один моль продукта. Это справедливо для всех энтальпий образования.
Стандартная энтальпия образования измеряется в единицах энергии на количество вещества, обычно выражаемой в килоджоулях на моль (кДж моль -1 ), но также в килокалориях на моль , джоулях на моль или килокалориях на грамм (любая комбинация этих единиц, соответствующая с указанием энергии на массу или количество).
Все элементы в исходных состояниях ( газообразный кислород , твердый углерод в форме графита и т. д.) имеют стандартную энтальпию образования, равную нулю, поскольку при их образовании не происходит никаких изменений.
Реакция образования представляет собой процесс при постоянном давлении и постоянной температуре. Поскольку давление стандартной реакции образования фиксировано на уровне 1 бар, стандартная энтальпия образования или теплота реакции является функцией температуры. Для целей таблицы все стандартные энтальпии образования указаны при одной температуре: 298 К, обозначенной символом Δ f H.⦵
298 К.
Для многих веществ реакцию образования можно рассматривать как сумму ряда более простых реакций, реальных или вымышленных. Затем энтальпию реакции можно проанализировать, применив закон Гесса , который гласит, что сумма изменений энтальпии для ряда отдельных стадий реакции равна изменению энтальпии всей реакции. Это верно, поскольку энтальпия — это функция состояния , значение которой для всего процесса зависит только от начального и конечного состояний, а не от каких-либо промежуточных состояний. Примеры приведены в следующих разделах.
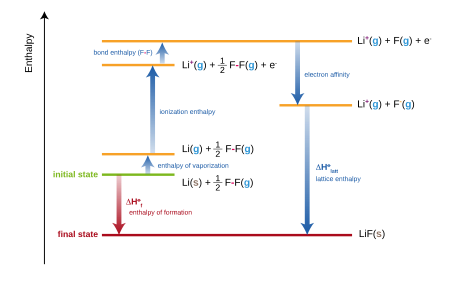
Для ионных соединений стандартная энтальпия образования эквивалентна сумме нескольких членов, входящих в цикл Борна–Габера . Например, образование фторида лития ,
можно рассматривать как сумму нескольких ступеней, каждая из которых имеет свою энтальпию (или энергию, примерно):
Сумма этих энтальпий дает стандартную энтальпию образования ( Δ f H ) фторида лития:
На практике энтальпию образования фторида лития можно определить экспериментально, но энергию решетки невозможно измерить напрямую. Поэтому уравнение переформулировано для оценки энергии решетки: [3]
Реакции образования большинства органических соединений являются гипотетическими. Например, углерод и водород не вступают в прямую реакцию с образованием метана ( CH 4 ), поэтому стандартную энтальпию образования невозможно измерить напрямую. Однако стандартную энтальпию сгорания легко измерить с помощью бомбовой калориметрии . Затем стандартную энтальпию образования определяют с помощью закона Гесса . Горение метана:
эквивалентна сумме гипотетического разложения на элементы с последующим сжиганием элементов с образованием углекислого газа ( CO 2 ) и воды ( H 2 O ):
Применяя закон Гесса,
Решая стандарт энтальпии образования,
Значение определено как -74,8 кДж/моль. Знак минус показывает, что реакция, если бы она протекала, была бы экзотермической ; то есть метан энтальпически более стабилен, чем газообразный водород и углерод.
Прогнозировать теплоты образования простых ненапряженных органических соединений можно с помощью метода групповой аддитивности теплоты образования .
Стандартное изменение энтальпии любой реакции можно рассчитать на основе стандартных энтальпий образования реагентов и продуктов с использованием закона Гесса. Данную реакцию рассматривают как разложение всех реагирующих веществ на элементы в их стандартных состояниях с последующим образованием всех продуктов. Теплота реакции тогда минус сумма стандартных энтальпий образования реагентов (каждый из которых умножается на соответствующий стехиометрический коэффициент ν ) плюс сумма стандартных энтальпий образования продуктов (каждый из которых также умножается на соответствующий стехиометрический коэффициент). коэффициент), как показано в уравнении ниже: [4]
Если стандартная энтальпия продуктов меньше стандартной энтальпии реагентов, стандартная энтальпия реакции отрицательна. Это означает, что реакция является экзотермической. Обратное также верно; стандартная энтальпия реакции положительна для эндотермической реакции. В этом расчете неявно предполагается идеальное решение между реагентами и продуктами, при котором энтальпия смешения равна нулю.
Например, при сжигании метана :
Однако элемент находится в стандартном состоянии, так что , и теплота реакции упрощается до
это уравнение из предыдущего раздела для энтальпии сгорания .
Термохимические свойства отдельных веществ при 298,15 К и 1 атм.