Йод-131 ( 131 I , I-131 ) — важный радиоизотоп йода , открытый Гленном Сиборгом и Джоном Ливингудом в 1938 году в Калифорнийском университете в Беркли. [3] Он имеет период полураспада радиоактивного распада около восьми дней. Он связан с ядерной энергетикой, медицинскими диагностическими и лечебными процедурами и добычей природного газа. Он также играет важную роль как радиоактивный изотоп, присутствующий в продуктах ядерного деления , и внес значительный вклад в опасность для здоровья от испытаний атомной бомбы на открытом воздухе в 1950-х годах и от катастрофы на Чернобыльской АЭС , а также был большой долей опасности загрязнения в первые недели ядерного кризиса в Фукусиме . Это связано с тем, что 131 I является основным продуктом деления урана и плутония , составляя почти 3% от общего количества продуктов деления (по весу). См. Выход продуктов деления для сравнения с другими радиоактивными продуктами деления . 131I также является основным продуктом деления урана-233 , получаемого из тория .
Из-за своего режима бета-распада йод-131 вызывает мутацию и смерть в клетках, в которые он проникает, и других клетках на расстоянии до нескольких миллиметров. По этой причине высокие дозы изотопа иногда менее опасны, чем низкие дозы, поскольку они имеют тенденцию убивать ткани щитовидной железы , которые в противном случае стали бы раковыми в результате облучения. Например, у детей, получавших умеренную дозу 131I для лечения аденомы щитовидной железы, наблюдалось заметное увеличение рака щитовидной железы, но у детей, получавших гораздо более высокую дозу, этого не наблюдалось. [4] Аналогично, большинство исследований очень высокой дозы 131I для лечения болезни Грейвса не обнаружили никакого увеличения рака щитовидной железы, хотя существует линейное увеличение риска рака щитовидной железы при поглощении 131I в умеренных дозах. [5] Таким образом, йод-131 все реже используется в малых дозах в медицинских целях (особенно у детей), но все чаще используется только в больших и максимальных дозах лечения как способ уничтожения целевых тканей. Это известно как «терапевтическое использование».
Йод-131 можно «увидеть» методами визуализации ядерной медицины (например, гамма-камерами ) всякий раз, когда он дается для терапевтического использования, так как около 10% его энергии и дозы облучения приходится на гамма-излучение. Однако, поскольку остальные 90% излучения (бета-излучение) вызывают повреждение тканей, не способствуя какой-либо способности видеть или «изображение» изотопа, другие менее разрушительные радиоизотопы йода, такие как йод-123 (см. изотопы йода ), предпочтительны в ситуациях, когда требуется только ядерная визуализация. Изотоп 131 I по-прежнему иногда используется для чисто диагностической (т. е. визуализации) работы из-за его низкой стоимости по сравнению с другими радиоизотопами йода. Очень малые дозы медицинской визуализации 131 I не показали никакого увеличения рака щитовидной железы. Низкая стоимость 131 I, в свою очередь, обусловлена относительной простотой создания 131 I путем нейтронной бомбардировки природного теллура в ядерном реакторе, а затем выделения 131 I различными простыми методами (например, нагреванием для удаления летучего йода). Напротив, другие радиоизотопы йода обычно создаются гораздо более дорогими методами, начиная с циклотронного облучения капсул с газом ксенона под давлением . [6]
Йод-131 также является одним из наиболее часто используемых гамма-излучающих радиоактивных промышленных трассеров . Радиоактивные изотопы трассера вводятся в жидкость для гидроразрыва пласта для определения профиля инъекции и местоположения трещин, созданных при гидроразрыве пласта. [7]
Гораздо меньшие случайные дозы йода-131, чем те, которые используются в медицинских терапевтических процедурах, как предполагается некоторыми исследованиями, являются основной причиной увеличения рака щитовидной железы после случайного ядерного заражения. Эти исследования предполагают, что рак возникает из-за остаточного радиационного повреждения тканей, вызванного 131 I, и должен появляться в основном через годы после воздействия, намного позже того, как 131 I распадется. [8] [9] Другие исследования не обнаружили корреляции. [10] [11]
Большая часть 131 I производится при нейтронном облучении мишени из природного теллура в ядерном реакторе. Облучение природного теллура производит почти полностью 131 I как единственный радионуклид с периодом полураспада более часов, поскольку большинство более легких изотопов теллура становятся более тяжелыми стабильными изотопами или же стабильным йодом или ксеноном. Однако самый тяжелый встречающийся в природе нуклид теллура, 130 Te (34% природного теллура), поглощает нейтрон, превращаясь в теллур-131, который бета-распадается с периодом полураспада 25 минут до 131 I.
Соединение теллура может быть облучено, будучи связанным в виде оксида с ионообменной колонкой, с выделением 131 I, затем элюированным в щелочной раствор. [12] Чаще всего облучают порошкообразный элементарный теллур, а затем отделяют 131 I от него сухой перегонкой йода, который имеет гораздо более высокое давление паров . Затем элемент растворяют в слабощелочном растворе стандартным способом, чтобы получить 131 I в виде йодида и гипойодата (который вскоре восстанавливается до йодида). [13]
131I является продуктом деления с выходом 2,878% от урана-235 , [14] и может быть выпущен при испытаниях ядерного оружия и ядерных авариях . Однако короткий период полураспада означает, что он не присутствует в значительных количествах в охлажденном отработанном ядерном топливе , в отличие от йода-129, период полураспада которого почти в миллиард раз больше, чем у 131I .
В небольших количествах он выбрасывается в атмосферу некоторыми атомными электростанциями. [15]
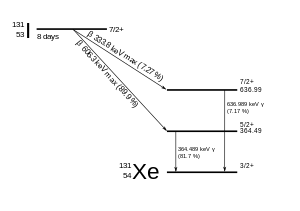
131 I распадается с периодом полураспада 8,0249(6) дней [1] с бета-минус и гамма- излучением. Этот изотоп йода имеет 78 нейтронов в своем ядре, в то время как единственный стабильный нуклид, 127 I, имеет 74. Распадаясь, 131 I чаще всего (89% времени) расходует свои 971 кэВ энергии распада, превращаясь в стабильный ксенон-131 в два этапа, с гамма-распадом, быстро следующим за бета-распадом:
Первичные выбросы распада 131 I, таким образом, представляют собой электроны с максимальной энергией 606 кэВ (89% распространенности, другие 248–807 кэВ) и гамма-лучи 364 кэВ (81% распространенности, другие 723 кэВ). [16] Бета-распад также производит антинейтрино , которое уносит переменное количество энергии бета-распада. Электроны, из-за их высокой средней энергии (190 кэВ, с типичными присутствующими спектрами бета-распада), имеют проникновение в ткани от 0,6 до 2 мм . [17]
Йод из пищи усваивается организмом и преимущественно концентрируется в щитовидной железе , где он необходим для функционирования этой железы. Когда 131 I присутствует в высоких уровнях в окружающей среде из-за радиоактивных осадков , он может усваиваться через загрязненную пищу, а также накапливаться в щитовидной железе. По мере распада он может вызывать повреждение щитовидной железы. Основной риск от воздействия 131 I — это повышенный риск рака, вызванного радиацией , в пожилом возрасте. Другие риски включают возможность нераковых новообразований и тиреоидита . [5]
Риск рака щитовидной железы в более позднем возрасте, по-видимому, уменьшается с увеличением возраста на момент облучения. Большинство оценок риска основаны на исследованиях, в которых облучение радиацией происходило у детей или подростков. Когда взрослые подвергаются облучению, эпидемиологам сложно обнаружить статистически значимую разницу в показателях заболеваний щитовидной железы по сравнению с аналогичной, но в остальном не подвергавшейся облучению группой. [5] [19]
Риск можно снизить, принимая добавки йода, увеличивая общее количество йода в организме и, следовательно, уменьшая поглощение и задержку в лице и груди и снижая относительную долю радиоактивного йода. Однако такие добавки не были последовательно распространены среди населения, проживающего ближе всего к Чернобыльской АЭС после катастрофы [20] , хотя они были широко распространены среди детей в Польше.
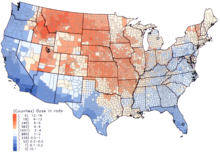
В США самые высокие дозы 131 I от выпадений наблюдались в 1950-х и начале 1960-х годов у детей, потреблявших свежее молоко из источников, загрязненных в результате наземных испытаний ядерного оружия. [8] Национальный институт рака предоставляет дополнительную информацию о последствиях для здоровья от воздействия 131 I от выпадений, [21] а также индивидуальные оценки для тех, кто родился до 1971 года, для каждого из 3070 округов США. Расчеты основаны на данных, собранных относительно выпадений от испытаний ядерного оружия, проведенных на испытательном полигоне в Неваде . [22]
27 марта 2011 года Департамент общественного здравоохранения Массачусетса сообщил, что 131 I был обнаружен в очень низких концентрациях в дождевой воде из образцов, собранных в Массачусетсе, США, и что это, вероятно, произошло от АЭС Фукусима. [23] Фермеры около завода сбрасывали сырое молоко, в то время как тестирование в Соединенных Штатах обнаружило 0,8 пикокюри на литр йода-131 в образце молока, но уровни радиации были в 5000 раз ниже, чем «уровень вмешательства», установленный FDA. Ожидалось, что уровни снизятся относительно быстро [24]
Распространенным методом лечения для предотвращения воздействия йода-131 является насыщение щитовидной железы обычным стабильным йодом-127 в виде йодидной или йодатной соли.

Йод-131 используется для радиотерапии с открытым источником в ядерной медицине для лечения нескольких состояний. Он также может быть обнаружен гамма-камерами для диагностической визуализации , однако он редко применяется только в диагностических целях, визуализация обычно проводится после терапевтической дозы. [26] Использование 131I в виде соли йода использует механизм поглощения йода нормальными клетками щитовидной железы.
Основные применения 131 I включают лечение тиреотоксикоза (гипертиреоза) из-за болезни Грейвса , а иногда и гиперактивных узлов щитовидной железы (аномально активная ткань щитовидной железы, которая не является злокачественной). Терапевтическое использование радиоактивного йода для лечения гипертиреоза из-за болезни Грейвса было впервые описано Саулом Герцем в 1941 году. Доза обычно вводится перорально (в виде жидкости или капсул) в амбулаторных условиях и обычно составляет 400–600 мегабеккерелей (МБк). [27] Радиоактивный йод (йод-131) сам по себе может потенциально ухудшить тиреотоксикоз в первые несколько дней после лечения. Одним из побочных эффектов лечения является начальный период в несколько дней усиления симптомов гипертиреоза. Это происходит потому, что когда радиоактивный йод разрушает клетки щитовидной железы, они могут выделять гормон щитовидной железы в кровоток. По этой причине иногда пациентам предварительно назначают тиреостатические препараты, такие как метимазол, и/или назначают симптоматическое лечение, такое как пропранолол. Лечение радиоактивным йодом противопоказано при кормлении грудью и беременности [28]
Йод-131 в более высоких дозах, чем при тиреотоксикозе, используется для удаления остатков ткани щитовидной железы после полной тиреоидэктомии для лечения рака щитовидной железы . [29] [27]
Типичные терапевтические дозы I-131 составляют от 2220 до 7400 мегабеккерелей (МБк). [30] Из-за этой высокой радиоактивности и из-за того, что воздействие бета-излучения на ткани желудка будет высоким вблизи нерастворенной капсулы, I-131 иногда вводят пациентам-людям в небольшом количестве жидкости. Введение этой жидкой формы обычно осуществляется через соломинку, которая используется для медленного и осторожного всасывания жидкости из экранированного контейнера. [31] Для введения животным (например, кошкам с гипертиреозом) по практическим причинам изотоп должен вводиться путем инъекции. Европейские руководящие принципы рекомендуют введение капсулы из-за «большего удобства для пациента и превосходной защиты от радиации для лиц, осуществляющих уход». [32]
Дозы абляции обычно вводятся в стационарных условиях, и Международные основные стандарты безопасности МАГАТЭ рекомендуют не выписывать пациентов, пока активность не упадет ниже 1100 МБк. [33] Рекомендации МКРЗ гласят, что «лица, оказывающие поддержку и уход» за пациентами, проходящими радионуклидную терапию, должны рассматриваться как члены общественности в целях ограничения дозы, и любые ограничения для пациента должны разрабатываться на основе этого принципа. [34]
Пациентам, получающим лечение радиоактивным йодом I-131, могут рекомендовать не заниматься сексом в течение одного месяца (или меньше, в зависимости от введенной дозы), а женщинам рекомендуется не беременеть в течение шести месяцев после этого. «Это связано с тем, что теоретический риск для развивающегося плода существует, хотя количество оставшейся радиоактивности может быть небольшим, и нет никаких медицинских доказательств фактического риска от лечения радиоактивным йодом. Такая мера предосторожности по сути исключит прямое воздействие радиоактивности на плод и значительно снизит возможность зачатия спермой, которая теоретически могла быть повреждена воздействием радиоактивного йода». [35] Эти рекомендации различаются в разных больницах и будут зависеть от национального законодательства и руководств, а также от введенной дозы радиации. Некоторые также советуют не обнимать и не держать детей, когда уровень радиации все еще высок, и может быть рекомендовано расстояние в один или два метра от других. [36]
I-131 будет выведен из организма в течение следующих нескольких недель после его введения. Большая часть I-131 будет выведена из организма человека в течение 3–5 дней путем естественного распада и через выделение с потом и мочой. Меньшие количества будут продолжать выделяться в течение следующих нескольких недель, поскольку организм перерабатывает гормоны щитовидной железы, созданные с помощью I-131. По этой причине рекомендуется регулярно чистить туалеты, раковины, простыни и одежду, которую использовал человек, прошедший лечение. Пациентам также может быть рекомендовано постоянно носить тапочки или носки и избегать длительного тесного контакта с другими людьми. Это сводит к минимуму случайное воздействие на членов семьи, особенно детей. [37] Может быть рекомендовано использование дезактивирующего средства, специально предназначенного для удаления радиоактивного йода. Использование растворов хлорного отбеливателя или чистящих средств, содержащих хлорный отбеливатель, для очистки не рекомендуется, поскольку может выделяться радиоактивный газообразный элементарный йод. [38] Воздушный I-131 может вызвать больший риск вторичного воздействия, распространяя загрязнение на большую площадь. Пациенту рекомендуется, если это возможно, оставаться в комнате с ванной комнатой, соединенной с ней, чтобы ограничить непреднамеренное воздействие на членов семьи.
Во многих аэропортах есть детекторы радиации для обнаружения контрабанды радиоактивных материалов. Пациентов следует предупредить, что если они путешествуют по воздуху, они могут активировать детекторы радиации в аэропортах в течение 95 дней после их лечения 131 I. [39]
Изотоп 131 I также используется в качестве радиоактивной метки для некоторых радиофармацевтических препаратов , которые могут использоваться в терапии, например, 131 I- метайодобензилгуанидин ( 131 I-MIBG) для визуализации и лечения феохромоцитомы и нейробластомы . Во всех этих терапевтических применениях 131 I разрушает ткани бета-излучением с коротким радиусом действия . Около 90% его радиационного повреждения тканей происходит через бета-излучение, а остальное происходит через его гамма-излучение (на большем расстоянии от радиоизотопа). Его можно увидеть при диагностическом сканировании после его использования в терапии, поскольку 131 I также является гамма-излучателем.
Из-за канцерогенности его бета-излучения в щитовидной железе в малых дозах, I-131 редко используется в первую очередь или исключительно для диагностики (хотя в прошлом это было более распространено из-за относительной простоты производства этого изотопа и низкой стоимости). Вместо этого более чисто гамма-излучающий радиоактивный йод йод-123 используется в диагностических тестах ( ядерное медицинское сканирование щитовидной железы). Более долгоживущий йод-125 также иногда используется, когда для диагностики необходим более длительный период полураспада радиоактивного йода, и в лечении брахитерапией (изотоп, заключенный в небольшие металлические капсулы, похожие на семена), где низкоэнергетическое гамма-излучение без бета-компонента делает йод-125 полезным. Другие радиоизотопы йода никогда не используются в брахитерапии.
Использование 131 I в качестве медицинского изотопа было признано причиной того, что обычная партия биоматериалов была отклонена при пересечении границы Канады и США. [40] Такой материал может попасть в канализацию непосредственно из медицинских учреждений или выделяться пациентами после лечения.
Впервые использованный в 1951 году для локализации утечек в системе питьевого водоснабжения Мюнхена , Германия, йод-131 стал одним из наиболее часто используемых промышленных радиоактивных гамма-излучающих индикаторов , с применением в изотопной гидрологии и обнаружении утечек. [41] [42] [43] [44]
С конца 1940-х годов радиоактивные трассеры использовались в нефтяной промышленности. Помеченная на поверхности вода затем отслеживается в скважине с помощью соответствующего гамма-детектора для определения потоков и обнаружения подземных утечек. I-131 был наиболее широко используемым маркирующим изотопом в водном растворе йодида натрия . [45] [46] [47] Он используется для характеристики жидкости для гидроразрыва пласта , чтобы помочь определить профиль инъекции и местоположение трещин, созданных при гидроразрыве пласта . [48] [49] [50]
В 1997 г. NCI провел детальную оценку дозы облучения щитовидной железы жителей США от I-131 в осадках от испытаний в Неваде. (...) мы оценили риски рака щитовидной железы от этого воздействия и подсчитали, что в Соединенных Штатах может произойти около 49 000 случаев, связанных с осадками, почти все из них среди лиц, которым в какой-то момент в период 1951–57 гг. было меньше 20 лет, с 95-процентными пределами неопределенности 11 300 и 212 000.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка )связей между выбросами йода-131 в Ханфорде и заболеваниями щитовидной железы не наблюдалось. [Результаты] показывают, что если и существует повышенный риск заболеваний щитовидной железы из-за воздействия йода-131 в Ханфорде, то он, вероятно, слишком мал, чтобы его можно было наблюдать с использованием лучших эпидемиологических методов.Управляющее резюме
{{cite book}}: |website=проигнорировано ( помощь ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )