Некротический фасциит ( НФ ), также известный как плотоядное заболевание , представляет собой бактериальную инфекцию , которая приводит к отмиранию частей мягких тканей тела . [3] Это тяжелое заболевание, возникающее внезапно и быстро распространяющееся. [3] Симптомы обычно включают покраснение или пурпурную кожу в пораженной области, сильную боль, лихорадку и рвоту. [3] Чаще всего поражаются конечности и промежность . [2]
Обычно инфекция попадает в организм через повреждения кожи, такие как порез или ожог . [3] Факторы риска включают плохую иммунную функцию , например, из-за диабета или рака , ожирения , алкоголизма , внутривенного употребления наркотиков и заболеваний периферических артерий . [2] [3] Обычно он не распространяется между людьми. [3] Заболевание подразделяется на четыре типа, в зависимости от возбудителя. [4] От 55 до 80% случаев связаны с более чем одним типом бактерий . [4] Метициллин-резистентный золотистый стафилококк (MRSA) встречается примерно в трети случаев. [4] Медицинская визуализация часто помогает подтвердить диагноз. [4]
Некротический фасциит можно предотвратить путем надлежащего ухода за раной и мытья рук . [3] Обычно его лечат хирургическим путем по удалению инфицированной ткани и внутривенным введением антибиотиков . [2] [3] Часто используется комбинация антибиотиков, таких как пенициллин G , клиндамицин , ванкомицин внутривенно и гентамицин . [2] Задержки в операции связаны с гораздо более высоким риском смерти. [4] Несмотря на качественное лечение, риск смерти составляет от 25 до 35%. [2]
Некротический фасциит встречается примерно у 0,4 человек на 100 000 в год в США и примерно у 1 на 100 000 в Западной Европе. [4] Оба пола страдают в равной степени. [2] Оно становится более распространенным среди пожилых людей и редко встречается у детей. [4] Это было описано, по крайней мере, со времен Гиппократа . [2] Термин «некротический фасциит» впервые вошел в употребление в 1952 году. [4] [7]
Симптомы могут включать лихорадку, отек и жалобы на чрезмерную боль. Начальные изменения кожи подобны целлюлиту или абсцессу , что затрудняет диагностику на ранних стадиях. Уплотнение кожи и мягких тканей, а также отек за пределами области кожных изменений обычно наблюдаются у пациентов с ранними некротическими изменениями. [2] Покраснение и отек обычно сливаются с окружающими нормальными тканями. Поверхностная кожа может выглядеть блестящей и напряженной. [8] Другими признаками, более характерными для некротических изменений (но присутствующих на более поздних стадиях в 7–44% случаев), являются: образование булл , кровотечение в кожу , которое присутствует до некроза кожи [2] (поворот кожи из красный, фиолетовый и черный из-за тромбоза кровеносных сосудов), [8] наличие газа в тканях и снижение или отсутствие чувствительности на коже [2] (из-за некроза подлежащих нервов). [8] Быстрое развитие шока, несмотря на терапию антибиотиками, является еще одним признаком некротического фасциита. Некротические изменения, поражающие пах, известны как гангрена Фурнье . [2]
Однако у людей с ослабленным иммунитетом (болеют раком, принимают кортикостероиды , проходят лучевую терапию , химиотерапию , ВИЧ/СПИД или перенесли трансплантацию органов или костного мозга ) типичные симптомы могут не проявляться. У людей с ослабленным иммунитетом также в два раза выше риск смерти от некротизирующих инфекций, поэтому в этой группе следует сохранять более высокую подозрительность. [2]
Более 70% случаев регистрируются у людей, имеющих хотя бы одну из следующих клинических ситуаций: иммуносупрессию, диабет, алкоголизм/наркоманию/курение, злокачественные новообразования и хронические системные заболевания. По неясным причинам оно иногда возникает у людей с внешне нормальным общим состоянием. [9]
Некротический фасциит может возникнуть в любой части тела, но чаще всего он наблюдается на конечностях, промежности и половых органах . Лишь немногие из таких случаев возникают в области груди и живота. Травма является обычной причиной инфекции, например, в результате внутривенной инъекции лекарства, инъекции инсулина, укусов животных и насекомых, введения катетера на кожу или свища, соединяющего кожу с внутренними органами тела. Кожные инфекции, такие как абсцесс и язвы, также могут осложнять некротический фасциит. У больных стрептококковым фарингитом предполагается распространение инфекции через кровь. Обычными причинами инфекции промежности и половых органов ( гангрена Фурнье ) являются травмы, хирургические вмешательства, инфекции мочевыводящих путей , камни и абсцесс бартолиновой железы . [2]
Риск развития некротического фасциита из раны можно снизить, если тщательно ухаживать за раной и мыть руки. [3]
Типы некротизирующей инфекции мягких тканей можно разделить на четыре класса в зависимости от типа бактерий, поражающих мягкие ткани. Эта система классификации была впервые описана Джулиано и его коллегами в 1977 году. [4] [2]
Инфекция I типа : это наиболее распространенный тип инфекции, на него приходится от 70 до 80% случаев. Это заболевание вызывается смесью типов бактерий, обычно в области живота или паха. [4] Этот тип инфекции обычно вызывают различные виды грамположительных кокков ( Staphylococcus aureus , Streptococcus pyogenes и энтерококки ), грамотрицательные палочки ( Escherichia coli , Pseudomonas aeruginosa ) и анаэробы ( Bacteroides и Clostridium ). разновидность). [4] Пострадавшие обычно старшего возраста и имеют сопутствующие заболевания, такие как сахарный диабет, ожирение и иммунодефицит. [4] Обычно травма не является причиной таких инфекций. Можно выявить предшествующую абсцессную инфекцию или перфорацию кишечника с бактериальной транслокацией . Клостридиальная инфекция составляет 10% инфекций I типа. Задействованными видами Clostridium являются Clostridium perfringens , Clostridium septicum и Clostridium sordellii , которые обычно вызывают газовую гангрену (также известную как мионекроз). Clostridium perfringens вырабатывает два смертельных токсина: альфа-токсин и тета-токсин. Альфа-токсин вызывает чрезмерную агрегацию тромбоцитов, которая блокирует кровеносные сосуды и лишает жизненно важные органы снабжения кислородом. Это создает кислую среду с дефицитом кислорода для размножения бактерий. Когда альфа-токсин поглощается мягкими тканями, он может ингибировать миграцию лейкоцитов из кровеносных сосудов в мягкие ткани , тем самым нарушая функцию фагоцитов . Два токсина вместе могут вызвать разрушение эритроцитов в кровеносных сосудах , повреждение целостности кровеносных сосудов и подавление функции сердца. [ нужна цитата ]
Clostridium sordellii также может продуцировать два основных токсина: все известные вирулентные штаммы продуцируют летальный токсин существенного фактора вирулентности (TcsL), а некоторые также продуцируют геморрагический токсин (TcsH). TcsL и TcsH являются членами семейства больших клостридиальных цитотоксинов (LCC). [10] Ключевым фактором вирулентности Clostridium septicum является порообразующий токсин, называемый альфа-токсином, хотя он не связан с альфа-токсином Clostridium perfringens . Мионекротические инфекции, вызываемые этими видами клостридий, обычно возникают у потребителей героина путем инъекций . Пациенты с клостридиальной инфекцией обычно испытывают сильную боль в месте раны, из которой обычно выделяется зловонная кровь, смешанная с сывороткой (серозно-кровянистые выделения). Шок может быстро прогрессировать после первоначальной травмы или инфекции, и как только состояние шока наступит, вероятность смерти превышает 50%. Другой бактерией, связанной с таким же быстрым прогрессированием заболевания, является стрептококковая инфекция группы А (в основном Streptococcus pyogenes ). Между тем, для появления симптомов других бактериальных инфекций требуется два или более дней. [2]
Инфекция типа II : на эту инфекцию приходится от 20 до 30% случаев, преимущественно поражаются конечности. [4] [11] В основном это касается бактерий Streptococcus pyogenes , отдельно или в сочетании со стафилококковыми инфекциями. Оба типа бактерий могут быстро прогрессировать и проявляться синдромом токсического шока . Виды Streptococcus производят белок М , который действует как суперантиген , стимулируя массивный системный иммунный ответ, который неэффективен против бактериального антигена, провоцируя шок. Инфекция типа II чаще поражает молодых, здоровых взрослых с травмами в анамнезе. [2]
Инфекция III типа : Vibrio vulnificus , бактерия, обнаруженная в соленой воде , является редкой причиной этой инфекции, которая возникает через повреждение кожи. Прогрессирование заболевания аналогично типу II, но иногда с незначительными видимыми изменениями кожи. [2]
Инфекция IV типа . Инфекция IV типа, составляющая менее 1% случаев, вызвана грибком Candida albicans . Факторы риска включают возраст и иммунодефицит. [4] [12]

Ранняя диагностика затруднена, поскольку на ранних стадиях заболевание часто выглядит как простая поверхностная инфекция кожи . [4] Хотя ряд лабораторных методов и методов визуализации могут вызвать подозрение на некротический фасциит, ни один из них не может его исключить. [14] Золотым стандартом диагностики является хирургическое вмешательство в условиях высокого подозрения. В случае сомнений можно сделать небольшой разрез пораженной ткани, и если палец легко отделяет ткань вдоль фасциальной плоскости, диагноз подтверждается и следует провести обширную санацию . [2]
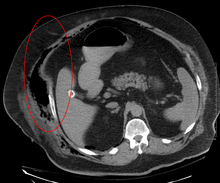
Роль визуализации в диагностике некротического фасциита ограничена. Задержка во времени при выполнении визуализации является серьезной проблемой. Обычная рентгенография может выявить подкожную эмфизему (газ в подкожной клетчатке ), что убедительно указывает на некротические изменения, но она недостаточно чувствительна, чтобы обнаружить все случаи, поскольку некротические инфекции кожи, вызванные бактериями, отличными от клостридиальных инфекций, обычно не выявляют подкожных поражений. эмфизема. Если диагноз все еще вызывает сомнения, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) являются более чувствительными методами, чем обычная рентгенография. Однако и КТ, и МРТ недостаточно чувствительны, чтобы полностью исключить некротические изменения. [2] КТ может выявить утолщение фасции, отек, подкожный газ и образование абсцесса. [2] При МРТ, когда происходит скопление жидкости с глубоким поражением фасции, ее утолщение или усиление при инъекции контраста , следует заподозрить некротический фасциит. Между тем, УЗИ может выявить образование поверхностного абсцесса, но оно недостаточно чувствительно для диагностики некротического фасциита. [2] КТ способна обнаружить около 80% случаев, тогда как МРТ может выявить немного больше. [15]
Число лейкоцитов более 15 000 клеток/мм 3 и уровень натрия в сыворотке менее 135 ммоль/л имеют чувствительность 90% при выявлении некротизирующей инфекции мягких тканей. [ нужна цитация ] Он также имеет 99% шанс исключить некротические изменения, если значения показали иное . Для определения вероятности развития некротического фасциита разрабатываются различные системы оценки, но наиболее часто используется система оценки, разработанная Вонгом и его коллегами в 2004 году. Это лабораторный показатель риска некротического фасциита (LRINEC), который можно использовать для стратификации по риску тех людей, у которых есть признаки тяжелого целлюлита или абсцесса, чтобы определить вероятность наличия некротического фасциита. Он использует шесть лабораторных показателей: С-реактивный белок , общее количество лейкоцитов , гемоглобин , натрий , креатинин и глюкозу в крови . [2] Оценка 6 и более указывает на то, что следует серьезно подозревать некротический фасциит. [16] Критериями оценки являются:
Однако система подсчета баллов не была утверждена. Значения будут ложноположительными, если присутствуют какие-либо другие воспалительные состояния. Поэтому значения, полученные с помощью этой системы оценок, следует интерпретировать с осторожностью. [2] Около 10% пациентов с некротизирующим фасциитом в оригинальном исследовании все еще имели показатель LRIEC <6. [16] Валидационное исследование показало, что пациенты с оценкой LRIEC ≥6 имеют более высокий уровень смертности и ампутаций. [18]
Некротический фасциит можно частично предотвратить путем тщательного ухода за раной и мытья рук. [3]
Хирургическая обработка (удаление пораженных тканей) является основой лечения некротического фасциита. Раннее медицинское лечение часто носит предполагаемый характер; таким образом, прием антибиотиков следует начинать сразу при подозрении на это состояние. Для определения надлежащего покрытия антибиотиками берутся тканевые культуры (а не мазки из ран), и антибиотики могут быть изменены в зависимости от результатов. Помимо контроля артериального давления и гидратации, следует оказать поддержку тем, у кого нестабильные показатели жизнедеятельности и низкий диурез. [2]
Агрессивную обработку раны следует проводить как можно раньше, обычно сразу после установления диагноза некротизирующей инфекции мягких тканей (НМТИ). Хирургические разрезы часто выходят за пределы участков уплотнения (затвердевшей ткани), чтобы удалить поврежденные кровеносные сосуды, ответственные за уплотнение. Однако целлюлитные мягкие ткани иногда не подвергают хирургической обработке для последующего покрытия раны кожей. Для удаления дополнительной некротической ткани может быть использовано более одной операции. В некоторых случаях, когда конечность поражена НМТИ, хирургическим лечением выбора может быть ампутация. После обработки раны следует наложить соответствующие повязки, чтобы предотвратить обнажение костей, сухожилий и хрящей , чтобы такие структуры не высыхали, и чтобы способствовать заживлению ран. [2]
При некротической инфекции области промежности (гангрене Фурнье) обработка раны и уход за ней могут быть затруднены из-за продуктов выделения, которые часто загрязняют эту область и влияют на процесс заживления ран. Таким образом, регулярная смена повязок с использованием системы контроля фекалий может помочь сохранить рану в области промежности чистой. Иногда может потребоваться колостома для отвода продуктов выделения и поддержания чистоты раны в области промежности. [2]
Эмпирическое назначение антибиотиков обычно начинают сразу же после постановки диагноза НИМП, а затем заменяют антибиотикотерапией под контролем культуры. В случае НИППП эмпирические антибиотики имеют широкий спектр действия и охватывают грамположительные (включая MRSA), грамотрицательные и анаэробные бактерии. [19]
Хотя в исследованиях сравнивались моксифлоксацин (фторхинолон) и амоксициллин-клавуланат (пенициллин) и оценивалась соответствующая продолжительность лечения (от 7 до 21 дня), окончательных выводов об эффективности лечения, идеальной продолжительности лечения или побочных эффектах не было. могло быть сделано из-за доказательств низкого качества. [19]
Некротический фасциит поражает примерно 0,4 человека на каждые 100 000 человек в год в США. [4] В Соединенных Штатах ежегодно регистрируется около 1000 случаев некротического фасциита, но их частота растет. Это может быть связано с повышением осведомленности об этом состоянии, что приводит к увеличению количества сообщений, или с вирулентностью бактерий, или с увеличением устойчивости бактерий к антибиотикам. [2] В некоторых регионах мира это встречается примерно один раз на 100 000 человек. [4]
Более высокие показатели некротического фасциита наблюдаются у людей с ожирением или диабетом, а также у людей с ослабленным иммунитетом, алкоголиков или людей с заболеваниями периферических артерий . Однако заболевание может возникнуть и у молодых, здоровых взрослых без каких-либо основных заболеваний. НПВП могут увеличивать частоту некротических инфекций из-за модификации иммунного ответа в организме, поскольку НПВП ингибируют ферменты циклоксигеназу -1 и циклоксигеназу-2, которые играют важную роль в выработке тромбоксана и простагландина Е2 . Простагландин отвечает за лихорадку, воспаление и боль. Ингибирование выработки простагландина Е2 снижает воспалительную реакцию и адгезию лейкоцитов и, таким образом, снижает иммунный ответ на бактериальную инвазию, вызывающую инфекцию мягких тканей. [2]
В пятом веке до нашей эры Гиппократ описывал некротизирующую инфекцию мягких тканей как заболевание, при котором у пострадавших возникает « рожа по всему телу, а причиной является всего лишь банальный несчастный случай. Кости, плоть и сухожилия (пуповина, сухожилие или нерв) поражаются». отвалились от тела, и было много смертей». Первое английское описание некротизирующей инфекции мягких тканей было сделано британским хирургом Леонардом Гиллеспи и британскими врачами Гилбертом Блейном и Томасом Троттером в 18 веке. В то время некротизирующие инфекции мягких тканей были известны под разными названиями: «фагеденическая язва» (изъязвление, которое распространяется и разрушает окружающие ткани), «гангренозная фагедена», «гангренозная язва», «злокачественная язва», «гнилостная язва», «молниеносная гангрена». «, «некротизирующая рожа», «гангренозная рожа», «крепитирующий целлюлит», «гангренозный целлюлит», «целлюлит Мелени», «некротизирующий синергический целлюлит», «гемолитическая стрептококковая гангрена», «прогрессирующая бактериальная синергическая гангрена» или «некротизирующий абсцесс». ". [20] Позже термин «госпитальная гангрена» стал более широко использоваться. В 1871 году хирург армии Конфедеративных Штатов Джозеф Джонс сообщил о 2642 случаях госпитальной гангрены с уровнем смертности 46%. В 1883 году доктор Жан-Альфред Фурнье описал некротизирующую инфекцию промежности и мошонки , ныне называемую гангреной Фурнье . Термин «некротический фасциит» был впервые введен Уилсоном в 1952 году. Его определение стало более широким и теперь включает не только инфекцию фасции , но и другие инфекции мягких тканей. [2] Несмотря на неприязнь медицинского сообщества, термин «галопирующая гангрена» часто используется в сенсационных средствах массовой информации для обозначения вспышек некротизирующего фасциита. [21]