В органической химии пираноза — собирательный термин для сахаридов , химическая структура которых включает шестичленное кольцо , состоящее из пяти атомов углерода и одного атома кислорода ( гетероцикл ). Могут быть и другие атомы углерода, внешние по отношению к кольцу. Название происходит от его сходства с кислородным гетероциклом пираном , но кольцо пиранозы не имеет двойных связей . Пираноза, в которой аномерная -OH ( гидроксильная группа ) при C(l) преобразована в OR-группу, называется пиранозидом .
Пиранозное кольцо образуется в результате реакции гидроксильной группы углерода 5 (C-5) сахара с альдегидом при углероде 1. При этом образуется внутримолекулярный полуацеталь . Если реакция происходит между гидроксилом C-4 и альдегидом, вместо этого образуется фураноза . [1] Форма пиранозы термодинамически более стабильна, чем форма фуранозы, что можно увидеть по распределению этих двух циклических форм в растворе. [2]

Герман Эмиль Фишер получил Нобелевскую премию по химии (1902) за работу по определению структуры D - альдогексоз . [1] Однако линейные структуры свободных альдегидов, предложенные Фишером, представляют собой очень незначительный процент форм, которые гексозные сахара принимают в растворе. Эдмунд Херст и Клиффорд Первс из исследовательской группы Уолтера Хаворта окончательно определили, что гексозные сахара преимущественно образуют пиранозное, или шестичленное, кольцо. Хаворт нарисовал кольцо в виде плоского шестиугольника с группами выше и ниже плоскости кольца — проекция Хаворта . [3]
Дальнейшее уточнение конформации пиранозных колец произошло, когда Спонслер и Доре (1926) поняли , что математическая обработка шестичленных колец Саксом может быть применена к их рентгеновской структуре целлюлозы . [3] Было установлено, что кольцо пиранозы сморщено, чтобы все атомы углерода кольца имели геометрию, близкую к идеальной тетраэдрической.
Это сморщивание приводит к образованию в общей сложности 38 различных основных пиранозных конформаций : 2 стульев, 6 лодочек, 6 косых лодочек, 12 полустульев и 12 конвертов. [4]

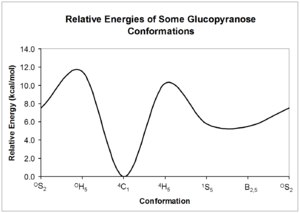
Эти конформеры могут конвертироваться друг с другом; однако каждая форма может иметь очень разную относительную энергию, поэтому может присутствовать значительный барьер для взаимного превращения. Энергию этих конформаций можно рассчитать с помощью квантовой механики ; приведен пример возможных взаимопревращений глюкопиранозы . [5]
Конформации пиранозного кольца внешне аналогичны конформациям циклогексанового кольца . Однако специфическая номенклатура пираноз включает ссылку на кислород кольца, а присутствие гидроксилов в кольце оказывает отчетливое влияние на его конформационные предпочтения. Существуют также конформационные и стереохимические эффекты, специфичные для пиранозного кольца.

Чтобы назвать конформации пиранозы, сначала определяют конформер. Общие конформеры аналогичны тем, которые встречаются в циклогексане , и они составляют основу названия. Распространенными формами являются стул (С), лодочка (Б), косой (S), полустул (Н) или конверт (Е). Затем атомы кольца нумеруются; аномерный , или полуацеталь, углерод всегда равен 1. Атомы кислорода в структуре обычно обозначаются атомом углерода, к которому они присоединены в ациклической форме, и обозначаются O. Тогда :
Как показывают относительные энергии структур на диаграмме выше, структуры стула представляют собой наиболее стабильную форму углеводов. Эта относительно определенная и стабильная конформация означает, что атомы водорода пиранозного кольца расположены под относительно постоянными углами друг к другу. ЯМР углеводов использует эти двугранные углы для определения конфигурации каждой из гидроксильных групп вокруг кольца.