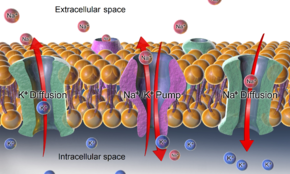
Относительно статический мембранный потенциал покоящихся клеток называется мембранным потенциалом покоя (или напряжением покоя), в отличие от специфических динамических электрохимических явлений, называемых потенциалом действия и градуированным мембранным потенциалом . Мембранный потенциал покоя имеет значение приблизительно -70 мВ или -0,07 В. [ 1]
Помимо последних двух, которые происходят в возбудимых клетках ( нейронах , мышцах и некоторых секреторных клетках желез ), мембранный потенциал в большинстве невозбудимых клеток также может претерпевать изменения в ответ на внешние или внутриклеточные стимулы. Потенциал покоя существует из-за различий в проницаемости мембран для ионов калия , натрия , кальция и хлорида , которые, в свою очередь, являются результатом функциональной активности различных ионных каналов , ионных транспортеров и обменников. Условно мембранный потенциал покоя можно определить как относительно стабильное, основное значение трансмембранного напряжения в клетках животных и растений.
Поскольку проницаемость мембраны для калия намного выше, чем для других ионов, и из-за сильного химического градиента для калия, ионы калия вытекают из цитозоля во внеклеточное пространство, неся положительный заряд, пока их движение не будет уравновешено накоплением отрицательного заряда на внутренней поверхности мембраны. Опять же, из-за высокой относительной проницаемости для калия результирующий мембранный потенциал почти всегда близок к потенциалу реверсии калия . Но для того, чтобы этот процесс произошел, сначала должен быть установлен градиент концентрации ионов калия. Эта работа выполняется ионными насосами/транспортерами и/или обменниками и, как правило, обеспечивается АТФ .
В случае покоящегося мембранного потенциала через плазматическую мембрану животной клетки градиенты калия (и натрия) устанавливаются Na + /K + -АТФазой (натрий-калиевый насос), которая переносит 2 иона калия внутрь и 3 иона натрия наружу за счет 1 молекулы АТФ. В других случаях, например, мембранный потенциал может быть установлен за счет подкисления внутренней части мембранного отсека (например, протонный насос, который генерирует мембранный потенциал через мембраны синаптических везикул ). [ необходима цитата ]
В большинстве количественных трактовок мембранного потенциала, таких как вывод уравнения Голдмана , предполагается электронейтральность ; то есть, что нет измеримого избытка заряда по обе стороны мембраны. Таким образом, хотя электрический потенциал на мембране существует из-за разделения зарядов, нет фактической измеримой разницы в глобальной концентрации положительных и отрицательных ионов по обе стороны мембраны (как это оценивается ниже), то есть нет фактического измеримого избытка заряда по обе стороны. Это происходит, потому что влияние заряда на электрохимический потенциал намного больше, чем влияние концентрации, поэтому необнаруживаемое изменение концентрации создает большое изменение электрического потенциала. [ необходима цитата ]
Клеточные мембраны обычно проницаемы только для подмножества ионов. К ним обычно относятся ионы калия, ионы хлора, ионы бикарбоната и другие. Чтобы упростить описание ионной основы покоящегося мембранного потенциала, наиболее полезно сначала рассмотреть только один вид ионов, а остальные рассмотреть позже. Поскольку трансплазматические мембранные потенциалы почти всегда определяются в первую очередь проницаемостью калия, то именно с этого и следует начать.

Напряжение покоя является результатом работы нескольких ферментов, перемещающих ионы ( унипортеров , котранспортеров и насосов ) в плазматической мембране, которые постоянно работают параллельно, причем каждый ион-переносчик имеет свою характерную электродвижущую силу (= потенциал реверсии = «равновесное напряжение»), зависящую от концентраций конкретного субстрата внутри и снаружи (внутренний АТФ включен в случае некоторых насосов). АТФаза, экспортирующая H +, делает мембранное напряжение в растениях и грибах гораздо более отрицательным, чем в более подробно исследованных животных клетках, где напряжение покоя в основном определяется селективными ионными каналами.
В большинстве нейронов потенциал покоя имеет значение около −70 мВ. Потенциал покоя в основном определяется концентрацией ионов в жидкостях по обе стороны клеточной мембраны и белками транспорта ионов , которые находятся в клеточной мембране. То, как концентрации ионов и мембранных транспортных белков влияют на значение потенциала покоя, описано ниже.
Потенциал покоя клетки можно наиболее полно понять, думая о нем в терминах равновесных потенциалов. В приведенной здесь диаграмме модельной клетке был дан только один проникающий ион (калий). В этом случае потенциал покоя этой клетки будет таким же, как равновесный потенциал для калия.
Однако реальная клетка более сложна, поскольку имеет проницаемости для многих ионов, каждый из которых вносит вклад в потенциал покоя. Чтобы лучше понять, рассмотрим клетку только с двумя проникающими ионами, калием и натрием. Рассмотрим случай, когда эти два иона имеют равные градиенты концентрации, направленные в противоположных направлениях, и что проницаемости мембраны для обоих ионов равны. K +, покидающий клетку, будет стремиться перетянуть мембранный потенциал к E K . Na +, поступающий в клетку, будет стремиться перетянуть мембранный потенциал к обратному потенциалу для натрия E Na . Поскольку проницаемости для обоих ионов были установлены равными, мембранный потенциал в конце перетягивания каната Na + /K + окажется на полпути между E Na и E K . Поскольку E Na и E K были равны, но имели противоположные знаки, середина между ними равна нулю, что означает, что мембрана будет находиться в состоянии покоя при 0 мВ.
Обратите внимание, что даже если мембранный потенциал при 0 мВ стабилен, это не равновесное состояние, поскольку ни один из участвующих ионов не находится в равновесии. Ионы диффундируют вниз по своим электрохимическим градиентам через ионные каналы, но мембранный потенциал поддерживается постоянным притоком K + и оттоком Na + через ионные транспортеры . Такая ситуация с аналогичными проницаемостями для противодействующих ионов, таких как калий и натрий в животных клетках, может быть чрезвычайно затратной для клетки, если эти проницаемости относительно велики, поскольку для перекачивания ионов обратно требуется много энергии АТФ . Поскольку ни одна реальная клетка не может позволить себе такие равные и большие ионные проницаемости в состоянии покоя, потенциал покоя животных клеток определяется преобладающей высокой проницаемостью для калия и регулируется до требуемого значения путем модуляции проницаемостей и градиентов натрия и хлорида.
В здоровой животной клетке проницаемость Na + составляет около 5% от проницаемости K + или даже меньше, тогда как соответствующие потенциалы реверсии составляют +60 мВ для натрия ( E Na ) и −80 мВ для калия ( E K ). Таким образом, мембранный потенциал не будет точно равен E K , а скорее будет деполяризован от E K на величину приблизительно 5% от 140 мВ разницы между E K и E Na . Таким образом, потенциал покоя клетки будет около −73 мВ.
В более формальной записи мембранный потенциал — это средневзвешенное значение равновесного потенциала каждого иона, вносящего вклад. Величина каждого веса — это относительная проводимость каждого иона. В обычном случае, когда три иона вносят вклад в мембранный потенциал:
где
Для определения мембранных потенциалов два наиболее важных типа мембранных ионных транспортных белков — это ионные каналы и ионные транспортеры . Белки ионных каналов создают пути через клеточные мембраны, по которым ионы могут пассивно диффундировать без прямого расхода метаболической энергии. Они обладают селективностью к определенным ионам, таким образом, существуют калий- , хлорид- и натрий-селективные ионные каналы . Различные клетки и даже различные части одной клетки ( дендриты , клеточные тела , перехваты Ранвье ) будут иметь разное количество различных ионных транспортных белков. Как правило, количество определенных калиевых каналов наиболее важно для контроля потенциала покоя (см. ниже). Некоторые ионные насосы, такие как Na+/K+-АТФаза, являются электрогенными, то есть они создают дисбаланс заряда на клеточной мембране, а также могут напрямую вносить вклад в мембранный потенциал. Большинство насосов используют метаболическую энергию (АТФ) для функционирования.
Для большинства клеток животных ионы калия (K + ) являются наиболее важными для потенциала покоя. [2] Из-за активного транспорта ионов калия концентрация калия внутри клеток выше, чем снаружи. Большинство клеток имеют белки калий-селективных ионных каналов, которые остаются открытыми все время. Будет происходить чистое движение положительно заряженных ионов калия через эти калиевые каналы с последующим накоплением избыточного отрицательного заряда внутри клетки. Внешнее движение положительно заряженных ионов калия происходит из-за случайного молекулярного движения ( диффузии ) и продолжается до тех пор, пока внутри клетки не накопится достаточно избыточного отрицательного заряда, чтобы сформировать мембранный потенциал, который может уравновесить разницу в концентрации калия между внутренней и внешней частью клетки. «Баланс» означает, что электрическая сила ( потенциал ), которая возникает в результате накопления ионного заряда и которая препятствует внешней диффузии, увеличивается до тех пор, пока она не станет равной по величине, но противоположной по направлению тенденции к внешнему диффузионному движению калия. Эта точка равновесия является равновесным потенциалом , поскольку чистый трансмембранный поток (или ток ) K + равен нулю. Хорошее приближение для равновесного потенциала данного иона требует только концентрации по обе стороны мембраны и температуры. Его можно рассчитать с помощью уравнения Нернста :
где
Равновесные потенциалы калия около −80 милливольт (внутри отрицательные) являются обычными. Различия наблюдаются у разных видов, разных тканей одного и того же животного и одних и тех же тканей в разных условиях окружающей среды. Применяя уравнение Нернста выше, можно объяснить эти различия изменениями относительной концентрации K + или различиями в температуре.
Для общего использования уравнение Нернста часто приводится в упрощенной форме, предполагая типичную температуру человеческого тела (37 °C), уменьшая константы и переходя к основанию логарифма 10. (Единицы, используемые для концентрации, не важны, поскольку они будут сокращаться в соотношении). Для калия при нормальной температуре тела можно рассчитать равновесный потенциал в милливольтах следующим образом:
Аналогично равновесный потенциал для натрия (Na + ) при нормальной температуре человеческого тела рассчитывается с использованием той же упрощенной константы. Вы можете рассчитать E, предположив внешнюю концентрацию, [K + ] o , равную 10 мМ и внутреннюю концентрацию, [K + ] i , равную 100 мМ. Для ионов хлора (Cl − ) знак константы должен быть обратным (−61,54 мВ). При расчете равновесного потенциала для кальция (Ca 2+ ) заряд 2+ вдвое уменьшает упрощенную константу до 30,77 мВ. Если работать при комнатной температуре, около 21 °C, рассчитанные константы составляют приблизительно 58 мВ для K + и Na + , −58 мВ для Cl − и 29 мВ для Ca 2+ . При физиологической температуре около 29,5 °C и физиологических концентрациях (которые различаются для каждого иона) расчетные потенциалы составляют приблизительно 67 мВ для Na + , −90 мВ для K + , −86 мВ для Cl− и 123 мВ для Ca2 + .
Мембранный потенциал покоя не является равновесным потенциалом, поскольку он зависит от постоянного расхода энергии (для ионных насосов , как упоминалось выше) для своего поддержания. Это динамический диффузионный потенциал, который учитывает этот механизм — в отличие от равновесного потенциала подушек, который является верным независимо от природы рассматриваемой системы. Мембранный потенциал покоя доминирует в системе за счет ионных видов, которые имеют наибольшую проводимость через мембрану. Для большинства клеток это калий. Поскольку калий также является ионом с самым отрицательным равновесным потенциалом, обычно потенциал покоя не может быть более отрицательным, чем равновесный потенциал калия. Потенциал покоя можно рассчитать с помощью уравнения напряжения Голдмана-Ходжкина-Каца, используя концентрации ионов в качестве равновесного потенциала, а также включая относительные проницаемости каждого ионного вида. В нормальных условиях можно с уверенностью предположить, что только ионы калия, натрия (Na + ) и хлорида (Cl − ) играют большую роль в потенциале покоя:
Это уравнение напоминает уравнение Нернста, но имеет член для каждого проникающего иона. Кроме того, в уравнение было вставлено z , в результате чего внутриклеточные и внеклеточные концентрации Cl − меняются местами относительно K + и Na + , поскольку отрицательный заряд хлорида обрабатывается путем инвертирования дроби внутри логарифмического члена. * E m — мембранный потенциал, измеряемый в вольтах * R , T , и F такие же, как указано выше * P s — относительная проницаемость иона s *[s] Y — концентрация иона s в отсеке Y, как указано выше. Другой способ рассмотрения мембранного потенциала, рассматривающий вместо этого проводимость ионных каналов, а не проницаемость мембраны, — это использование уравнения Миллмана (также называемого уравнением хордовой проводимости):
или переформулировать
где g tot — это объединенная проводимость всех видов ионов, снова в условных единицах. Последнее уравнение описывает потенциал покоящейся мембраны как средневзвешенное значение потенциалов реверсии системы, где веса — это относительные проводимости каждого вида ионов ( g X / g tot ). Во время потенциала действия эти веса изменяются. Если проводимости Na + и Cl − равны нулю, мембранный потенциал уменьшается до потенциала Нернста для K + (как g K + = g tot ). Обычно в условиях покоя g Na+ и g Cl− не равны нулю, но они намного меньше, чем g K+ , что делает E m близким к E eq,K+ . Медицинские состояния, такие как гиперкалиемия , при которой изменяется калий сыворотки крови (который управляет [K + ] o ), очень опасны, поскольку они компенсируют E eq,K+ , тем самым влияя на E m . Это может вызвать аритмии и остановку сердца . Использование болюсной инъекции хлорида калия при казнях с помощью смертельной инъекции останавливает сердце, сдвигая потенциал покоя в сторону более положительного значения, что деполяризует и постоянно сокращает сердечные клетки, не позволяя сердцу реполяризоваться и , таким образом, войти в диастолу для повторного наполнения кровью.
Хотя уравнение напряжения GHK и уравнение Миллмана связаны, они не эквивалентны. Критическое различие заключается в том, что уравнение Миллмана предполагает, что зависимость тока от напряжения является омической, тогда как уравнение напряжения GHK учитывает небольшие мгновенные выпрямления, предсказанные уравнением потока GHK, вызванные градиентом концентрации ионов. Таким образом, более точную оценку мембранного потенциала можно рассчитать с помощью уравнения GHK, чем с помощью уравнения Миллмана. [3]
В некоторых клетках мембранный потенциал постоянно меняется (например, в клетках кардиостимуляторов ). Для таких клеток никогда не существует «покоя», а «потенциал покоя» является теоретической концепцией. Другие клетки с небольшими функциями мембранного транспорта, которые меняются со временем, имеют мембранный потенциал покоя, который можно измерить, вставив электрод в клетку. [4] Трансмембранные потенциалы также можно измерить оптически с помощью красителей, которые изменяют свои оптические свойства в соответствии с мембранным потенциалом.
Токи покоя в нервах были измерены и описаны Юлиусом Бернштейном в 1902 году, когда он предложил «Мембранную теорию», которая объясняла потенциал покоя нервов и мышц как диффузионный потенциал. [9]