Сигнальный белок агути — это белок , который у человека кодируется геном ASIP . [5] [6] Он отвечает за распределение пигмента меланина у млекопитающих. [7] [8] Агути взаимодействует с рецептором меланокортина 1 , чтобы определить, производит ли меланоцит (пигментная клетка) феомеланин (красно-желтый пигмент) или эумеланин (коричнево-черный пигмент). [9] Это взаимодействие отвечает за появление четких светлых и темных полос в волосах животных, таких как агути , в честь которых назван этот ген. У других видов, таких как лошади , передача сигналов агути отвечает за определение того, какие части тела будут красными или черными. Мыши с агути дикого типа будут серо-коричневыми , причем каждый волосок будет частично желтым, а частично черным. Мутации потери функции у мышей и других видов вызывают черную окраску шерсти, тогда как мутации, вызывающие экспрессию по всему телу у мышей, вызывают желтую шерсть и ожирение. [10]
Сигнальный белок агути (ASIP) является конкурентным антагонистом альфа -меланоцитстимулирующего гормона (α-MSH) при связывании с белками рецептора меланокортина 1 (MC1R) . Активация α-MSH вызывает выработку более темного эумеланина, тогда как активация ASIP вызывает выработку более красного феомеланина. [11] Это означает, что там и во время проявления агути часть растущих волос будет желтой, а не черной.
У мышей ген агути кодирует паракринную сигнальную молекулу, которая заставляет меланоциты волосяных фолликулов синтезировать желтый пигмент феомеланин вместо черного или коричневого пигмента эумеланин . Плейотропные эффекты конститутивной экспрессии мышиного гена включают ожирение во взрослом возрасте , повышенную восприимчивость к опухолям и преждевременное бесплодие. Этот ген очень похож на ген мыши и кодирует секретируемый белок, который может (1) влиять на качество пигментации волос , (2) действовать как обратный агонист альфа-меланоцитстимулирующего гормона , (3) играть роль в нейроэндокринной аспекты действия меланокортина и (4) играют функциональную роль в регуляции липидного обмена в адипоцитах . [12]
У мышей аллель агути дикого типа (А) представляет серый фенотип, однако с помощью генетического анализа было идентифицировано множество вариантов аллеля, что приводит к широкому спектру фенотипов, отличных от типичного серого окраса. [13] Наиболее широко изученными вариантами аллелей являются летальная желтая мутация (A y ) и жизнеспособная желтая мутация (A vy ), которые вызваны эктопической экспрессией агути . [13] Эти мутации также связаны с синдромом желтого ожирения , который характеризуется ранним ожирением , гиперинсулинемией и онкогенезом . [13] [14] Локус гена агути у мышей находится на хромосоме 2 и кодирует белок, состоящий из 131 аминокислоты. Этот белок сигнализирует о распределении пигментов меланина в эпителиальных меланоцитах , расположенных у основания волосяных фолликулов, причем экспрессия более чувствительна на вентральных волосах, чем на дорсальных волосах. [15] [16] Агути не секретируется непосредственно в меланоцитах, поскольку он действует как паракринный фактор на клетки дермальных сосочков, ингибируя высвобождение меланокортина . [17] Меланокортин действует на фолликулярные меланоциты, увеличивая выработку эумеланина , пигмента меланина, отвечающего за коричневые и черные волосы. При выраженной агути преобладает выработка феомеланина , пигмента меланина, который придает волосам желтый или красный цвет. [18]
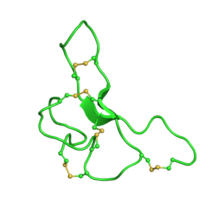
Сигнальный пептид агути принимает мотив ингибиторного цистинового узла . [19] Наряду с гомологичным пептидом, родственным агути , это единственные известные белки млекопитающих, принимающие эту укладку. Пептид состоит из 131 аминокислоты. [20]
Мутация летального желтого цвета (A y ) была первой эмбриональной мутацией, охарактеризованной у мышей, поскольку гомозиготные мыши летального желтого цвета (A y / A y ) умирают на ранних стадиях развития из-за ошибки дифференцировки трофэктодермы . [15] Летальные желтые гомозиготы сегодня редки, тогда как летальные желтые и жизнеспособные желтые гетерозиготы (A y /a и A vy /a) остаются более распространенными. У мышей дикого типа агути экспрессируется только в коже во время роста волос, но эти доминантные мутации желтого цвета вызывают его экспрессию и в других тканях . [10] Эта эктопическая экспрессия гена агути связана с синдромом желтого ожирения , характеризующимся ожирением с ранним началом , гиперинсулинемией и онкогенезом . [15]
Мутация летального желтого (A y ) возникает из-за делеции вышележащего сайта в стартовом сайте транскрипции агути . Эта делеция приводит к потере геномной последовательности агути , за исключением промотора и первого некодирующего экзона Raly , повсеместно экспрессируемого гена у млекопитающих. [16] Кодирующие экзоны агути помещаются под контроль промотора Raly , инициируя повсеместную экспрессию агути , увеличивая выработку феомеланина по сравнению с эумеланином и приводя к развитию желтого фенотипа. [21]

Мутация жизнеспособного желтого цвета (A vy ) обусловлена изменением длины мРНК агути , поскольку экспрессируемый ген становится длиннее нормальной длины гена агути. Это вызвано вставкой единственной внутрицистернальной ретротранспозона A-частицы (IAP) выше места начала транскрипции агути . [22] В проксимальном конце гена неизвестный промотор затем вызывает конституциональную активацию агути , и у людей появляются фенотипы, соответствующие летальной желтой мутации. Хотя механизм активации промотора, контролирующего жизнеспособную желтую мутацию, неизвестен, интенсивность окраса шерсти коррелирует со степенью метилирования гена , которая определяется диетой матери и воздействием окружающей среды. [22] Поскольку агути сам по себе ингибирует рецепторы меланокортина, ответственные за выработку эумеланина, желтый фенотип усугубляется как при летальных желтых , так и при жизнеспособных желтых мутациях, поскольку экспрессия гена агути увеличивается. Агути уникален, потому что, хотя это рецессивный аллель, гетерозиготы будут желтыми, а не доминантными коричневыми или черными. [23]
Жизнеспособные желтые (A vy /a) и летально-желтые (A y /a) гетерозиготы сокращают продолжительность жизни и повышают риск развития раннего ожирения, сахарного диабета II типа и различных опухолей. [17] [24] Повышенный риск развития ожирения обусловлен нарушением регуляции аппетита, поскольку агути агонизирует родственный агути белок (AGRP), ответственный за стимуляцию аппетита через орексигенные нейроны гипоталамуса NPY/AGRP. [22] Агути также способствует ожирению, противодействуя меланоцитстимулирующему гормону (MSH) на рецепторе меланокортина (MC4R), поскольку MC4R отвечает за регулирование потребления пищи путем подавления сигналов аппетита. [25] Увеличение аппетита связано с изменениями в метаболизме питательных веществ из-за паракринного действия агути на жировую ткань, повышения уровня липогенеза в печени , снижения уровня липолиза и увеличения гипертрофии адипоцитов. [26] Это увеличивает массу тела и приводит к трудностям с потерей веса, поскольку метаболические пути нарушаются. Гиперинсулинемия вызвана мутациями агути , поскольку белок агути функционирует кальций-зависимым образом, увеличивая секрецию инсулина в бета-клетках поджелудочной железы, увеличивая риск резистентности к инсулину . [27] Повышенное образование опухолей происходит из-за увеличения скорости митоза агути , которые локализуются в эпителиальных и мезенхимальных тканях. [21]

Для правильного функционирования агути требуется метилирование ДНК. Метилирование происходит в шести богатых гуанин-цитозином (GC) последовательностях в 5'-длинном концевом повторе элемента IAP в жизнеспособной желтой мутации. [24] Метилирование гена приводит к тому, что ген не экспрессируется, поскольку это приводит к отключению промотора . Внутриутробно диета матери может вызвать метилирование или деметилирование. Когда эта область неметилирована, происходит эктопическая экспрессия агути и проявляются желтые фенотипы, поскольку вместо эумеланина экспрессируется феомеланин. Когда область метилирована, агути экспрессируется нормально и возникают серые и коричневые фенотипы (эумеланин). Эпигенетическое состояние элемента IAP определяется уровнем метилирования, поскольку люди демонстрируют широкий спектр фенотипов в зависимости от степени метилирования ДНК. [24] Повышенное метилирование коррелирует с повышенной экспрессией нормального гена агути . Низкий уровень метилирования может вызвать импринтинг генов , в результате чего потомство демонстрирует фенотипы, соответствующие своим родителям, поскольку эктопическая экспрессия агути наследуется посредством негеномных механизмов. [22] [28]
Метилирование ДНК определяется внутриутробно питанием матери и воздействием окружающей среды. [24] Метил синтезируется de novo , но поступает с пищей за счет фолиевой кислоты, метионина, бетаина и холина, поскольку эти питательные вещества участвуют в последовательном метаболическом пути синтеза метила. [29] Для синтеза метила необходимо достаточное количество цинка и витамина B12 , поскольку они действуют как кофакторы для переноса метильных групп. [6]
Когда неадекватный метил доступен на ранних стадиях эмбрионального развития, метилирование ДНК не может произойти, что увеличивает эктопическую экспрессию агути и приводит к появлению летального желтого и жизнеспособного желтого фенотипов, которые сохраняются и во взрослом возрасте. Это приводит к развитию синдрома желтого ожирения , что нарушает нормальное развитие и повышает предрасположенность к развитию хронических заболеваний. Обеспечение высокого содержания метиловых эквивалентов в рационе матери является ключевой профилактической мерой для снижения эктопической экспрессии агути у потомства. Вмешательство в диету с помощью добавок метила уменьшает импринтинг в локусе агути , поскольку повышенное потребление метила приводит к тому, что элемент IAP становится полностью метилированным, а эктопическая экспрессия агути снижается . [30] Это снижает долю потомства с желтым фенотипом и увеличивает количество потомков, напоминающих мышей дикого типа агути с серой шерстью. [22] Две генетически идентичные мыши могли сильно отличаться фенотипически из-за диеты матерей, когда мыши находились в утробе матери. Если у мышей есть ген агути, он может проявиться из-за того, что мать придерживается типичной диеты, и у потомства будет желтая шерсть. Если бы та же мать питалась богатой метилом пищей с добавлением цинка, витамина B12 и фолиевой кислоты, то ген агути у потомства, скорее всего, стал бы метилированным, он не был бы выражен, и цвет шерсти вместо этого был бы коричневым. У мышей желтый цвет шерсти также связан с проблемами со здоровьем, включая ожирение и диабет. [31]
Сигнальный белок агути (ASP) является человеческим гомологом мышиного агути . Он кодируется геном агути человека на 20 хромосоме и представляет собой белок, состоящий из 132 аминокислот. Он экспрессируется гораздо шире, чем мышиный агути , и обнаруживается в жировой ткани, поджелудочной железе, семенниках и яичниках, тогда как мышиный агути экспрессируется исключительно в меланоцитах. [6] ASP имеет 85% сходство с мышиной формой агути . [32] Поскольку эктопическая экспрессия мышиного агути приводит к развитию синдрома желтого ожирения , ожидается, что это будет характерно и для людей. [32] Синдром желтого ожирения увеличивает развитие многих хронических заболеваний, включая ожирение, сахарный диабет II типа и онкогенез. [13]
ASP имеет фармакологическую активацию, аналогичную мышиному агути , поскольку рецепторы меланокортина ингибируются посредством конкурентного антагонизма. [33] Ингибирование меланокортина с помощью ASP также может осуществляться неконкурентными методами, что расширяет диапазон его эффектов. [21] Функция ASP отличается от мышиного агути . ASP влияет на качество пигментации волос, тогда как мышиный агути контролирует распределение пигментов, определяющих цвет шерсти. [22] ASP обладает нейроэндокринными функциями, соответствующими мышиным агути , поскольку он агонизирует через нейроны AgRP в гипоталамусе и противодействует MSH в MC4R, которые снижают сигналы насыщения. AgRP действует как стимулятор аппетита и повышает аппетит, одновременно снижая метаболизм. Благодаря этим механизмам AgRP может быть связан с увеличением массы тела и ожирением как у людей, так и у мышей. [34] Чрезмерная экспрессия AgRP связана с ожирением у мужчин, в то время как определенные полиморфизмы AgRP связаны с расстройствами пищевого поведения, такими как нервная анорексия . [35] [36] Механизм, лежащий в основе гиперинсулинемии у людей, согласуется с мышиным агути , поскольку секреция инсулина усиливается за счет чувствительной к кальцию передачи сигналов в бета-клетках поджелудочной железы. [6] Механизм онкогенеза, индуцированного ASP, у человека остается неизвестным. [6]
Эта статья включает текст из Национальной медицинской библиотеки США , который находится в свободном доступе .