Аноксическая деполяризация — это прогрессирующая и неконтролируемая деполяризация нейронов во время инсульта или ишемии головного мозга , при которой происходит недостаточное кровоснабжение мозга . [1] Аноксическая деполяризация индуцируется потерей проницаемости селективной мембраны нейронов и ионными градиентами через мембрану, которые необходимы для поддержания активности нейронов. В норме насос Na+/K+-АТФазы поддерживает трансмембранные градиенты ионов K + и Na + , но при аноксическом повреждении головного мозга запас энергии для приведения в действие этого насоса теряется. [2] Признаками аноксической деполяризации являются повышенные концентрации внеклеточных ионов K + , внутриклеточных ионов Na + и Ca2 + , а также внеклеточных глутамата и аспартата . Глутамат и аспартат обычно присутствуют в качестве основных возбуждающих нейротрансмиттеров мозга , но высокие концентрации активируют ряд нижестоящих апоптотических и некротических путей . Это приводит к дисфункции нейронов и смерти мозга . [3]

Нейроны функционируют в центральной нервной системе , генерируя сигналы из синапсов , и это работает только в соответствующей химической среде. [4] Электрический сигнал передается через натриевые каналы и протекающие калиевые каналы , в которых внутриклеточная концентрация ионов K + выше, чем соответствующая внеклеточная концентрация, тогда как внеклеточные концентрации ионов Na + , Ca 2+ и Cl - выше, чем соответствующие внутриклеточные концентрации. Такое неравномерное распределение ионов поддерживается Na + /K + -АТФазным насосом, который активно выкачивает Na + и K + в клетку в соотношении 3:2 на использованную АТФ . Мембранный потенциал покоя нейрона составляет -70 мВ из-за негерметичных калиевых каналов. [5] Когда нейрон деполяризуется из-за притока ионов Na + через натриевые каналы, мембрана достигает порогового потенциала , а затем запускает потенциал действия «все или ничего» , который либо распространяется вниз по аксону , либо переходит к другим нейронам через несколько промежутков . узлы , которые их связывают. [4]
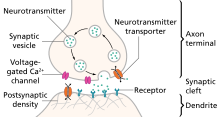
Химический сигнал ( синаптическая передача ) начинается с потенциала действия, который распространяется вниз по аксону так называемого пресинаптического окончания , вызывая приток Ca 2+ , который заставляет синаптические пузырьки сливаться и высвобождать нейротрансмиттеры посредством экзоцитоза в синаптическую щель . [5] [6] Высвобожденные нейротрансмиттеры затем связывают свои специфические нейрорецепторы на постсинаптической мембране или активируют их специфические лиганд-управляемые ионные каналы , запуская потенциал действия, который может быть либо возбуждающим , либо тормозящим , в зависимости от природы лиганд-управляемых ионный канал. Нейромедиаторы удаляются из синаптической щели либо путем ферментативной деградации, либо путем повторного захвата тем же пресинаптическим нейроном посредством эндоцитоза или специфических переносчиков нейромедиаторов . [4]
В течение нескольких секунд после начала инсульта мозг реагирует переходом в состояние метаболической депрессии , при котором потребление энергии снижается, чтобы компенсировать снижение производства энергии. Метаболическая депрессия возникает в результате подавления синаптической передачи и гиперполяризации .
Подавление синаптической передачи происходит потому, что пресинаптический импульс временно не может вызвать высвобождение нейромедиаторов, что в сочетании с измененной ионной проводимостью и изменением постсинаптических нейрорецепторов делает синапсы невосприимчивыми к связыванию нейромедиаторов, тем самым подавляя постсинаптическое возбуждение. [5]
С другой стороны, гиперполяризация используется для снижения активности нейронов путем установления высокого порогового потенциала для срабатывания потенциала действия. Эта энергосберегающая реакция обусловлена непрерывным входящим током ионов K + , которые помогают поддерживать градиент ионов мембраны до тех пор, пока сопротивление не будет нарушено и не начнется бескислородная деполяризация. [5]
Поддержание баланса между внутриклеточными и внеклеточными концентрациями ионов на постсинаптическом терминале имеет решающее значение для нормальной функции нейронов. Во время истощения кислорода в мозге два события, которые инициируют, а также распространяют аноксическую деполяризацию, включают чрезмерный приток катионов, а также отток АТФ в постсинаптическом терминале . [1] Рецепторы, которые обеспечивают этот приток и отток, представляют собой ионотропные рецепторы , которые представляют собой лиганд-управляемые ионные каналы, которые связывают специфические нейротрансмиттеры, высвобождаемые из синаптических везикул пресинаптического окончания, чтобы вызвать открытие каналов, которые служат проводниками. для катионов, которые, в свою очередь, инициируют потенциал действия на постсинаптических терминалях нормально функционирующих нейронов. [7]
Ключевым игроком в драматическом процессе притока катионов является глутамат, возбуждающий нейромедиатор, который вызывает эксайтотоксичность во время аноксической деполяризации. [8] Было обнаружено, что ряд ионотропных рецепторов способствуют аноксической деполяризации мембран нервных клеток . К ним относятся рецепторы NMDA , рецепторы AMPA , пуринергические рецепторы P2X7 , каналы паннексина (Panx1), каналы переходного рецепторного потенциала (TRP) и кислоточувствительные ионные каналы (ASIC). [1]
При ишемии головного мозга глутамат высвобождается в избытке из пресинаптического терминаля, что приводит к неконтролируемому открытию глутаматных рецепторов , в том числе NMDA и AMPA-рецепторов, что обеспечивает избыточный приток Са 2+ во внутриклеточную среду. Пуринергические и NMDA-рецепторы активируют каналы паннексина-1, которые становятся гиперактивными и позволяют высвобождать АТФ из внутриклеточной среды. По мере увеличения внеклеточного глутамата и АТФ несколько комплексов активируются и сходятся в каскадных путях апоптоза и некроза, которые вызывают повреждение и гибель нейронов. [1]
.jpg/440px-Low_Ca2+_buffering_and_excitotoxicity_under_physiological_stress_and_pathophysiological_conditions_in_motor_neuron_(MNs).jpg)
После аноксической деполяризации в области инфаркта высвобождение глутамата и аспартата во внеклеточное пространство вызывает неконтролируемую внутриклеточную мобилизацию Ca 2+ , главным образом через NMDA-рецепторы. [9] Это критическая стадия в развитии повреждения нейронов, поскольку именно перегрузка Ca 2+ приводит к нескольким последующим каскадам событий, которые приводят к некротической гибели нейронов или к апоптозу, включая продукцию свободных радикалов и оксида азота. которые вызывают повреждение мембраны. [10]
Другим цитотоксическим явлением, которое следует за аноксической деполяризацией, является накопление лактата и ацидоз в результате гликолиза, который вызывает повреждение митохондрий . [10] Ишемическое инсульт также вызывает нарушение гематоэнцефалического барьера . [9] Другие сопутствующие повреждения включают липолиз , протеолиз , набухание клеток, дезагрегацию микротрубочек и фрагментацию ДНК . [5]
Нейроны более восприимчивы к ишемии головного мозга, чем поддерживающие глиальные клетки , поскольку нейроны имеют более высокую потребность в энергии, проводят потенциал действия и производят глутамат, тогда как глиальные клетки лишены этих свойств. Тем не менее, нейроны различаются между собой по своей чувствительности к ишемии в зависимости от конкретных свойств, которые они проявляют, связанных с их расположением в мозге. [11]
Избирательная уязвимость заключается в том, что некоторые части мозга более чувствительны к гипоксии , чем другие, и, следовательно, к ишемическому инсульту . [10] Склонные к аноксии клетки головного мозга включают пирамидные клетки гиппокампа CA1 , клетки Пуркинье мозжечка , пирамидные нейроны неокортекса в некоторых слоях, базальные ганглии , ретикулярные нейроны таламуса и нейроны ствола мозга . [12]
В то время как базальные ганглии, клетки Пуркинье мозжечка, гиппокамп и клетки неокортекса более уязвимы к транзиторной ишемической атаке (ТИА), ствол мозга и ретикулярные нейроны таламуса более уязвимы к длительной ишемической атаке (собственно инсульту). [11] Между тем, пирамидные клетки гиппокампа были идентифицированы как наиболее уязвимые клетки к ишемии. [12] Одно из возможных объяснений существования избирательной уязвимости объясняет это явление разным количеством глутамата, вырабатываемого разными нейронами, поскольку именно высвобождение глутамата в синаптическую щель запускает приток Ca 2+ , который, в свою очередь, запускает биохимические процессы, повреждающие нейроны. нейроны. [11] В другом исследовании было установлено, что вариации в экспрессии генов немедленной ранней стадии и белка теплового шока вызывают избирательную уязвимость. [12]
Расписная черепаха ( Chrysemys picta ) использует механизм метаболической депрессии для борьбы с истощением кислорода. [13] В течение нескольких минут после начала гипоксии в мозгу черепахи снижается мозговой кровоток, который в конечном итоге прекращается. Между тем, гликолиз стимулируется для поддержания почти оптимального производства АТФ . [3] Эта компенсаторная стимуляция гликолиза происходит потому, что в мозгу черепахи цитохромы а и а 3 имеют низкое сродство к кислороду. [13] Анаэробный гликолиз приводит к перегрузке лактатом, которую черепахи в некоторой степени компенсируют за счет увеличения выработки CaCO 3 в панцире и костях . [3]
Однако гликолиз неэффективен для производства АТФ, и для поддержания оптимальной концентрации АТФ мозг черепахи снижает потребление АТФ, подавляя активность нейронов и постепенно высвобождая аденозин . Это восстанавливает баланс потребления/производства АТФ, который затем поддерживается за счет снижения ионной проводимости и высвобождения ГАМК . Снижение активности нейронов приводит черепаху в коматозное состояние на время аноксии. [14]
Еще одним устойчивым к аноксии животным, которое обычно используется в качестве модели для изучения гипоксии в мозге млекопитающих, является карась , который может выжить в даже более экстремальных аноксических условиях, чем нарисованная черепаха. В отличие от C. picta , который принимает столь радикальные меры, чтобы впасть в коматозное состояние, чтобы поддерживать оптимальную концентрацию АТФ, карась не впадает в коматозное состояние при аноксии. Вместо этого он остается активным, поддерживая нормальный сердечный выброс , а также увеличивая мозговой кровоток. [5] Несмотря на то, что гликолиз стимулируется на ранней стадии гипоксии как у карася, так и у C. picta , карась способен оставаться активным благодаря своей способности перенаправлять гликолитический путь, так что лактат превращается в этанол , который может затем выбрасываться в воду через жабры , предотвращая тем самым перегрузку лактатом и ацидоз. [3]
Поскольку у карася есть более эффективная стратегия предотвращения накопления лактата, чем у C. picta , первоначальный гликолиз продолжается не прекращаясь, процесс, называемый эффектом Пастера . [14] Чтобы не отставать от быстрого метаболизма глюкозы посредством гликолиза, а также поддерживать баланс между выработкой и потреблением АТФ, карась умеренно подавляет свою двигательную активность, высвобождает ГАМК и избирательно подавляет некоторые ненужные сенсорные функции. [14] Карась также противодействует разрушительному воздействию кислородного голодания, плавая в более прохладную воду – явление, известное как добровольная гипотермия . [3]
Было обнаружено, что мозг нескольких новорожденных млекопитающих способен обеспечивать устойчивость к аноксии аналогично тому, как это происходит у водных организмов, толерантных к аноксии. [13] Это все еще относительно новая область исследований, которая может иметь клиническое значение в борьбе с инсультом у людей. Исследование, изучавшее толерантность к аноксии у новорожденных млекопитающих, выявило два основных способа, с помощью которых они справляются с острой гипоксией . В то время как большинство новорожденных преимущественно снижают скорость метаболизма, чтобы сохранить энергию во время гипоксии, некоторые новорожденные млекопитающих, такие как свиньи, олени и другие животные этого класса, которые с рождения способны к высокой степени независимой активности, используют гиперпноэ . (аномально быстрое или глубокое дыхание). [15] Почему метаболическая депрессия менее эффективна у взрослых млекопитающих по сравнению с новорожденными, на данный момент неясно. Из-за этических проблем толерантность к аноксии не тестировалась на новорожденных людях.
В настоящее время не существует эффективного способа борьбы с инсультом. Единственным препаратом, одобренным FDA для лечения инсульта, является растворяющий тромбы генетически модифицированный фермент , называемый тканевым активатором плазминогена , который необходимо вводить в течение 9 часов после появления симптомов [1], чтобы он был эффективным в уменьшении повреждений после ишемического инсульта . гладить . [16]
Многие клинические испытания в попытке разработать эффективные нейропротекторные препараты для борьбы с инсультом потерпели неудачу, возможно, потому, что эти препараты воздействуют только на один аспект инсульта и, следовательно, игнорируют тот факт, что инсульт является многогранной проблемой. Некоторые из потенциальных методов лечения инсульта, которые были протестированы рядом исследователей с использованием нескольких моделей животных, включают лиганды рецептора сигма-1 для модуляции высвобождения Ca 2+ , антагонисты рецептора NMDA для предотвращения перегрузки Ca 2+ и ионные каналы. блокаторы , чтобы предотвратить чрезмерные потоки ионов. [ нужна цитата ]