Ацетилацетонаты металлов представляют собой координационные комплексы , производные ацетилацетонат-аниона ( CH
3КОЧКОХ−
3) и ионы металлов, обычно переходных металлов . Бидентатный лиганд ацетилацетонат часто обозначают сокращенно acac . Обычно оба атома кислорода связываются с металлом, образуя шестичленное хелатное кольцо. Простейшие комплексы имеют формулы M(acac) 3 и M(acac) 2 . Также многочисленны смешанно-лигандные комплексы, например VO(acac) 2 . Также были разработаны варианты ацетилацетоната с множеством заместителей вместо метила (RCOCHCOR ' - ). [1] Многие такие комплексы растворимы в органических растворителях , в отличие от родственных галогенидов металлов. Благодаря этим свойствам комплексы асас иногда используются в качестве предшественников катализаторов и реагентов. Приложения включают их использование в качестве «реагентов сдвига» ЯМР , катализаторов органического синтеза и предшественников промышленных катализаторов гидроформилирования . С
5ЧАС
7О−
2в некоторых случаях также связывается с металлами через центральный атом углерода; этот тип связи более характерен для переходных металлов третьего ряда, таких как платина (II) и иридий (III).
Обычный синтез включает обработку соли металла ацетилацетоном acacH: [2]
Добавление основания способствует удалению протона из ацетилацетона и сдвигает равновесие в пользу комплекса. Оба кислородных центра связываются с металлом, образуя шестичленное хелатное кольцо. В некоторых случаях хелатный эффект настолько силен, что для образования комплекса не требуется добавление основания. Некоторые комплексы получают метатезисом с использованием Tl (acac).
В большинстве своих комплексов асас образует шестичленные хелатные кольца C 3 O 2 M. [3] Кольцо M(acac) плоское с плоскостью симметрии, делящей кольцо пополам.
Кольцо acacM обычно демонстрирует ароматический характер, что соответствует делокализованной связи в моноанионной части C 3 O 2 . В соответствии с этим сценарием, в некоторых комплексах лиганд acac подвержен электрофильному замещению, подобному электрофильному ароматическому замещению (в этом уравнении Me = CH 3 ): [4]
С точки зрения счета электронов нейтральный бидентатный O,O-связанный acac-лиганд представляет собой «лиганд LX», т.е. комбинацию основания Льюиса (L) и псевдогалогенида (X).
Исключением из классического описания, представленного выше, является бис(пиридин)-аддукт ацетилацетоната хрома(II) с неиннокентным асас -2- лигандом. [5]
Обработка TiCl 4 ацетилацетоном дает TiCl 2 (acac) 2 , октаэдрический комплекс красного цвета с симметрией C 2 :
Эта реакция не требует основания. В атмосферных условиях дибромкомплекс легко гидролизуется (1 ч), тогда как дихлор- и дифторкомплексы гидролизуются трудно (1-3 сут). Комплекс TiCl 2 (acac) 2 является флюсовым в растворе, спектр ЯМР демонстрирует одиночный метильный резонанс при комнатной температуре. [6]
В отличие от Ti(IV), как Zr(IV), так и Hf(IV) связывают четыре бидентатных ацетилацетоната, что отражает больший радиус этих металлов. Ацетилацетонат гафния и ацетилацетонат циркония имеют квадратную антипризматическую структуру.
Из ацетилацетонатов титана(III) хорошо изучен Ti(acac) 3 . Это соединение синего цвета образуется из трихлорида титана и ацетилацетона. [3]
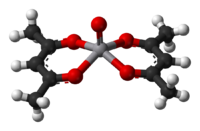
Ацетилацетонат ванадила представляет собой комплекс синего цвета с формулой V(O)(acac) 2 . Этот комплекс содержит ванадильную группу (IV), и известны многие родственные соединения. Молекула имеет квадратно-пирамидальную форму с идеализированной симметрией C2v . Комплекс катализирует эпоксидирование аллильных спиртов пероксидами. Ацетилацетонат ванадия(III) представляет собой твердое вещество темно-коричневого цвета. Комплексы β-дикетоната ванадия используются в качестве прекатализаторов в промышленном производстве этилен-пропилен-диеновых эластомеров (ЭПДМ). Их часто оценивают для других применений, связанных с проточными окислительно-восстановительными батареями, диабетом и повышением активности инсулина, а также в качестве предшественников неорганических материалов при сердечно-сосудистых заболеваниях. [7]
Ацетилацетонат хрома(III) , Cr(acac) 3 , представляет собой типичный октаэдрический комплекс, содержащий три acac - лиганда. Как и большинство подобных соединений, он хорошо растворим в неполярных органических растворителях. Этот конкретный комплекс, имеющий три неспаренных электрона, используется в качестве агента спиновой релаксации для повышения чувствительности в количественной ЯМР-спектроскопии углерода-13 . [8] Ацетилацетонат хрома (II) представляет собой высокочувствительное к кислороду соединение светло-коричневого цвета. Комплекс имеет квадратную плоскую структуру , слабо связанную со стопками в твердом состоянии. Он изоморфен Pd(acac) 2 и Cu(acac) 2 . [9] Mo(acac) 3 , фиолетовый, чувствительный к воздуху комплекс, получают метатезисом солей из гексахлормолибдата. [10] [11]

Mn(acac) 3 получен сопропорционированием соединения марганца(II) Mn(acac) 2 с перманганатом калия в присутствии дополнительного ацетилацетона. [12] Альтернативно прямая реакция ацетилацетона с перманганатом калия . [13] С точки зрения электронной структуры, Mn(acac) 3 является высокоспиновым . Его искаженная октаэдрическая структура отражает геометрические искажения из-за эффекта Яна-Теллера . Две наиболее распространенные структуры этого комплекса включают одну с тетрагональным удлинением и одну с тетрагональным сжатием. Что касается удлинения, две связи Mn–O имеют длину 2,12 Å, а остальные четыре - 1,93 Å. При сжатии две связи Mn–O имеют длину 1,95 Å, а остальные четыре — 2,00 Å. Эффекты тетрагонального удлинения заметно более значительны, чем эффекты тетрагонального сжатия. [14]
В органической химии Mn(acac) 3 использовался в качестве одноэлектронного окислителя для связывания фенолов. [15]
Оценены скорости переноса электронов для Mn(acac)3. [16] -
Ацетилацетонат железа(III) , Fe(acac) 3 , представляет собой красный высокоспиновый комплекс, хорошо растворимый в органических растворителях. Это высокоспиновый комплекс с пятью неспаренными электронами. Иногда его исследовали в качестве предшественника катализатора. [17] Fe(acac) 3 был частично разделен на его Δ и Λ изомеры . [18] Комплекс железа Fe(acac) 2 является олигомерным.
Как и железо, Ru(III) образует стабильный трис(ацетилацетонат) . Восстановление этого производного Ru(III) в присутствии других лигандов приводит к образованию смешанно-лигандных комплексов, например Ru(acac) 2 (алкен) 2 . [19]

Трис(ацетилацетонато)кобальт(III) , Co(acac) 3 , представляет собой низкоспиновый диамагнитный комплекс. Как и другие соединения типа M(acac) 3 , этот комплекс является хиральным (имеет ненакладываемое зеркальное отображение). [18]
Синтез Co(acac) 3 предполагает использование окислителя, поскольку предшественники кобальта двухвалентны:
Комплекс «Co(acac) 2 », как и комплекс никеля с аналогичной стехиометрией, обычно изолируется с двумя дополнительными лигандами, т.е. октаэдрическим Co(acac) 2 L 2 . Безводная форма существует в виде тетрамера [Co(acac) 2 ] 4 . Как и тримерный комплекс никеля, этот тетрамер проявляет ферромагнитные взаимодействия при низких температурах. [20]
Известны Ir(acac) 3 и Rh(acac) 3 . Известен второй изомер связи иридиевого комплекса, транс -Ir(acac) 2 ( CH (COMe) 2 )(H 2 O). Это производное с C -связью является предшественником гомогенных катализаторов активации C – H и связанных с ним химических процессов. [21] [22] [23] [24]
Двумя хорошо изученными ацетилацетонатами родия(I) и иридия(I) являются Rh(acac)(CO) 2 и Ir(acac)(CO) 2 . Эти комплексы плоскоквадратные, симметрии C 2v .

Бис(ацетилацетонат) никеля(II) существует в виде триметаллического комплекса [Ni(acac) 2 ] 3 . Объемные бета-дикетонаты образуют красные мономерные плоско-квадратные комплексы. [25] Бис(ацетилацетонат) никеля(II) реагирует с водой с образованием октаэдрического [26] аддукта [Ni(acac) 2 (H 2 O) 2 ] , мелово-зеленого твердого вещества.
В отличие от сложного магнетизма и структуры Ni(acac) 2 , бис(ацетилацетонат) платины(II) и бис(ацетилацетонат) палладия(II) являются диамагнитными монометаллическими соединениями.
Cu(acac) 2 получают обработкой ацетилацетона водным раствором Cu(NH
3)2+
4. Он доступен коммерчески, катализирует реакции сочетания и переноса карбена.
В отличие от производного меди (II), ацетилацетонат меди (I) представляет собой чувствительный к воздуху олигомерный вид. Он используется для катализа присоединения Михаэля . [27]
Моноаквокомплекс Zn(acac) 2 H 2 O ( т. пл. 138–140 °С) пятикоординированный, имеет квадратно-пирамидальную структуру. [28] Комплекс находит некоторое применение в органическом синтезе . [29] Дегидратация этого вида дает гигроскопичное безводное производное (т.пл. 127 °C). [30] Это более летучее производное использовалось в качестве предшественника пленок ZnO .
Бесцветный ацетилацетонат алюминия (Al(acac) 3 ) по структуре аналогичен другим трис-комплексам, например [Fe(acac) 3 ]. Трисацетилацетонаты лантаноидов часто имеют координационные числа выше 8.
Многие варианты ацетилацетонатов хорошо разработаны. Гексафторацетилацетонаты и трифторацетилацетонаты образуют комплексы, которые часто структурно родственны обычным ацетилацетонатам, но являются более кислотными по Льюису и более летучими. Комплекс Eufod Eu ( OCC(CH 3 ) 3 CHCOC 3 F 7 ) 3 имеет сложный частично фторированный лиганд. Этот комплекс представляет собой кислоту Льюиса, образующую аддукты с различными твердыми основаниями.
Один или оба кислородных центра в ацетилацетонате могут быть заменены группами RN, что приводит к образованию лигандов Nacac и Nacnac .
С
5ЧАС
7О−
2в некоторых случаях также связывается с металлами через центральный атом углерода ( С3 ); этот тип связи более характерен для переходных металлов третьего ряда, таких как платина (II) и иридий (III). Комплексы Ir(acac) 3 и соответствующие аддукты с основанием Льюиса Ir(acac) 3 L (L = амин ) содержат один связанный с углеродом лиганд acac. ИК-спектры ацетилацетонатов с О -связью характеризуются относительно низкоэнергетическими полосами ν CO 1535 см -1 , тогда как в ацетилацетонатах с углеродной связью карбонильное колебание происходит ближе к нормальному диапазону для кетона C=O, т.е. 1655 см -1. 1 .
{{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь )