В металлоорганической химии ацетилид относится к химическим соединениям с химическими формулами MC≡CH и MC≡CM , где M — металл . [1] Этот термин используется широко и может относиться к замещенным ацетилидам, имеющим общую структуру RC≡CM (где R представляет собой органическую боковую цепь ). Ацетилиды — реагенты в органическом синтезе . Ацетилид кальция, обычно называемый карбидом кальция, является основным коммерческим соединением.
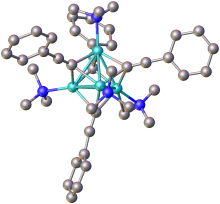

Ацетилиды щелочных и щелочноземельных металлов общей формулы MC≡CM представляют собой солеподобные соединения фазы Цинтла , содержащие C2−
2ионы. Доказательства этого ионного характера можно увидеть в легком гидролизе этих соединений с образованием ацетилена и оксидов металлов. Есть также некоторые доказательства растворимости C.2−
2ионы в жидком аммиаке. [4 ] С2−
2ион имеет основное состояние закрытой оболочки 1 Σ+
г, что делает его изоэлектронным нейтральной молекуле N 2 , [5] , что может придавать ему некоторую стабильность.
Аналогичные ацетилиды, полученные из других металлов, особенно переходных , обладают ковалентным характером и неизменно связаны со своими металлоцентрами. Это можно увидеть в их общей устойчивости к воде (например, ацетилид серебра , ацетилид меди ) и радикально различных химических применениях.
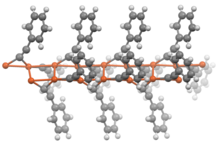
Ацетилиды общей формулы RC≡CM (где R = H или алкил) обычно проявляют свойства, аналогичные их дважды замещенным аналогам. В отсутствие дополнительных лигандов ацетилиды металлов принимают полимерные структуры, в которых ацетилидные группы являются мостиковыми лигандами .
Концевые алкины являются слабыми кислотами : [7]
Для получения ацетилидов из ацетилена и алкинов необходимо использовать металлорганические [8] или неорганические [9] супероснования в растворителях, которые менее кислые, чем концевой алкин. В ранних исследованиях использовался жидкий аммиак , но более распространены эфирные растворители.
Амид лития , [7] LiHMDS , [10] или литийорганические реагенты , такие как бутиллитий , [8] часто используются для образования ацетилидов лития:
Монокалий и мононатрий ацетилид можно получить из различных неорганических реагентов (например, амида натрия ) [9] или из их элементарных металлов, часто при комнатной температуре и атмосферном давлении. [7]
Ацетилид меди(I) можно получить пропусканием ацетилена через водный раствор хлорида меди(I) из-за низкой растворимости равновесия . [7] Аналогично ацетилиды серебра можно получить из нитрата серебра .
Карбид кальция получают путем нагревания углерода с известью ( оксидом кальция ) при температуре примерно 2000 °C. Похожий процесс используется для производства карбида лития .
Ацетилиды типа RC 2 M широко используются при алкинилировании в органической химии . Это нуклеофилы , которые присоединяются к множеству электрофильных и ненасыщенных субстратов. Классическим применением является реакция Фаворского .
Показательной является последовательность, показанная ниже: этилпропиолат депротонируется н -бутиллитием с образованием соответствующего ацетилида. Этот ацетилид присоединяется к карбонильному центру циклопентанона . Гидролитическая обработка выделяет алкиниловый спирт. [11]

Ацетилиды иногда являются промежуточными продуктами реакций сочетания . Примеры включают связь Соногаширы , связь Кадиота-Ходкевича , связь Глейзера и связь Эглинтона .
Некоторые ацетилиды общеизвестно взрывоопасны. [12] Образование ацетилидов представляет опасность при обращении с газообразным ацетиленом в присутствии таких металлов, как ртуть , серебро или медь , или сплавов с их высоким содержанием ( латунь , бронза , серебряный припой ).