Пропилен , также известный как пропен , является ненасыщенным органическим соединением с химической формулой CH3CH =CH2 . Он имеет одну двойную связь и является вторым по простоте членом класса алкенов углеводородов . Это бесцветный газ со слабым запахом, похожим на запах нефти. [ 4]
Пропилен является продуктом горения лесных пожаров, сигаретного дыма, выхлопных газов автомобилей и самолетов. [5] Он был открыт в 1850 году капитаном (позднее генерал-майором [6] ) Джоном Уильямсом Рейнольдсом, учеником А. В. фон Хоффмана , как единственный газообразный продукт термического разложения амилового спирта, реагирующий с хлором и бромом. [7]
Доминирующей технологией производства пропилена является паровой крекинг с использованием пропана в качестве сырья . Крекинг пропана дает смесь этилена , пропилена, метана , водорода и других родственных соединений. Выход пропилена составляет около 15%. Другим основным сырьем является нафта, особенно на Ближнем Востоке и в Азии. [8] Пропилен можно отделить фракционной перегонкой от углеводородных смесей, полученных в результате крекинга и других процессов переработки; пропен нефтеперерабатывающего класса составляет около 50-70%. [9] В Соединенных Штатах сланцевый газ является основным источником пропана.
В технологии преобразования триолефинов или олефинов Филлипса пропилен взаимопревращается с этиленом и 2-бутенами . Используются рениевые и молибденовые катализаторы: [10]
Технология основана на реакции метатезиса олефинов , открытой в компании Phillips Petroleum Company . [11] [12] Достигается выход пропилена около 90% масс.
Связанный процесс — метанол-в-олефины/метанол-в-пропен . Он преобразует синтез-газ (синтез-газ) в метанол , а затем преобразует метанол в этилен и/или пропен . В результате процесса в качестве побочного продукта образуется вода. Синтез-газ получают путем реформирования природного газа или паровым реформированием нефтепродуктов, таких как нафта, или путем газификации угля или природного газа.
Высокоинтенсивный каталитический крекинг с псевдоожиженным слоем (FCC) использует традиционную технологию FCC в жестких условиях (более высокие соотношения катализатора к маслу, более высокие скорости впрыска пара, более высокие температуры и т. д.) для того, чтобы максимизировать количество пропена и других легких продуктов. Высокоинтенсивный блок FCC обычно питается газойлями (парафинами) и остатками и производит около 20–25% (по массе) пропена на сырье вместе с большими объемами автомобильного бензина и побочных продуктов дистилляции. Эти высокотемпературные процессы являются дорогостоящими и имеют высокий углеродный след. По этим причинам альтернативные пути получения пропилена продолжают привлекать внимание. [13]
Технологии производства пропилена по назначению разрабатывались на протяжении всего двадцатого века. Из них технологии дегидрирования пропана, такие как процессы CATOFIN и OLEFLEX, стали обычными, хотя они по-прежнему составляют меньшинство рынка, при этом большая часть олефина поступает из вышеупомянутых технологий крекинга. Платиновые, хромовые и ванадиевые катализаторы широко распространены в процессах дегидрирования пропана.
Производство пропена оставалось неизменным на уровне около 35 миллионов тонн (только в Европе и Северной Америке) с 2000 по 2008 год, но оно росло в Восточной Азии, особенно в Сингапуре и Китае. [14] Общее мировое производство пропена в настоящее время составляет примерно половину от производства этилена.
Использование сконструированных ферментов изучалось, но не было коммерциализировано. [15]
Продолжаются исследования по использованию катализаторов-носителей кислорода для окислительного дегидрирования пропана. Это дает несколько преимуществ, поскольку этот механизм реакции может происходить при более низких температурах, чем обычное дегидрирование, и может не быть ограничен равновесием, поскольку кислород используется для сжигания побочного продукта водорода. [16]
Пропен является вторым по важности исходным продуктом в нефтехимической промышленности после этилена . Он является сырьем для широкого спектра продуктов. Производители полипропилена потребляют почти две трети мирового производства. [17] Конечные применения полипропилена включают пленки, волокна, контейнеры, упаковку, а также крышки и затворы. Пропен также используется для производства важных химикатов, таких как пропиленоксид , акрилонитрил , кумол , масляный альдегид и акриловая кислота . В 2013 году во всем мире было переработано около 85 миллионов тонн пропена. [17]
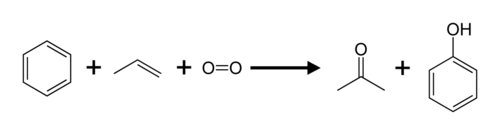
Пропен и бензол преобразуются в ацетон и фенол посредством кумольного процесса .
Пропен также используется для производства изопропилового спирта (пропан-2-ола), акрилонитрила , пропиленоксида и эпихлоргидрина . [18] Промышленное производство акриловой кислоты включает каталитическое частичное окисление пропена. [19] Пропилен является промежуточным продуктом в окислении в акриловую кислоту.
В промышленности и мастерских пропен используется как альтернативное ацетилену топливо при кислородно-топливной сварке и резке , пайке и нагреве металла с целью гибки. Он стал стандартом в продуктах BernzOmatic и других заменителях MAPP, [20] теперь, когда настоящий газ MAPP больше не доступен.
Пропен похож на другие алкены тем, что он относительно легко вступает в реакции присоединения при комнатной температуре. Относительная слабость его двойной связи объясняет его тенденцию реагировать с веществами, способными достичь этого превращения. Реакции алкенов включают: 1) полимеризацию , 2) окисление , 3) галогенирование и гидрогалогенирование , 4) алкилирование , 5) гидратацию , 6) олигомеризацию и 7) гидроформилирование .
Основой гидроформилирования, метатезиса алкенов и полимеризации являются комплексы металл-пропилен , которые являются промежуточными продуктами в этих процессах. Пропилен является прохиральным , что означает, что связывание реагента (такого как металлический электрофил) с группой C=C дает один из двух энантиомеров .
Большая часть пропена используется для формирования полипропилена, очень важного товарного термопластика , посредством полимеризации с ростом цепи . [17] В присутствии подходящего катализатора (обычно катализатора Циглера-Натта ) пропен полимеризуется. Существует несколько способов добиться этого, например, используя высокое давление для суспендирования катализатора в растворе жидкого пропена или пропуская газообразный пропен через реактор с псевдоожиженным слоем . [21]
В присутствии катализаторов пропилен димеризуется с образованием 2,3-диметил-1-бутена и/или 2,3-диметил-2-бутена . [22]
Пропен является продуктом сгорания лесных пожаров, сигаретного дыма, выхлопных газов автомобилей и самолетов. [5] Он является примесью в некоторых отопительных газах. Наблюдаемые концентрации находятся в диапазоне 0,1–4,8 частей на миллиард ( ppb ) в сельском воздухе, 4–10,5 ppb в городском воздухе и 7–260 ppb в образцах промышленного воздуха. [9]
В Соединенных Штатах и некоторых европейских странах было установлено предельное значение в 500 частей на миллион ( ppm ) для профессионального (8-часовое средневзвешенное по времени ) воздействия. Он считается летучим органическим соединением (ЛОС), и его выбросы регулируются многими правительствами, но он не включен в список Агентства по охране окружающей среды США (EPA) как опасный загрязнитель воздуха в соответствии с Законом о чистом воздухе . С относительно коротким периодом полураспада он, как ожидается, не будет биоаккумулироваться. [9]
Пропен имеет низкую острую токсичность при вдыхании и не считается канцерогенным. Исследования хронической токсичности на мышах не дали существенных доказательств, указывающих на неблагоприятные эффекты. Люди, кратковременно подвергавшиеся воздействию 4000 ppm, не испытали никаких заметных эффектов. [23] Пропен опасен из-за своей способности вытеснять кислород как удушающий газ , а также из-за его высокого риска воспламеняемости/взрыва.
Биопропилен — это пропилен на биологической основе . [24] [25] Он был изучен, мотивированный различными интересами, такими как углеродный след . Производство из глюкозы было рассмотрено. [26] Более продвинутые способы решения таких проблем сосредоточены на электрификации, альтернативной паровому крекингу .
Пропен огнеопасен. Пропен обычно хранится в виде жидкости под давлением, хотя его также можно безопасно хранить в виде газа при температуре окружающей среды в одобренных контейнерах. [27]
Пропен обнаружен в межзвездной среде с помощью микроволновой спектроскопии. [28] 30 сентября 2013 года НАСА также объявило, что орбитальный космический аппарат Кассини, являющийся частью миссии Кассини-Гюйгенс , обнаружил небольшие количества природного пропена в атмосфере Титана с помощью спектроскопии. [29] [30]