Sedoreoviridae (ранее Reoviridae ) — это семейство вирусов с двухцепочечной РНК . Вирусы-члены имеют широкий круг хозяев , включая позвоночных , беспозвоночных , растения, простейших и грибы. [1] У них нет липидных оболочек , и они упаковывают свой сегментированный геном в многослойные капсиды . Отсутствие липидной оболочки позволило получить трехмерные структуры этих крупных сложных вирусов (диаметром ~60–100 нм ), что выявило структурную и вероятную эволюционную связь с семейством цистовирусов бактериофагов . [2] В настоящее время в этом семействе насчитывается 97 видов , разделенных на 15 родов в двух подсемействах. [3] Реовирусы могут поражать желудочно-кишечную систему (например, ротавирусы ) и дыхательные пути . [4] Название «рео-» является аббревиатурой от « респираторно - энтерических сиротских » вирусов . [5] Термин « сиротский вирус » относится к тому факту, что некоторые из этих вирусов были обнаружены не связанными с какой-либо известной болезнью. Несмотря на то, что вирусы в семействе Reoviridae были недавно идентифицированы с различными болезнями, первоначальное название все еще используется.
Реовирусные инфекции часто встречаются у людей, но большинство случаев являются легкими или субклиническими. Ротавирусы , однако, могут вызывать сильную диарею и кишечные расстройства у детей, а лабораторные исследования на мышах выявили причастность ортореовирусов к проявлению целиакии у предрасположенных лиц. [6] Вирус можно легко обнаружить в кале , а также извлечь из глоточных или носовых выделений , мочи, спинномозговой жидкости и крови. Несмотря на простоту обнаружения реовирусов в клинических образцах, их роль в заболевании человека или лечении все еще не определена.
Некоторые вирусы этого семейства, такие как фитореовирусы и оризавирусы , заражают растения. Большинство реовирусов, заражающих растения, передаются между растениями насекомыми-переносчиками . Вирусы размножаются как в растении, так и в насекомом, обычно вызывая заболевание у растения, но не нанося или почти не нанося вреда зараженному насекомому. [7] : 148
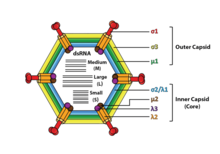
Реовирусы не имеют оболочки и имеют икосаэдрический капсид , состоящий из внешней ( T = 13) и внутренней (T = 2) белковой оболочки. [1] [8] Ультраструктурные исследования показывают, что капсиды вирионов состоят из двух или трех отдельных слоев, что зависит от типа вида. Самый внутренний слой (ядро) имеет икосаэдрическую симметрию T = 1 и состоит из 60 различных типов структурных белков. Ядро содержит сегменты генома, каждый из которых кодирует разнообразную структуру фермента, которая необходима для транскрипции. Ядро покрыто слоем капсида с икосаэдрической симметрией T = 13. Реовирусы имеют уникальную структуру, которая содержит гликолизированный шиповидный белок на поверхности. [9]
Геномы вирусов семейства Reoviridae содержат 9–12 сегментов, которые сгруппированы в три категории в соответствии с их размером: L (большие), M (средние) и S (маленькие). Сегменты варьируются от 0,2 до 3 кб, и каждый сегмент кодирует 1–3 белка (всего 10–14 белков [1] ). Белки вирусов семейства Reoviridae обозначаются греческим символом, соответствующим сегменту, с которого он был транслирован (сегмент L кодирует белки λ, сегмент M кодирует белки μ, а сегмент S кодирует белки σ). [8]

Вирусы семейства Reoviridae имеют геномы, состоящие из сегментированной двухцепочечной РНК (дцРНК). [4] Из-за этого репликация происходит исключительно в цитоплазме, и вирус кодирует несколько белков, которые необходимы для репликации и преобразования генома дцРНК в положительно-полярные РНК. [10]
Вирус может проникать в клетку-хозяина через рецептор на поверхности клетки. Рецептор неизвестен, но считается, что он включает сиаловую кислоту и молекулы адгезии соединений (JAM). [10] Вирус частично освобождается от оболочки протеазами в эндолизосоме, где капсид частично переваривается, чтобы обеспечить дальнейшее проникновение в клетку. Затем основная частица проникает в цитоплазму с помощью пока неизвестного процесса, где геном транскрибируется консервативно, вызывая избыток положительных цепей, которые используются в качестве шаблонов РНК-мессенджера для синтеза отрицательных цепей. [10]
Геном ротавируса разделен на 11 сегментов. Эти сегменты связаны с молекулой VP1, которая отвечает за синтез РНК. На ранних стадиях происходит процесс отбора, так что в клетку попадает 11 различных сегментов РНК. Эта процедура выполняется вновь синтезированными РНК. Это событие гарантирует, что будет получен один из 11 различных сегментов РНК. На поздних стадиях процесс транскрипции происходит снова, но на этот раз не ограничен в отличие от ранних стадий. Для вируса требуются разные количества РНК, поэтому на этапе трансляции есть контрольный механизм. Количество сегментов РНК одинаково, но количество белков разное. Причина этого в том, что сегменты РНК не транслируются с одинаковой скоростью. [7]
Вирусные частицы начинают собираться в цитоплазме через 6–7 часов после заражения. Трансляция происходит путем сканирования утечки, подавления терминации и пропускания рибосом . Вирус покидает клетку-хозяина путем однокомпонентного нетрубчатого вирусного движения, перемещения от клетки к клетке и существования в тельцах окклюзии после смерти клетки и сохранения инфекционности до тех пор, пока не найдет другого хозяина. [1]
Реактивация множественности (МР) — это процесс, посредством которого два или более вирусных генома, каждый из которых содержит инактивирующее повреждение генома, могут взаимодействовать внутри инфицированной клетки, образуя жизнеспособный вирусный геном. Макклейн и Спендлав [11] продемонстрировали МР для трех типов реовирусов после воздействия ультрафиолетового излучения. В их экспериментах частицы реовируса подвергались воздействию доз УФ-излучения, которые были бы летальными при единичных инфекциях. Однако, когда двум или более инактивированным вирусам позволяли инфицировать отдельные клетки-хозяева, происходила МР и производилось жизнеспособное потомство. Как они заявили, реактивация множественности по определению включает в себя некоторый тип репарации. Мишод и др. [12] рассмотрели многочисленные примеры МР в различных вирусах и предположили, что МР является распространенной формой полового взаимодействия у вирусов, которая обеспечивает преимущество рекомбинационной репарации повреждений генома. [ необходима цитата ]
Семейство Reoviridae делится на два подсемейства [13] на основе наличия «башенного» белка на внутреннем капсиде. [14] [15] Из сообщений ICTV: «Название Spinareovirinae будет использоваться для обозначения подсемейства, содержащего шипованные или башенные вирусы, и происходит от «reovirus» и латинского слова «spina» в качестве префикса, что означает шип, обозначая наличие шипов или башенок на поверхности частиц ядра. Термин «шипованный» является альтернативой термину «башенный», который использовался в ранних исследованиях для описания структуры частицы, особенно с циповирусами. Название Sedoreovirinae будет использоваться для обозначения подсемейства, содержащего роды вирусов без башенных вирусов, и происходит от «reovirus» и латинского слова «sedo», что означает гладкий, обозначая отсутствие шипов или башенок на частицах ядра этих вирусов, которые имеют относительно гладкую морфологию». [16]

Семейство Reoviridae делится на следующие подсемейства и роды:
Хотя реовирусы в основном непатогенны для людей, эти вирусы послужили очень продуктивными экспериментальными моделями для изучения вирусного патогенеза . [17] Новорожденные мыши чрезвычайно чувствительны к реовирусным инфекциям и использовались в качестве предпочтительной экспериментальной системы для изучения патогенеза реовирусов. [2]
Было показано, что реовирусы обладают онколитическими (убивающими рак) свойствами, что стимулирует разработку реовирусной терапии для лечения рака. [18] [19] [20]
Реолизин представляет собой препарат реовируса ( штамм серотипа 3 ортореовируса млекопитающих [21] ), который в настоящее время проходит клинические испытания для лечения различных видов рака [22] , включая исследования, которые в настоящее время разрабатываются для изучения роли реолизина в сочетании с другими видами иммунотерапии. [21]
{{cite book}}: |journal=проигнорировано ( помощь )