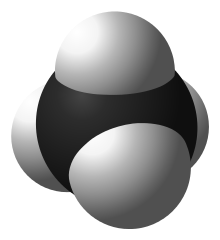
Галометановые соединения являются производными метана ( CH4 ) с одним или несколькими атомами водорода , замещенными атомами галогена ( F , Cl , Br или I ). Галометаны встречаются как в природе, особенно в морской среде, так и в результате деятельности человека, в частности в качестве хладагентов, растворителей, пропеллентов и фумигантов. Многие из них, включая хлорфторуглероды , привлекли широкое внимание, поскольку они становятся активными под воздействием ультрафиолетового света, встречающегося на больших высотах, и разрушают защитный озоновый слой Земли .
Как и сам метан, галометаны являются тетраэдрическими молекулами. Атомы галогена сильно отличаются по размеру и заряду от водорода и друг от друга. Следовательно, большинство галометанов отклоняются от идеальной тетраэдрической симметрии метана. [1]
Физические свойства галометанов зависят от количества и идентичности атомов галогена в соединении. В целом галометаны летучи, но менее летучи, чем метан, из-за поляризуемости галогенидов. Поляризуемость галогенидов и полярность молекул делают их полезными в качестве растворителей. Галометаны гораздо менее огнеопасны, чем метан. В общем, реакционная способность соединений наибольшая у иодидов и наименьшая у фторидов.
Галометаны производятся в промышленных масштабах из обильных прекурсоров, таких как природный газ или метанол , а также из галогенов или галогенидов . Обычно их готовят одним из трех методов. [2]
Этот метод полезен для производства CH 4− n Cl n ( n = 1, 2, 3 или 4). Основные проблемы этого метода в том, что он одновременно генерирует HCl и производит смеси различных продуктов. Использование CH 4 в большом избытке генерирует в основном CH 3 Cl , а использование Cl 2 в большом избытке генерирует в основном CCl 4 , но смеси других продуктов все равно будут присутствовать.
Следы галометанов в атмосфере возникают из-за попадания в нее других неприродных, промышленных материалов.
Многие морские организмы биосинтезируют галометаны, особенно бромсодержащие соединения. [3] Небольшие количества хлорметанов возникают в результате взаимодействия источников хлора с различными углеродными соединениями. Биосинтез этих галометанов катализируется ферментами хлорпероксидазой и бромпероксидазой соответственно. Идеализированное уравнение выглядит следующим образом:
Галоны обычно определяются как углеводороды, в которых атомы водорода заменены бромом, а также другими галогенами. [4] Они обозначаются системой кодовых номеров, аналогичной (но более простой) системе, используемой для фреонов. Первая цифра указывает число атомов углерода в молекуле, вторая — число атомов фтора, третья — атомов хлора, а четвертая — число атомов брома. Если число включает пятую цифру, то пятая цифра указывает число атомов йода (хотя йод в галонах встречается редко). Любые связи, не занятые атомами галогена, затем распределяются между атомами водорода.
Например, рассмотрим галон 1211. Этот галон имеет номер 1211 в своем названии, что говорит о том, что он имеет 1 атом углерода, 2 атома фтора, 1 атом хлора и 1 атом брома. Один атом углерода имеет только четыре связи, все из которых заняты атомами галогена, поэтому водорода нет. Таким образом, его формула CF 2 ClBr , отсюда его название по ИЮПАК — бромхлордифторметан.
Система наименования хладагентов в основном используется для фторированных и хлорированных коротких алканов, используемых в качестве хладагентов. В Соединенных Штатах стандарт указан в ANSI/ASHRAE Standard 34–1992 с дополнительными ежегодными дополнениями. [5] Указанные префиксы ANSI/ASHRAE были FC (фторуглерод) или R (хладагент), но сегодня большинство из них имеют префикс более конкретной классификации:
Система декодирования для CFC-01234a следующая:
Используются и другие системы кодирования.
Гидрофторуглероды (ГФУ) не содержат хлора. Они полностью состоят из углерода, водорода и фтора. Они не оказывают известного воздействия на озоновый слой; сам фтор не является озонотоксичным. [6] [7] Однако ГФУ и перфторуглероды (ПФУ) являются парниковыми газами , которые вызывают глобальное потепление . Две группы галогеналканов, гидрофторуглероды (ГФУ) и перфторуглероды , являются целями Киотского протокола . [8] Аллан Торнтон, президент Агентства по расследованию окружающей среды , неправительственной организации по охране окружающей среды, говорит, что ГФУ в 12 500 раз сильнее углекислого газа в глобальном потеплении. [9] Более высокий потенциал глобального потепления имеет две причины: ГФУ остаются в атмосфере в течение длительных периодов времени, и у них больше химических связей, чем у CO2 , что означает, что они способны поглощать больше солнечной энергии на молекулу, чем углекислый газ. Богатые страны ужесточают меры по борьбе с этими газами. Торнтон говорит, что многие страны напрасно производят эти химикаты только для того, чтобы получить углеродные кредиты. Таким образом, в результате правил торговли углеродом в рамках Киотского протокола, почти половина кредитов развивающихся стран приходится на ГФУ, а Китай получает миллиарды долларов от улавливания и уничтожения ГФУ, которые будут находиться в атмосфере в качестве промышленных побочных продуктов. [10]
Большинство перестановок водорода, фтора, хлора, брома и йода на одном атоме углерода были оценены экспериментально.
Поскольку галометаны имеют множество применений и их легко получать, они представляют большой коммерческий интерес.
Дихлорметан является наиболее важным растворителем на основе галометана. Его летучесть, низкая воспламеняемость и способность растворять широкий спектр органических соединений делают эту бесцветную жидкость полезным растворителем. [2] Он широко используется в качестве средства для снятия краски и обезжиривателя . В пищевой промышленности он ранее использовался для декофеинизации кофе и чая , а также для приготовления экстрактов хмеля и других ароматизаторов . [11] Его летучесть привела к его использованию в качестве пропеллента для аэрозольных спреев и в качестве вспенивающего агента для полиуретановых пен .
Одним из основных применений ХФУ было использование в качестве пропеллентов аэрозолей , включая дозированные ингаляторы для лекарств, используемых для лечения астмы . Перевод этих устройств и методов лечения с ХФУ на пропелленты, которые не разрушают озоновый слой, почти завершен. Производство и импорт в настоящее время запрещены в Соединенных Штатах.

При высоких температурах галоны разлагаются, высвобождая атомы галогена , которые легко соединяются с активными атомами водорода, гася реакции распространения пламени, даже когда остается достаточно топлива, кислорода и тепла. Химическая реакция в пламени протекает как цепная реакция свободных радикалов ; путем секвестрации радикалов, которые распространяют реакцию, галоны способны остановить огонь при гораздо более низких концентрациях , чем требуется для огнетушителей, использующих более традиционные методы охлаждения, лишения кислорода или разбавления топлива. С 2023 года из-за проблем истощения озонового слоя галоновые огнетушители в значительной степени запрещены в некоторых странах, и альтернативы развертываются вооруженными силами США. [12][обновлять]
Системы полного затопления на основе галона 1301 обычно используются при концентрациях не более 7% по объему в воздухе и могут подавлять многие пожары при 2,9% об. Напротив, системы затопления на основе углекислого газа работают при концентрации от 34% по объему (только поверхностное сжигание жидкого топлива) до 75% (пылеуловители). Углекислый газ может вызывать серьезные расстройства при концентрациях 3–6%, а при концентрации 10% он вызывал смерть от паралича дыхания в течение нескольких минут. Галон 1301 вызывает лишь легкое головокружение при своей эффективной концентрации 5%, и даже при 15% подвергшиеся воздействию остаются в сознании, но ослабленными и не испытывают долгосрочных последствий. (Подопытные животные также подвергались воздействию 2% концентрации галона 1301 в течение 30 часов в неделю в течение 4 месяцев, без каких-либо заметных последствий для здоровья. [ необходима ссылка ] ) Галон 1211 также имеет низкую токсичность, хотя он более токсичен, чем галон 1301, и поэтому считается непригодным для систем затопления.
Однако, пожаротушение с помощью Halon 1301 не является полностью нетоксичным; очень высокая температура пламени или контакт с раскаленным металлом могут вызвать разложение Halon 1301 на токсичные побочные продукты. Наличие таких побочных продуктов легко обнаружить, поскольку они включают бромистоводородную кислоту и плавиковую кислоту , которые являются сильно раздражающими. Галоны очень эффективны при пожарах класса A (органические твердые вещества), B (легковоспламеняющиеся жидкости и газы) и C (электрика), но они не подходят для пожаров класса D (металл), так как они не только будут выделять токсичный газ и не смогут остановить пожар, но в некоторых случаях представляют опасность взрыва. Галоны можно использовать при пожарах класса K (кухонные масла и жиры), но они не имеют никаких преимуществ по сравнению со специализированными пенами.
Галон 1301 распространен в системах полного затопления. В этих системах блоки баллонов с галоном поддерживаются под давлением около 4 МПа (600 фунтов на кв. дюйм ) с помощью сжатого азота , а фиксированная сеть трубопроводов ведет к защищенному корпусу. При срабатывании все измеренное содержимое одного или нескольких баллонов выгружается в корпус в течение нескольких секунд через сопла , предназначенные для обеспечения равномерного смешивания по всему помещению. Количество сбрасываемого вещества предварительно рассчитывается для достижения желаемой концентрации, обычно 3–7% об./об. Этот уровень поддерживается в течение некоторого времени, обычно с минимальным временем «выдержки» в десять минут, а иногда и до двадцати минут, чтобы гарантировать, что все предметы остыли, поэтому повторное возгорание вряд ли произойдет, затем воздух в корпусе продувается, как правило, с помощью фиксированной системы продувки, которая активируется соответствующими органами. В это время в корпус могут войти лица, носящие SCBA . (Существует распространенный миф, что это связано с тем, что галон очень токсичен; на самом деле, это связано с тем, что он может вызывать головокружение и легкое нарушение восприятия, а также с риском образования побочных продуктов сгорания.)

Системы затопления могут управляться вручную или автоматически запускаться VESDA или другой автоматической системой обнаружения. В последнем случае сначала на несколько секунд активируется предупреждающая сирена и стробоскопическая лампа, чтобы предупредить персонал о необходимости эвакуации из зоны. Быстрый выброс галона и последующее быстрое охлаждение наполняют воздух туманом и сопровождаются громким, дезориентирующим шумом.
Halon 1301 также используется в истребителе F-16 для предотвращения взрыва паров топлива в топливных баках ; когда самолет попадает в зону с возможностью атаки, Halon 1301 впрыскивается в топливные баки для одноразового использования. Из-за истощения озонового слоя в качестве альтернативы рассматривается трифториодометан ( CF 3 I ). [13]
Halon 1211 обычно используется в ручных огнетушителях, в которых поток жидкого галона направляется пользователем на небольшой пожар. Струя испаряется при пониженном давлении, создавая сильное локальное охлаждение, а также высокую концентрацию галона в непосредственной близости от пожара. В этом режиме пожар тушат путем охлаждения и лишения кислорода в ядре пожара, а также радикального тушения на большей площади. После тушения пожара галон рассеивается, не оставляя следов.
Хлорметан и бромметан используются для введения метильных групп в органическом синтезе . Хлордифторметан является основным предшественником тетрафторэтилена , который является мономерным предшественником тефлона . [1]
Галогеналканы разнообразны по своим свойствам, что затрудняет обобщения. Немногие из них остро токсичны, но многие представляют опасность при длительном воздействии. Некоторые проблемные аспекты включают канцерогенность и повреждение печени (например, четыреххлористый углерод). При определенных условиях горения хлорметаны превращаются в фосген , который является высокотоксичным.