

.tif/lossy-page1-440px-Parasite130059-fig7_Spermiogenesis_in_Pleurogenidae_(Digenea).tif.jpg)
Гликоген — это многоразветвленный полисахарид глюкозы , который служит формой хранения энергии у животных , [2] грибов и бактерий. [3] Это основная форма хранения глюкозы в организме человека.
Гликоген функционирует как одна из трех регулярно используемых форм энергетических резервов: креатинфосфат предназначен для очень краткосрочного хранения, гликоген предназначен для краткосрочного хранения, а запасы триглицеридов в жировой ткани (т. е. в жировых отложениях) предназначены для долгосрочного хранения. Белок, расщепленный на аминокислоты, редко используется в качестве основного источника энергии, за исключением случаев голодания и гликолитического кризиса (см. Биоэнергетические системы ) .
У человека гликоген вырабатывается и хранится в основном в клетках печени и скелетных мышц . [4] [5] В печени гликоген может составлять 5–6% от сырого веса органа: печень взрослого человека весом 1,5 кг может хранить примерно 100–120 граммов гликогена. [4] [6] В скелетных мышцах гликоген содержится в низкой концентрации (1–2% от мышечной массы): скелетные мышцы взрослого человека массой 70 кг хранят примерно 400 граммов гликогена. [4] Небольшое количество гликогена также обнаружено в других тканях и клетках, включая почки , эритроциты , [7] [8] [9] лейкоциты , [10] и глиальные клетки головного мозга . [11] Матка также сохраняет гликоген во время беременности для питания эмбриона. [12]
Количество гликогена, хранящегося в организме, в основном зависит от окислительных волокон 1 типа, [13] [14] физической подготовки, уровня основного обмена и привычек питания. [15] Различные уровни гликогена в покое в мышцах достигаются за счет изменения количества частиц гликогена, а не увеличения размера существующих частиц [14] , хотя большинство частиц гликогена в состоянии покоя меньше их теоретического максимума. [16]
В крови человека постоянно присутствует около 4 граммов глюкозы ; [4] у голодающих людей уровень глюкозы в крови поддерживается постоянным на этом уровне за счет запасов гликогена в печени и скелетных мышцах. [4] Запасы гликогена в скелетных мышцах служат формой хранения энергии для самих мышц; [4] однако распад мышечного гликогена препятствует поглощению глюкозы мышцами из крови, тем самым увеличивая количество глюкозы в крови, доступной для использования в других тканях. [4] Запасы гликогена в печени служат хранилищем глюкозы для использования во всем организме, особенно в центральной нервной системе . [4] Человеческий мозг потребляет около 60% глюкозы в крови у голодающих и малоподвижных людей. [4]
Гликоген – это аналог крахмала , полимера глюкозы , который служит хранилищем энергии в растениях . Он имеет структуру, похожую на амилопектин (компонент крахмала), но более разветвлен и компактен, чем крахмал. Оба представляют собой белые порошки в сухом состоянии. Гликоген содержится в форме гранул в цитозоле /цитоплазме многих типов клеток и играет важную роль в цикле глюкозы . Гликоген образует энергетический резерв, который можно быстро мобилизовать для удовлетворения внезапной потребности в глюкозе, но он менее компактен, чем энергетические запасы триглицеридов ( липидов ). Как таковой он также встречается в качестве резерва хранения у многих паразитических простейших. [17] [18] [19]
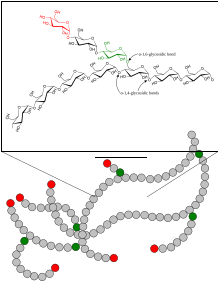
Гликоген — разветвленный биополимер , состоящий из линейных цепочек остатков глюкозы со средней длиной цепи примерно 8–12 единиц глюкозы и 2000–60 000 остатков на одну молекулу гликогена. [20] [21]
Как и амилопектин, единицы глюкозы связаны между собой линейно гликозидными связями α(1→4) от одной глюкозы к другой. Ветви связаны с цепями, от которых они отходят, гликозидными связями α(1→6) между первой глюкозой новой ветви и глюкозой в стволовой цепи. [22]
Каждый гликоген, по сути, представляет собой клубок глюкозных деревьев, примерно с 12 слоями, в центре которого находится белок гликогенин , с тремя видами цепей глюкозы: A, B и C. К гликогенину прикреплена только одна C-цепь. Эта С-цепь образуется в результате самоглюкозилирования гликогенина, образуя короткую цепь праймера. Из С-цепи вырастают В-цепи, а из В-цепей разветвляются В- и А-цепи. В-цепи имеют в среднем 2 точки ветвления, тогда как А-цепи являются терминальными и, следовательно, неразветвленными. В среднем каждая цепь имеет длину 12, строго ограниченную от 11 до 15. Все А-цепи достигают сферической поверхности гликогена. [23] [24]
Гликоген в мышцах, печени и жировых клетках хранится в гидратированной форме, состоящей из трех или четырех частей воды на часть гликогена, связанных с 0,45 миллимоль (18 мг) калия на грамм гликогена. [5]
Глюкоза является осмотической молекулой и может оказывать глубокое воздействие на осмотическое давление в высоких концентрациях, что может привести к повреждению или гибели клеток, если она хранится в клетке без модификации. [3] Гликоген является неосмотической молекулой, поэтому его можно использовать в качестве раствора для хранения глюкозы в клетке без нарушения осмотического давления. [3]
Когда еда, содержащая углеводы или белок, съедается и переваривается , уровень глюкозы в крови повышается, а поджелудочная железа выделяет инсулин . Глюкоза крови из воротной вены поступает в клетки печени ( гепатоциты ). Инсулин действует на гепатоциты, стимулируя действие нескольких ферментов , включая гликогенсинтазу . Молекулы глюкозы добавляются к цепям гликогена до тех пор, пока инсулина и глюкозы остается в избытке. В этом постпрандиальном или «насыщенном» состоянии печень поглощает из крови больше глюкозы, чем высвобождает.
После того, как еда переварилась и уровень глюкозы начинает падать, секреция инсулина снижается, а синтез гликогена прекращается. Когда гликоген необходим для получения энергии , он расщепляется и снова превращается в глюкозу. Гликогенфосфорилаза является основным ферментом расщепления гликогена. В течение следующих 8–12 часов глюкоза, полученная из гликогена печени, является основным источником глюкозы в крови, используемой остальным телом в качестве топлива.
Глюкагон , еще один гормон, вырабатываемый поджелудочной железой, во многих отношениях служит контрсигналом инсулину. В ответ на уровень инсулина ниже нормы (когда уровень глюкозы в крови начинает падать ниже нормального диапазона) глюкагон секретируется в возрастающих количествах и стимулирует как гликогенолиз (распад гликогена), так и глюконеогенез (производство глюкозы из других источников). .

Мышечный гликоген, по-видимому, функционирует как резерв быстродоступной фосфорилированной глюкозы в форме глюкозо-1-фосфата для мышечных клеток. Гликоген, содержащийся в клетках скелетных мышц, находится преимущественно в форме β-частиц. [25] Другие клетки, которые содержат небольшие количества, также используют его локально. Поскольку в мышечных клетках отсутствует глюкозо-6-фосфатаза , которая необходима для передачи глюкозы в кровь, гликоген, который они хранят, доступен исключительно для внутреннего использования и не передается другим клеткам. В этом отличие от клеток печени, которые при необходимости легко расщепляют накопленный гликоген на глюкозу и отправляют его через кровоток в качестве топлива для других органов. [26]
Скелетным мышцам необходима АТФ (обеспечивает энергию) для сокращения и расслабления мышц, что известно как теория скользящих нитей . Скелетные мышцы преимущественно полагаются на гликогенолиз в течение первых нескольких минут при переходе от покоя к активности, а также во время высокоинтенсивной аэробной активности и любой анаэробной активности. [27] Во время анаэробной активности, такой как тяжелая атлетика и изометрические упражнения , фосфагенная система (АТФ-ПЦр) и мышечный гликоген являются единственными используемыми субстратами, поскольку они не требуют ни кислорода, ни кровотока. [27]
Различные биоэнергетические системы производят АТФ с разной скоростью, причем АТФ вырабатывается из мышечного гликогена гораздо быстрее, чем окисление жирных кислот. [28] Уровень интенсивности упражнений также определяет, сколько какого субстрата (топлива) используется для синтеза АТФ. Мышечный гликоген может поставлять гораздо больше субстрата для синтеза АТФ, чем глюкоза в крови. Во время упражнений максимальной интенсивности мышечный гликоген может обеспечивать 40 ммоль глюкозы на кг сырого веса в минуту [29] , тогда как глюкоза в крови может обеспечивать 4–5 ммоль. [30] [4] Из-за высокой скорости поступления и быстрого синтеза АТФ во время высокоинтенсивной аэробной активности (например, быстрой ходьбы, бега или бега) чем выше интенсивность тренировки, тем больше мышечная клетка производит АТФ из мышц. гликоген. [31] Такая зависимость от мышечного гликогена предназначена не только для обеспечения мышц достаточным количеством АТФ во время высокоинтенсивных упражнений, но и для поддержания гомеостаза глюкозы в крови (то есть для предотвращения гипогликемии из-за того, что мышцам необходимо извлечь гораздо больше глюкозы из мышц). крови, чем может обеспечить печень). [30] Дефицит мышечного гликогена приводит к мышечной усталости , известной как «удар о стену» или «бонк» (см. ниже об истощении гликогена) .
В 1999 году Мелендес и др. показали, что структура гликогена оптимальна в рамках конкретной модели метаболических ограничений. Более подробно, структура гликогена — это оптимальная конструкция, которая максимизирует функцию приспособленности, основанную на максимизации трех величин: количества единиц глюкозы на поверхности цепи, доступных для ферментативного расщепления, количества мест связывания, к которым могут прикрепиться расщепляющие ферменты, общее количество сохраненных единиц глюкозы; и минимизация одного качества: общего объема.
Если каждая цепь имеет 0 или 1 точку ветвления, мы получаем по существу длинную цепь, а не сферу, и она будет занимать слишком большой объем, имея лишь несколько концевых единиц глюкозы для разложения. Если каждая цепь имеет три точки ветвления, гликоген будет заполняться слишком быстро. Точка равновесия равна 2.
Для этой ветви номер 2 длина цепи должна быть не менее 4. Согласно модели Мелендеса и др., функция приспособленности достигает максимума в точке 13, а затем медленно снижается.
Эмпирически число ветвей составляет 2, а длина цепи колеблется от 11 до 15 для большинства организмов, от позвоночных до бактерий и грибов. Единственным существенным исключением является устрица, длина гликогеновой цепи которой варьируется от 2 до 30, в среднем 7. [32] [33]
Гликоген был открыт Клодом Бернаром . Его эксперименты показали, что в печени содержится вещество, которое может привести к восстановлению сахара под действием «фермента» в печени. К 1857 году он описал выделение вещества, которое он назвал « la matière гликоген », или «сахарообразующее вещество». Вскоре после открытия гликогена в печени А. Сансон обнаружил, что мышечная ткань также содержит гликоген. Эмпирическая формула гликогена ( C
6ЧАС
10О
5) n был основан Кекуле в 1858 году. [34]
Синтез гликогена, в отличие от его распада, эндергоничен — он требует затрат энергии. Энергия для синтеза гликогена поступает из уридинтрифосфата (УТФ), который реагирует с глюкозо-1-фосфатом , образуя УДФ-глюкозу , в реакции, катализируемой УТФ — глюкозо-1-фосфатуридилилтрансферазой . Гликоген синтезируется из мономеров УДФ-глюкозы первоначально белком гликогенином , имеющим два тирозиновых якоря на восстанавливающем конце гликогена, поскольку гликогенин является гомодимером. После того, как к остатку тирозина было добавлено около восьми молекул глюкозы, фермент гликогенсинтаза постепенно удлиняет гликогеновую цепь с помощью УДФ-глюкозы, добавляя α(1→4)-связанную глюкозу к невосстанавливающему концу гликогеновой цепи. [35]
Фермент разветвления гликогена катализирует перенос терминального фрагмента из шести или семи остатков глюкозы с невосстанавливающего конца на гидроксильную группу С-6 остатка глюкозы глубже внутрь молекулы гликогена. Фермент разветвления может действовать только на ветвь, имеющую по меньшей мере 11 остатков, и фермент может переносить ту же цепь глюкозы или соседние цепи глюкозы.
Гликоген отщепляется от невосстанавливающих концов цепи ферментом гликогенфосфорилазой с образованием мономеров глюкозо-1-фосфата:
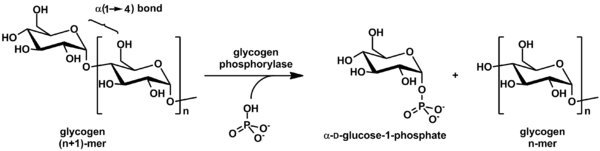
In vivo фосфоролиз протекает в направлении распада гликогена, поскольку соотношение фосфата и глюкозо-1-фосфата обычно превышает 100. [36] Глюкозо-1-фосфат затем превращается в глюкозо-6-фосфат (G6P) под действием фосфоглюкомутазы . Для удаления разветвлений α(1→6) в разветвленном гликогене и преобразования цепи в линейный полимер необходим специальный разветвляющий фермент . Произведенные мономеры G6P имеют три возможных судьбы:
Наиболее распространенным заболеванием, при котором метаболизм гликогена нарушается, является диабет , при котором из-за аномального количества инсулина гликоген в печени может аномально накапливаться или истощаться. Восстановление нормального метаболизма глюкозы обычно нормализует и метаболизм гликогена.
При гипогликемии , вызванной избытком инсулина, уровень гликогена в печени высок, но высокий уровень инсулина предотвращает гликогенолиз, необходимый для поддержания нормального уровня сахара в крови. Глюкагон является распространенным средством лечения этого типа гипогликемии.
Различные врожденные нарушения углеводного обмена вызваны недостатком ферментов или транспортных белков, необходимых для синтеза или распада гликогена. В совокупности они называются болезнями накопления гликогена .
Спортсмены на длинные дистанции, такие как марафонцы , лыжники и велосипедисты , часто испытывают истощение гликогена, когда почти все запасы гликогена у спортсменов истощаются после длительных периодов нагрузки без достаточного потребления углеводов. Это явление называется « ударом о стену » при беге и «стук» при езде на велосипеде.
Истощение гликогена можно предотвратить тремя возможными способами:
Когда спортсмены после изнурительных тренировок употребляют и углеводы, и кофеин , их запасы гликогена пополняются быстрее; [44] [45] однако минимальная доза кофеина, при которой наблюдается клинически значимое влияние на восполнение запасов гликогена, не установлена. [45]
Недавно наночастицы гликогена были исследованы как потенциальные системы доставки лекарств. [46]
В крови человека массой 70 кг циркулирует четыре грамма глюкозы. Эта глюкоза имеет решающее значение для нормального функционирования многих типов клеток. В соответствии с важностью этих 4 г глюкозы существует сложная система контроля для поддержания постоянного уровня глюкозы в крови. Наше внимание было сосредоточено на механизмах, с помощью которых регулируется поток глюкозы из печени в кровь и из крови в скелетные мышцы. ... Мозг потребляет ~60% глюкозы в крови человека, ведущего сидячий образ жизни и голодающего. ...Количество глюкозы в крови сохраняется за счет резервуаров гликогена (рис. 2). У людей после абсорбции около 100 г гликогена содержится в печени и около 400 г гликогена в мышцах. Окисление углеводов работающими мышцами может увеличиться примерно в 10 раз при физической нагрузке, но через 1
час
уровень глюкозы в крови поддерживается на уровне примерно 4 г.