Фермент лактоилглутатионлиаза (EC 4.4.1.5, также известный как глиоксалаза I ) катализирует изомеризацию гемитиоацетальных аддуктов , которые образуются в результате спонтанной реакции между глутатионильной группой и альдегидами , такими как метилглиоксаль . [1] [2]
Глиоксалаза I получила свое название от катализа первого шага в системе глиоксалаза , критической двухэтапной системе детоксикации метилглиоксаля . Метилглиоксаль вырабатывается естественным образом как побочный продукт нормальной биохимии, но он очень токсичен из-за его химических реакций с белками , нуклеиновыми кислотами и другими клеточными компонентами. Второй шаг детоксикации, на котором ( R )-S - лактоилглутатион расщепляется на глутатион и D-лактат, осуществляется глиоксалазой II , гидролазой . Необычно, что эти реакции, осуществляемые системой глиоксалаза, не окисляют глутатион, который обычно действует как окислительно-восстановительный кофермент . Хотя альдозоредуктаза также может детоксифицировать метилглиоксаль, система глиоксалаза более эффективна и, по-видимому, является наиболее важным из этих путей. Глиоксалаза I является привлекательной целью для разработки лекарств для лечения инфекций, вызванных некоторыми паразитическими простейшими, и рака . Было идентифицировано несколько ингибиторов глиоксалазы I, такие как S-(N-гидрокси-N-метилкарбамоил)глутатион.
Глиоксалаза I классифицируется как углерод-серная лиаза , хотя, строго говоря, фермент не образует и не разрывает связь углерод-сера. Вместо этого фермент смещает два атома водорода с одного атома углерода метилглиоксаля на соседний атом углерода. По сути, реакция является внутримолекулярной окислительно-восстановительной реакцией; один углерод окисляется, а другой восстанавливается. Механизм протекает путем вычитания и последующего добавления протонов , образуя промежуточное соединение энедиолят, а не путем переноса гидридов . Необычно для металлопротеина , что этот фермент проявляет активность с несколькими различными металлами. Глиоксалаза I также необычна тем, что она стереоспецифична во второй половине своего механизма, но не в первой половине. Структурно фермент представляет собой димер с обменом доменами у многих видов, хотя две субъединицы слились в мономер у дрожжей посредством дупликации гена .
Систематическое название этого класса ферментов — ( R ) -S -лактоилглутатионметилглиоксаль-лиаза (изомеризующая; глутатионобразующая); другие названия включают:
В некоторых случаях глутатионильная часть может поставляться трипанотионом , аналогом глутатиона у паразитических простейших, таких как трипаносомы . Человеческий ген этого фермента называется GLO1 .
Лактоилглутатионлиаза у людей кодируется геном GLO1 . [ 7] [8] [9]
Было решено несколько структур глиоксалазы I. Было опубликовано четыре структуры человеческой формы с кодами доступа PDB 1BH5, 1FRO, 1QIN и 1QIP. Было опубликовано пять структур формы Escherichia coli с кодами доступа 1FA5, 1FA6, 1FA7, 1FA8 и 1F9Z. Наконец, была решена одна структура трипанотион-специфической версии из Leishmania major , 2C21. Во всех этих случаях четвертичная структура биологической единицы представляет собой димер с обменом доменами, в котором активный центр и вторичная структура 8-цепочечного бета-слоя образованы из обеих субъединиц. Однако у дрожжей , таких как Saccharomyces cerevisiae , две субъединицы слились в один мономер двойного размера посредством дупликации гена . Каждая половина структурного димера представляет собой сэндвич из 3-4 альфа-спиралей по обе стороны 8-цепочечного антипараллельного бета-слоя; интерфейс димера в основном состоит из встречи лицом к лицу двух бета-слоев. [1]
Третичная и четвертичная структуры глиоксалазы I похожи на структуры нескольких других типов белков. Например, глиоксалаза I напоминает несколько белков, которые позволяют бактериям противостоять антибиотикам, таким как фосфомицин , блеомицин и митомицин . Аналогично, неродственные ферменты метилмалонил-КоА-эпимераза , 3-деметилубихинон-9 3-O-метилтрансфераза и многочисленные диоксигеназы, такие как бифенил-2,3-диол 1,2-диоксигеназа , катехол 2,3-диоксигеназа , 3,4-дигидроксифенилацетат 2,3-диоксигеназа и 4-гидроксифенилпируват диоксигеназа, все напоминают глиоксалазу I по структуре. [1] Наконец, многие белки с неизвестной или неопределенной функцией также напоминают глиоксалазу I, например, At5g48480 из растения Arabidopsis thaliana .
Активный участок состоит из четырех основных областей.
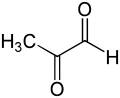
Основная физиологическая функция глиоксалазы I — детоксикация метилглиоксаля , реактивного 2-оксоальдегида , который является цитостатическим при низких концентрациях [10] и цитотоксичным при миллимолярных концентрациях. [11] Метилглиоксаль — побочный продукт нормальной биохимии, который является канцерогеном, мутагеном [12] и может химически повреждать несколько компонентов клетки, таких как белки и нуклеиновые кислоты. [11] [13] Метилглиоксаль образуется спонтанно из дигидроксиацетонфосфата ферментативно триозофосфатизомеразой и метилглиоксальсинтазой, а также при катаболизме треонина . [ 14]
Чтобы минимизировать количество токсичного метилглиоксаля и других реактивных 2-оксоальдегидов, развилась система глиоксалаза . Метилглиоксаль спонтанно реагирует с восстановленным глутатионом (или его эквивалентом, трипанотионом ), [15] ), образуя гемитиоацеталь. Система глиоксалаза преобразует такие соединения в D- лактат и восстанавливает глутатион. [14] В этом преобразовании два карбонильных углерода 2-оксоальдегида окисляются и восстанавливаются соответственно, альдегид окисляется до карбоновой кислоты, а ацетальная группа восстанавливается до спирта. Система глиоксалаза развилась очень рано в истории жизни и встречается почти повсеместно в формах жизни.
Система глиоксалаза состоит из двух ферментов, глиоксалаза I и глиоксалаза II . Первый фермент, описанный здесь, перестраивает гемитиоацеталь, образованный естественным путем при атаке глутатиона на метилглиоксаль, в продукт. Глиоксалаза II гидролизует продукт, чтобы повторно сформировать глутатион и произвести D- лактат . Таким образом, глутатион действует необычно как кофермент и требуется только в каталитических (т. е. очень малых) количествах; обычно глутатион действует вместо этого как окислительно-восстановительная пара в окислительно-восстановительных реакциях.
Предполагается, что система глиоксалазы также играет роль в регуляции роста клеток [16] и в сборке микротрубочек [17] .
Глиоксалаза I требует связанных ионов металла для катализа. [18] Человеческий фермент [19] и его аналоги в дрожжах ( Saccharomyces cerevisiae ) [20] и Pseudomonas putida [21] используют двухвалентный цинк , Zn 2+ . Напротив, прокариотические версии часто используют ион никеля . Глиоксалаза I, обнаруженная в эукариотических трипаносомных паразитах, таких как Leishmania major и Trypanosoma cruzi, также может использовать никель для своей активности, [15] возможно, отражая приобретение ими гена GLO1 путем горизонтального переноса генов . [22]
Свойством глиоксалазы I является отсутствие специфичности к каталитическому иону металла. Большинство ферментов связывают один конкретный тип металла, и их каталитическая активность зависит от связывания этого металла. Например, оксидоредуктазы часто используют определенный ион металла, такой как железо , марганец или медь , и не будут функционировать, если их предпочтительный ион металла будет заменен из-за различий в окислительно-восстановительном потенциале ; таким образом, супероксиддисмутаза железа не может функционировать, если ее каталитическое железо будет заменено марганцем, и наоборот. Напротив, хотя человеческая глиоксалаза I предпочитает использовать двухвалентный цинк, она способна функционировать со многими другими двухвалентными металлами, включая магний , марганец , кобальт , никель и даже кальций .; [23] Однако фермент неактивен с катионом железа. [24] Аналогично, хотя прокариотическая глиоксалаза I предпочитает никель, она способна функционировать с кобальтом, марганцем и кадмием ; однако фермент инертен со связанным цинком из-за изменения геометрии координации с октаэдрической на тригонально-бипирамидальную . [15] Структурные и вычислительные исследования показали, что металл связывает два карбонильных кислорода метилглиоксалевого фрагмента в двух его координационных участках, стабилизируя промежуточный энедиолатный анион.
Другим необычным свойством глиоксалазы I является ее непоследовательная стереоспецифичность. Первый шаг ее реакционного механизма (отрыв протона от C 1 и последующее протонирование O 2 ) не является стереоспецифичным и работает одинаково хорошо независимо от начальной хиральности при C 1 в полутиоацетальном субстрате. Полученный промежуточный энедиолят является ахиральным, но второй шаг реакционного механизма (отрыв протона от O 1 и последующее протонирование C 2 ) определенно стереоспецифичен, производя только ( S )-форму D-лактоилглутатиона. Считается, что это происходит из-за двух глутаматов, связанных противоположно на ионе металла; любой из них способен выполнить первый шаг, но только один способен выполнить второй шаг. Причина этой асимметрии еще полностью не определена.
Молекула метилглиоксаля состоит из двух карбонильных групп, фланкированных атомом водорода и метильной группой. В обсуждении ниже эти два карбонильных углерода будут обозначены как C1 и C2 соответственно. Как в субстрате гемитиоацеталя, так и в продукте (R)-S-лактоилглутатиона фрагмент глутатиона связан с карбонильной группой C1.
Основной механизм глиоксалазы I заключается в следующем. Субстрат гемитиоацеталь образуется, когда молекула глутатиона — вероятно, в его реактивной тиолатной форме — атакует карбонил C1 метилглиоксаля или родственного соединения, делая этот углерод четырехвалентным. Эта реакция происходит спонтанно в клетке, без участия фермента. Затем этот гемитиоацеталь связывается ферментом, который сдвигает водород из C1 в C2. Карбонил C2 восстанавливается до четырехвалентной спиртовой формы путем добавления двух протонов, тогда как карбонил C1 восстанавливается путем потери водорода при сохранении его связи с фрагментом глутатиона.
Вычислительное исследование в сочетании с имеющимися экспериментальными данными предполагает следующий механизм атомного разрешения для глиоксалазы I. [25] В активном центре каталитический металл принимает октаэдрическую координационную геометрию и, в отсутствие субстрата, связывает две воды, два противоположных глутамата , гистидин и одну другую боковую цепь, обычно другой гистидин или глутаматы . Когда субстрат попадает в активный центр, две воды сбрасываются, и два карбонильных кислорода субстрата связываются непосредственно с ионом металла. Два противоположных глутамата добавляют и вычитают протоны из C1 и C2 и их соответствующие кислороды, O1 и O2. Первая половина реакции переносит протон из C1 в O2, тогда как вторая половина переносит протон из O1 в C2. Первая реакция может быть осуществлена любым из противоположных глутаматов, в зависимости от начальной хиральности C1 в полутиоацетальном субстрате; Однако вторая половина является стереоспецифической и осуществляется только одним из противостоящих глутаматов.
Стоит отметить, что первый теоретически подтвержденный механизм для R -субстрата глиоксалазы был опубликован недавно. [26]
Каталитический механизм глиоксалазы был изучен с помощью теории функционала плотности, моделирования молекулярной динамики и гибридных методов QM/MM. Причиной особой специфичности фермента (он принимает оба энантиомера своего хирального субстрата, но преобразует их в один и тот же энантиомер продукта) является более высокая основность и гибкость одного из глутаматов активного центра (Glu172). [27] [28] [29]
Первоначально считалось, что глиоксалаза I действует путем переноса гидрида , который представляет собой протон, окруженный двумя электронами (H – ). [30] В этом, как считалось, она напоминает классический механизм реакции Канниццаро , в котором атака гидроксилата на альдегид превращает его в четырехвалентный спиртовой анион; этот анион отдает свои водороды второму альдегиду, образуя карбоновую кислоту и спирт. (По сути, два идентичных альдегида восстанавливают и окисляют друг друга, оставляя чистую степень окисления одинаковой.)
В глиоксалазе I такой механизм переноса гидрида будет работать следующим образом. Атака глутатиона оставит заряженный O – и водород альдегида, связанный с C 1 . Если карбонильный кислород C 2 может захватить водород из услужливой кислотной боковой цепи фермента, образуя спирт, то водород C 1 может одновременно соскользнуть со своими электронами на C 2 (перенос гидрида). В то же время, дополнительный электрон на кислороде C 1 может преобразовать двойную связь карбонила, таким образом давая конечный продукт.
Альтернативный (и в конечном итоге правильный) механизм с использованием переноса протона (H + ) был предложен в 1970-х годах. [31] В этом механизме основная боковая цепь фермента отщепляет протон альдегида от C 1 ; в то же время протон a присоединяется к кислороду C 2 , образуя таким образом энедиол . Эн означает, что между C 2 и C 1 образовалась двойная связь из электронов, оставшихся после отщепления протона альдегида; диол относится к тому факту, что из исходных двух карбонильных групп образовались два спирта. В этом механизме промежуточное соединение образует продукт путем добавления еще одного протона к C 2 .
Ожидалось, что протоны растворителя будут способствовать образованию продукта из промежуточного продукта ендиола механизма переноса протона, и когда такие вклады не наблюдались в тритированной воде, 3 H 1 O, предпочтение отдавалось механизму переноса гидрида. Однако альтернативная гипотеза — что активный центр фермента глубоко скрыт от воды — не могла быть исключена и в конечном итоге оказалась верной. Первые указания появились, когда постоянно растущие температуры показали постоянно увеличивающееся включение трития, что согласуется с переносом протона и неожиданно при переносе гидрида. Окончательное доказательство может быть получено с исследованиями эффекта изотопа водорода-дейтерия на субстратах, фторированных по метильной группе и дейтерированных по альдегиду. Фторид является хорошей уходящей группой; механизм переноса гидрида предсказывает меньшее устранение ионов фтора с дейтерированным образцом, тогда как механизм переноса протона предсказывает большее . Эксперименты с тремя типами глиоксалазы I (дрожжевой, крысиной и мышиной формами) подтвердили механизм переноса протонов в каждом случае. [32] Этот механизм был в конечном итоге обнаружен в кристаллических структурах глиоксалазы I.
Экспрессия Glo1 коррелирует с различиями в поведении, подобном тревожности, у мышей [33] [34], а также с поведением в тесте подвешивания за хвост , который чувствителен к антидепрессантам ; [35] однако, направление этих эффектов не всегда было последовательным, что вызвало скептицизм. [36] Различия в экспрессии Glo1 у мышей, по-видимому, вызваны вариантом числа копий , который распространен среди инбредных линий мышей. [37] Было высказано предположение, что поведенческие эффекты Glo1 обусловлены активностью его основного субстрата метилглиоксаля на рецепторах ГАМК А. [38] Было показано, что ингибитор глиоксалазы I, представляющий собой небольшую молекулу , обладает анксиолитическими свойствами, что определяет еще одно возможное показание для ингибиторов глиоксалазы I. [38]
Глиоксалаза I является целью для разработки фармацевтических препаратов против бактерий, простейших (особенно Trypanosoma cruzi и Leishmania ) и рака человека. [39] Было разработано множество ингибиторов, большинство из которых разделяют фрагмент глутатиона . Среди наиболее прочно связывающихся с человеческим ферментом ингибиторов есть производные S -( N -арил- N -гидроксикарбамоил)глутатиона, в частности производное p -бромфенила, имеющее константу диссоциации 14 нМ. [40] Считается, что ближайшим аналогом переходного состояния является S -( N -гидрокси- N -p -иодфенилкарбамоил)глутатион; кристаллическая структура этого соединения , связанного с человеческим ферментом, была решена с разрешением 2 Å (код доступа PDB 1QIN). [41]
Эксперименты показывают, что метилглиоксаль преимущественно токсичен для пролиферирующих клеток, таких как раковые. [42]
Недавние исследования показывают, что экспрессия GLO1 повышается в различных злокачественных опухолях человека, включая метастатическую меланому. [43] [44]