Дистилляция , или классическая дистилляция, — это процесс отделения компонентов или веществ от жидкой смеси с помощью селективного кипячения и конденсации , обычно внутри аппарата, известного как перегонный куб . Сухая перегонка — это нагревание твердых материалов с получением газообразных продуктов (которые могут конденсироваться в жидкости или твердые вещества); это может включать химические изменения, такие как деструктивная перегонка или крекинг . Дистилляция может привести к практически полному разделению (что приводит к почти чистым компонентам) или к частичному разделению, которое увеличивает концентрацию выбранных компонентов; в любом случае в этом процессе используются различия в относительной летучести компонентов смеси. В промышленности дистилляция представляет собой единичную операцию практически универсального значения, но представляет собой процесс физического разделения, а не химическую реакцию . Установка, используемая для перегонки, особенно дистиллированных напитков , представляет собой винокуренный завод. Дистилляция включает в себя следующие применения:

Ранние свидетельства дистилляции были обнаружены на аккадских табличках, датированных ок. 1200 г. до н.э. , описание парфюмерной деятельности. Таблички предоставили текстовое свидетельство того, что ранняя, примитивная форма дистилляции была известна вавилонянам древней Месопотамии . [8]
Аристотель знал, что вода, конденсирующаяся в результате испарения морской воды, является пресной: [9]
Я доказал опытным путем, что испаряющаяся соленая вода образует пресную, и пар, конденсируясь, не конденсируется снова в морскую воду.
- Аристотель, Метеорология, Книга II, Глава III.
Позволить морской воде испаряться и конденсироваться в пресную воду — это не дистилляция, поскольку дистилляция предполагает кипячение, но эксперимент мог стать важным шагом на пути к дистилляции. [10]
Дистилляция практиковалась на древнем Индийском субконтиненте , о чем свидетельствуют реторты и приемники из обожженной глины, найденные в Таксиле , Шайхан-Дхери и Чарсадде в Пакистане и Ранг-Махале в Индии , относящиеся к первым векам нашей эры . [11] [12] [13] Фрэнк Рэймонд Олчин говорит, что эти терракотовые дистилляционные трубки были «сделаны, чтобы имитировать бамбук». [14] Эти « перегонные кубы Гандхары » были способны производить только очень слабые спиртные напитки , поскольку не было эффективных средств сбора паров при слабом нагревании. [15]
Дистилляция в Китае, возможно, началась во времена династии Восточная Хань (I–II века н.э.).
Ранние свидетельства дистилляции были обнаружены у алхимиков , работавших в Александрии в Римском Египте в I веке нашей эры. [16] : 57, 89
Дистиллированная вода используется, по крайней мере, c. 200 г. н. э. , когда Александр Афродисийский описал этот процесс. [17] [18] Работы по перегонке других жидкостей продолжались в раннем византийском Египте при Зосиме Панопольском в 3 веке.
Средневековые мусульманские химики, такие как Джабир ибн Хайян (лат. Гебер, девятый век) и Абу Бакр ар-Рази (лат. Разес, ок. 865–925 ) широко экспериментировали с перегонкой различных веществ.
Дистилляция вина засвидетельствована в арабских работах, приписываемых аль-Кинди ( ок. 801–873 гг. Н. Э. ) и аль-Фараби ( ок. 872–950 ), а также в 28-й книге аз-Захрави (лат. Abulcasis). , 936–1013) Китаб ат-Тасриф (позже переведенный на латынь как Liber servatoris ). [19] В двенадцатом веке рецепты производства aqua ardens («горящей воды», т. е. этанола) путем перегонки вина с солью стали появляться в ряде латинских работ, а к концу тринадцатого века они были стали широко известным веществом среди западноевропейских химиков. [20] В работах Таддео Альдеротти (1223–1296) описан метод концентрирования спирта, включающий повторную перегонку через перегонный куб с водяным охлаждением, с помощью которого можно было получить спирт чистотой 90%. [21]
Фракционная перегонка органических веществ играет важную роль в работах, приписываемых Джабиру, таких как « Китаб ас-Сабин» («Книга семидесяти»), переведенная на латынь Герардом Кремонским ( ок. 1114–1187 ) под название Liber de septuaginta . [22] Эксперименты Джабира с фракционной перегонкой животных и растительных веществ, а также, в меньшей степени, минеральных веществ, являются основной темой De anima in arte alkimiae , первоначально арабского труда, ошибочно приписываемого Авиценне и переведенного на латынь. и впоследствии стал самым важным алхимическим источником для Роджера Бэкона ( ок. 1220–1292 ). [23]
Согласно археологическим данным, дистилляция напитков началась во времена династий Южная Сун (10–13 века) и Цзинь (12–13 века). [24] На археологическом участке в Цинлуне, провинция Хэбэй , Китай, был найден перегонный куб, датируемый XII веком. Дистиллированные напитки были распространены во времена династии Юань (13–14 века). [24]
В 1500 году немецкий алхимик Иероним Бруншвиг опубликовал Liber de arte distillandi de simplicibus ( «Книга искусства дистилляции из простых ингредиентов »), [25] первую книгу, посвященную исключительно теме дистилляции, за которой в 1512 году последовала значительно расширенная версия. . В 1651 году Джон Френч опубликовал «Искусство дистилляции» , [26] первый крупный английский сборник по этой практике, но утверждалось, [27] что большая часть его заимствована из работы Брауншвейга. Сюда входят диаграммы с людьми на них, показывающие промышленный, а не лабораторный масштаб операции.


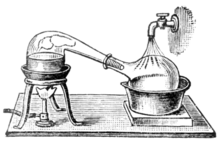


Когда алхимия превратилась в химическую науку , для дистилляции стали использоваться сосуды, называемые ретортами . И перегонные кубы , и реторты представляют собой стеклянную посуду с длинными горлышками , направленными в сторону под углом вниз, которые действуют как конденсаторы с воздушным охлаждением , конденсируя дистиллят и позволяя ему капать вниз для сбора. Позже были изобретены медные перегонные кубы. Клепаные соединения часто сохраняли герметичностью с помощью различных смесей, например теста из ржаной муки. [28] Эти перегонные кубы часто имели систему охлаждения вокруг клюва, например, с использованием холодной воды, что делало конденсацию спирта более эффективной. Их называли перегонными кубами . Сегодня в большинстве промышленных процессов реторты и перегонные кубы в значительной степени вытеснены более эффективными методами дистилляции. Тем не менее, перегонный куб до сих пор широко используется для производства некоторых прекрасных спиртных напитков, таких как коньяк , шотландский виски , ирландский виски , текила , ром , кашаса и некоторые виды водки . Перегонные кубы из различных материалов (дерева, глины, нержавеющей стали) также используются бутлегерами в разных странах. Также продаются небольшие перегонные кубы для использования в домашнем производстве [29] цветочной воды или эфирных масел .
Ранние формы дистилляции включали периодические процессы с использованием одного испарения и одной конденсации. Чистоту повышали дальнейшей перегонкой конденсата. Большие объемы обрабатывались простым повторением перегонки. Сообщается, что химики провели от 500 до 600 перегонок, чтобы получить чистое соединение. [30]
В начале 19 века были разработаны основы современных технологий, включая предварительный нагрев и кипячение . [30] В 1822 году Энтони Перье разработал один из первых перегонных аппаратов непрерывного действия, а затем, в 1826 году, Роберт Стейн усовершенствовал эту конструкцию и получил патент на перегонный аппарат . В 1830 году Эней Коффи получил патент на дальнейшее усовершенствование конструкции. [31] Непрерывный перегонный аппарат Коффи можно рассматривать как архетип современных нефтехимических установок. Французский инженер Арман Саваль разработал свой паровой регулятор примерно в 1846 году . масла и духи.
С появлением химической инженерии как дисциплины в конце XIX века стали применяться научные, а не эмпирические методы. Развивающаяся нефтяная промышленность в начале 20-го века дала толчок к развитию точных методов проектирования, таких как метод Маккейба-Тиле Эрнеста Тиле и уравнение Фенске . Первый промышленный завод в Соединенных Штатах, использующий дистилляцию как средство опреснения океана, открылся во Фрипорте, штат Техас, в 1961 году с надеждой обеспечить водную безопасность в регионе. [33] Наличие мощных компьютеров позволило проводить прямое компьютерное моделирование дистилляционных колонн.
Применение дистилляции можно условно разделить на четыре группы: лабораторный масштаб, промышленная дистилляция, дистилляция трав для парфюмерии и лекарств ( травяной дистиллят ) и пищевая промышленность. Последние два существенно отличаются от первых двух тем, что дистилляция используется не как настоящий метод очистки, а скорее для переноса всех летучих веществ из исходных материалов в дистиллят при обработке напитков и трав.
Основное различие между дистилляцией в лабораторном масштабе и промышленной дистилляцией заключается в том, что дистилляция в лабораторном масштабе часто выполняется периодически, тогда как промышленная дистилляция часто происходит непрерывно. При периодической перегонке в ходе перегонки изменяются состав исходного материала, паров перегоняемых соединений и дистиллята. При периодической перегонке в куб загружают (поставляют) порцию сырьевой смеси, которую затем разделяют на составляющие ее фракции, которые собираются последовательно от наиболее летучих к менее летучим, при этом кубовый остаток - оставшаяся наименее или нелетучая фракция - удалил в конце. Затем куб можно перезарядить и процесс повторить.
При непрерывной дистилляции исходные материалы, пары и дистиллят поддерживаются в постоянном составе за счет тщательного пополнения исходного материала и удаления фракций как из пара, так и из жидкости в системе. Это приводит к более детальному контролю процесса разделения.
Точка кипения жидкости — это температура, при которой давление пара жидкости равно давлению вокруг жидкости, что позволяет пузырькам образовываться без разрушения. Особым случаем является нормальная температура кипения , при которой давление пара жидкости равно атмосферному давлению окружающей среды .
Это заблуждение, что в жидкой смеси при данном давлении каждый компонент кипит при температуре кипения, соответствующей данному давлению, позволяя парам каждого компонента собираться отдельно и в чистоте. Однако этого не происходит даже в идеализированной системе. Идеализированные модели дистилляции по существу подчиняются законам Рауля и закона Дальтона и предполагают, что достигается равновесие пар-жидкость .
Закон Рауля гласит, что давление пара раствора зависит от 1) давления пара каждого химического компонента в растворе и 2) доли раствора, которую составляет каждый компонент, то есть мольной доли . Этот закон применяется к идеальным растворам или растворам, которые имеют разные компоненты, но молекулярные взаимодействия которых такие же или очень похожи на чистые растворы.
Закон Дальтона гласит, что общее давление представляет собой сумму парциальных давлений каждого отдельного компонента смеси. Когда многокомпонентная жидкость нагревается, давление пара каждого компонента повышается, что приводит к увеличению общего давления пара. Когда общее давление паров достигает давления, окружающего жидкость, происходит кипение , и жидкость превращается в газ во всем объеме жидкости. Смесь заданного состава имеет одну температуру кипения при данном давлении, когда компоненты взаимно растворимы. Смесь постоянного состава не имеет кратных температур кипения.
Следствием одной точки кипения является то, что более легкие компоненты никогда не «закипают» полностью. При температуре кипения все летучие компоненты кипят, но для компонента его процентное содержание в паре такое же, как и его процентное содержание в общем давлении пара. Более легкие компоненты имеют более высокое парциальное давление и, таким образом, концентрируются в паре, но более тяжелые летучие компоненты также имеют (меньшее) парциальное давление и обязательно также испаряются, хотя и с более низкой концентрацией в паре. Действительно, периодическая перегонка и фракционирование достигают успеха за счет изменения состава смеси. При периодической перегонке шихта испаряется, что изменяет ее состав; при фракционировании жидкость, находящаяся выше в ректификационной колонне, содержит больше легких веществ и кипит при более низких температурах. Поэтому, исходя из данной смеси, она оказывается не температурой кипения, а интервалом кипения, хотя это происходит потому, что меняется ее состав: каждая промежуточная смесь имеет свою, особую температуру кипения.
Идеализированная модель точна в случае химически подобных жидкостей, таких как бензол и толуол . В других случаях наблюдаются серьезные отклонения от закона Рауля и закона Дальтона, особенно в смеси этанола и воды. Эти соединения при совместном нагревании образуют азеотроп , то есть паровая фаза и жидкая фаза содержат один и тот же состав. Хотя существуют вычислительные методы , которые можно использовать для оценки поведения смеси произвольных компонентов, единственный способ получить точные данные о равновесии пар-жидкость — это измерения.
Невозможно полностью очистить смесь компонентов перегонкой, так как для этого потребуется, чтобы каждый компонент смеси имел нулевое парциальное давление . Если целью является получение сверхчистых продуктов, необходимо применять дальнейшее химическое разделение . Когда бинарная смесь испаряется, а другой компонент, например соль, имеет для практических целей нулевое парциальное давление, процесс упрощается.
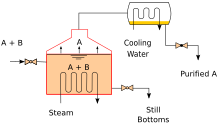
Нагревание идеальной смеси двух летучих веществ, А и В, причем А имеет более высокую летучесть или более низкую температуру кипения, в установке периодической дистилляции (например, в аппарате, изображенном на первом рисунке) до тех пор, пока смесь не закипит, приводит к пар над жидкостью, содержащей смесь A и B. Соотношение между A и B в паре будет отличаться от соотношения в жидкости. Соотношение в жидкости будет определяться тем, как была приготовлена исходная смесь, тогда как соотношение в паре будет обогащено более летучим соединением А (в соответствии с законом Рауля, см. выше). Пар проходит через конденсатор и удаляется из системы. Это, в свою очередь, означает, что соотношение соединений в оставшейся жидкости теперь отличается от исходного (т.е. более обогащено B, чем в исходной жидкости).
В результате соотношение в жидкой смеси меняется, становясь богаче компонентом B. Это приводит к повышению температуры кипения смеси, что приводит к повышению температуры в паре, что приводит к изменению соотношения A. : B в газовой фазе (по мере продолжения дистилляции доля B в газовой фазе увеличивается). Это приводит к медленно меняющемуся соотношению A:B в дистилляте.
Если разница в давлении паров между двумя компонентами A и B велика (обычно выражается как разница в температурах кипения), смесь в начале перегонки сильно обогащается компонентом A, а когда компонент A отгоняется, кипение жидкость обогащена компонентом Б.
Непрерывная дистилляция — это непрерывная дистилляция, при которой жидкая смесь непрерывно (без перерывов) подается в процесс, а отделенные фракции непрерывно удаляются по мере появления выходных потоков во время работы. Непрерывная перегонка дает минимум две выходные фракции, включая по меньшей мере одну летучую фракцию дистиллята, которая кипела и отдельно улавливалась в виде пара, а затем конденсировалась в жидкость. Всегда существует кубовая фракция (или остаток), представляющая собой наименее летучий остаток, который не улавливается отдельно в виде конденсированного пара.
Непрерывная дистилляция отличается от периодической дистилляции тем, что концентрации не должны меняться с течением времени. Непрерывную дистилляцию можно проводить в установившемся режиме в течение произвольного периода времени. Для любого исходного материала определенного состава основными переменными, влияющими на чистоту продуктов при непрерывной перегонке, являются флегмовое число и количество теоретических стадий равновесия, на практике определяемое количеством тарелок или высотой насадки. Рефлюкс — это поток из конденсатора обратно в колонну, который создает рециркуляцию, обеспечивающую лучшее разделение при заданном количестве тарелок. Стадии равновесия являются идеальными этапами, на которых композиции достигают равновесия пар-жидкость, повторяя процесс разделения и обеспечивая лучшее разделение с учетом флегмового числа. Колонна с высоким флегмовым числом может иметь меньше ступеней, но в ней циркулирует большое количество жидкости, что дает широкую колонну с большой задержкой. И наоборот, колонна с низким флегмовым числом должна иметь большое количество ступеней, поэтому требуется более высокая колонна.
Как периодическую, так и непрерывную дистилляцию можно улучшить, установив ректификационную колонну поверх перегонной колбы. Колонна улучшает разделение, обеспечивая большую площадь поверхности для контакта пара и конденсата. Это помогает ему оставаться в равновесии как можно дольше. Колонна может даже состоять из небольших подсистем («подносов» или «тарелок»), каждая из которых содержит обогащенную кипящую жидкую смесь со своим собственным парожидкостным равновесием.
Существуют различия между фракционирующими колоннами лабораторного и промышленного масштаба, но принципы одинаковы. Примеры фракционирующих колонн лабораторного масштаба (с повышением эффективности) включают:
Дистилляция в лабораторном масштабе почти всегда проводится периодической дистилляцией. Устройство, используемое при перегонке, иногда называемое перегонным аппаратом , состоит как минимум из ребойлера или котла , в котором нагревается исходный материал, конденсатора, в котором нагретый пар охлаждается обратно до жидкого состояния , и приемника, в котором собирают концентрированную или очищенную жидкость, называемую дистиллятом. Существует несколько лабораторных методов дистилляции (см. также типы дистилляции ).
Полностью герметичный дистилляционный аппарат может испытывать сильное и быстро меняющееся внутреннее давление, что может привести к разрыву его соединений. Поэтому какой-то путь обычно оставляют открытым (например, в приемной колбе), чтобы внутреннее давление уравнялось с атмосферным давлением. В качестве альтернативы можно использовать вакуумный насос , чтобы поддерживать в аппарате давление ниже атмосферного. Если используемые вещества чувствительны к воздуху или влаге, соединение с атмосферой может быть осуществлено через одну или несколько сушильных трубок , заполненных материалами, которые удаляют нежелательные компоненты воздуха, или через барботеры , которые обеспечивают подвижный жидкостный барьер. Наконец, попадание нежелательных компонентов воздуха можно предотвратить, закачивая в аппарат небольшой, но постоянный поток подходящего инертного газа, такого как азот .
При простой перегонке пар сразу же направляется в конденсатор. Следовательно, дистиллят не является чистым, а его состав идентичен составу паров при данной температуре и давлении. Эта концентрация подчиняется закону Рауля .
В результате простая перегонка эффективна только тогда, когда температуры кипения жидкостей сильно различаются (практическое правило: 25 ° C) [34] или при отделении жидкостей от нелетучих твердых веществ или масел. В этих случаях давление пара компонентов обычно достаточно различно, чтобы дистиллят мог быть достаточно чистым для использования по назначению.
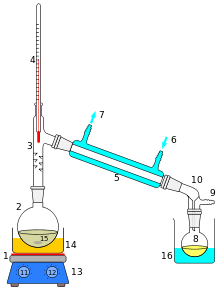
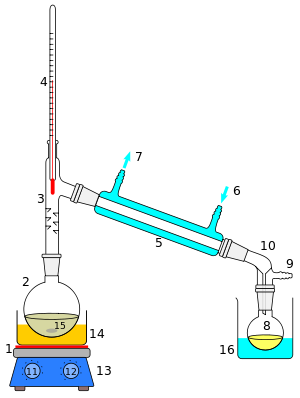
Схема простой операции дистилляции в разрезе показана справа. Исходная жидкость 15 в кипящей колбе 2 нагревается с помощью комбинированной плиты и магнитной мешалки 13 через баню с силиконовым маслом (оранжевая, 14). Пар проходит через короткую колонну Вигро 3, затем через конденсатор Либиха 5, охлаждается водой (синий цвет), циркулирующей через порты 6 и 7. Сконденсировавшаяся жидкость капает в приемную колбу 8, находящуюся в охлаждающей ванне (синий цвет, 16). Переходник 10 имеет соединение 9, которое можно подключить к вакуумному насосу. Компоненты соединены притертыми стеклянными соединениями .
Во многих случаях температуры кипения компонентов смеси будут достаточно близки, поэтому необходимо учитывать закон Рауля . Следовательно, для разделения компонентов посредством повторных циклов испарения-конденсации внутри насадочной ректификационной колонны необходимо использовать фракционную перегонку. Такое разделение путем последовательной перегонки также называется ректификацией. [35]
По мере нагревания очищаемого раствора его пары поднимаются в ректификационную колонну . Поднимаясь, он охлаждается, конденсируясь на стенках конденсатора и поверхностях насадочного материала. Здесь конденсат продолжает нагреваться поднимающимися горячими парами; он испаряется еще раз. Однако состав свежих паров снова определяется законом Рауля. Каждый цикл испарения-конденсации (называемый теоретической тарелкой ) дает более чистый раствор более летучего компонента. [36] В действительности, каждый цикл при данной температуре не происходит точно в одном и том же месте в ректификационной колонне; Таким образом, теоретическая тарелка представляет собой скорее концепцию, чем точное описание.
Большее количество теоретических тарелок приводит к лучшему разделению. В системе дистилляции с вращающейся лентой используется вращающаяся лента из тефлона или металла, чтобы обеспечить тесный контакт поднимающихся паров с нисходящим конденсатом, увеличивая количество теоретических тарелок. [37]
Как и вакуумная дистилляция , паровая дистилляция представляет собой метод перегонки термочувствительных соединений. [1] : 151–153 Температуру пара легче контролировать, чем поверхность нагревательного элемента , и он обеспечивает высокую скорость теплопередачи без нагрева при очень высокой температуре. Этот процесс включает в себя пропускание пара через нагретую смесь сырья. По закону Рауля часть целевого соединения испаряется (в соответствии с его парциальным давлением). Паровая смесь охлаждается и конденсируется, обычно образуя слой масла и слой воды.
Паровая дистилляция различных ароматических трав и цветов может дать два продукта: эфирное масло и водянистый травяной дистиллят . Эфирные масла часто используются в парфюмерии и ароматерапии , а водные дистилляты находят множество применений в ароматерапии , пищевой промышленности и уходе за кожей .


Некоторые соединения имеют очень высокие температуры кипения. Для кипячения таких соединений часто лучше понизить давление, при котором такие соединения кипятятся, вместо того, чтобы повышать температуру. Как только давление снизится до давления паров соединения (при данной температуре), может начаться кипение и остальная часть процесса дистилляции. Этот метод называется вакуумной дистилляцией и обычно используется в лаборатории в виде роторного испарителя .
Этот метод также очень полезен для соединений, температура кипения которых превышает температуру разложения при атмосферном давлении и которые, следовательно, будут разлагаться при любой попытке кипячения их при атмосферном давлении.
Молекулярная дистилляция — это вакуумная перегонка при давлении ниже 0,01 Торр . 0,01 торр — это на порядок выше высокого вакуума , где жидкости находятся в режиме свободномолекулярного потока , т. е. длина свободного пробега молекул сравнима с размером оборудования. Газовая фаза уже не оказывает существенного давления на испаряемое вещество и, следовательно, скорость испарения больше не зависит от давления. То есть, поскольку предположения о континууме гидродинамики больше не применяются, массоперенос регулируется молекулярной динамикой, а не динамикой жидкости. Таким образом, необходим короткий путь между горячей поверхностью и холодной поверхностью, обычно путем подвешивания горячей пластины, покрытой пленкой корма, рядом с холодной пластиной на прямой видимости между ними. Молекулярная дистилляция используется в промышленности для очистки масел.
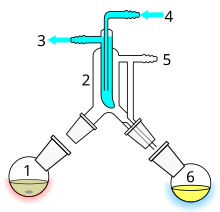
Дистилляция по короткому пути — это метод дистилляции, при котором дистиллят проходит небольшое расстояние, часто всего несколько сантиметров, и обычно проводится при пониженном давлении. [1] : 150 Классическим примером может быть дистилляция, при которой дистиллят перемещается из одной стеклянной колбы в другую без необходимости использования конденсатора, разделяющего две камеры. Этот метод часто используется для соединений, нестабильных при высоких температурах, или для очистки небольших количеств соединений. Преимущество состоит в том, что температура нагрева может быть значительно ниже (при пониженном давлении), чем точка кипения жидкости при стандартном давлении, и дистилляту нужно пройти лишь небольшое расстояние до конденсации. Короткий путь гарантирует, что по бокам устройства потеряется мало материала. Аппарат Кугельрора представляет собой разновидность метода дистилляции с коротким путем, который часто содержит несколько камер для сбора фракций дистиллята.
Некоторые соединения имеют высокие температуры кипения, а также чувствительны к воздуху . Можно использовать простую систему вакуумной дистилляции, приведенную выше, в которой вакуум заменяется инертным газом после завершения дистилляции. Однако это менее удовлетворительная система, если требуется собирать фракции при пониженном давлении. Для этого к концу конденсатора можно добавить переходник «корова» или «свинья», а для лучших результатов или для очень чувствительных к воздуху соединений можно использовать треугольный аппарат Перкина .
Треугольник Перкина имеет средства с помощью ряда стеклянных или тефлоновых кранов, позволяющие изолировать фракции от остальной части куба без удаления основной части дистилляции из вакуума или источника тепла и, таким образом, может оставаться в состоянии рефлюкса . _ Для этого образец сначала изолируют от вакуума с помощью кранов, затем вакуум над образцом заменяют инертным газом (например, азотом или аргоном ), после чего его можно закупорить и удалить. Затем в систему можно добавить свежий резервуар для сбора, откачать его и снова подключить к системе дистилляции через краны для сбора второй фракции и так далее, пока не будут собраны все фракции.
Зонная дистилляция — процесс дистилляции в длинной емкости с частичным плавлением очищенного вещества в движущейся жидкой зоне и конденсацией паров в твердой фазе при вытягивании конденсата в холодную зону. Этот процесс работает в теории. При движении зонального нагревателя сверху вниз по емкости образуется твердый конденсат с неравномерным распределением примесей. Тогда наиболее чистая часть конденсата может быть извлечена в качестве продукта. Процесс можно повторять многократно, перемещая (без оборота) полученный конденсат в нижнюю часть контейнера на место очищенного вещества. Неравномерность распределения примесей в конденсате (т.е. эффективность очистки) возрастает с увеличением количества итераций. Зонная перегонка является дистилляционным аналогом зонной перекристаллизации. Распределение примесей в конденсате описывается известными уравнениями зонной рекристаллизации – с заменой коэффициента распределения кристаллизации k на коэффициент разделения α перегонки. [38] [39] [40]
Неконденсирующийся газ может быть вытеснен из аппарата парами относительно летучего сорастворителя, который самопроизвольно испаряется при первоначальной откачке, и этого можно добиться с помощью обычного масляного или диафрагменного насоса. [41] [42]
Единичный процесс испарения можно также назвать «дистилляцией»:
Другое использование:
Взаимодействия между компонентами раствора создают уникальные свойства раствора, поскольку большинство процессов влекут за собой неидеальные смеси, в которых закон Рауля не выполняется. Такие взаимодействия могут привести к образованию азеотропа с постоянной температурой кипения , который ведет себя так, как если бы он был чистым соединением (т. е. кипит при одной температуре, а не в определенном диапазоне). В азеотропе раствор содержит данный компонент в той же пропорции, что и пар, поэтому выпаривание не изменяет чистоту, а перегонка не приводит к разделению. Например, 95,6% этанола (по массе) в воде образует азеотроп при 78,1 °C.
Если азеотроп не считается достаточно чистым для использования, существуют некоторые методы разрушения азеотропа с получением более чистого дистиллята. Эти методы известны как азеотропная дистилляция . Некоторые методы достигают этого путем «перепрыгивания» через азеотропную композицию (путем добавления другого компонента для создания нового азеотропа или изменения давления). Другие работают путем химического или физического удаления или изоляции примесей. Например, чтобы очистить этанол выше 95%, можно добавить осушитель (или осушитель , такой как карбонат калия ), чтобы превратить растворимую воду в нерастворимую кристаллизационную воду . Для этой цели часто используют молекулярные сита .
Несмешивающиеся жидкости, такие как вода и толуол , легко образуют азеотропы. Обычно эти азеотропы называют низкокипящими азеотропами, поскольку температура кипения азеотропа ниже, чем температура кипения любого чистого компонента. Температуру и состав азеотропа легко предсказать по давлению паров чистых компонентов без использования закона Рауля. Азеотроп легко разрушается в дистилляционной установке с помощью сепаратора жидкость-жидкость (декантатор) для разделения двух слоев жидкости, которые конденсируются наверху. Только один из двух слоев жидкости направляют в дистилляционную установку с обратным холодильником.
Также существуют высококипящие азеотропы, такие как 20-процентная по массе смесь соляной кислоты в воде. Как следует из названия, температура кипения азеотропа выше, чем температура кипения любого чистого компонента.
Точки кипения компонентов в азеотропе перекрываются, образуя полосу. Подвергая азеотроп воздействию вакуума или положительного давления, можно отклонить точку кипения одного компонента от другого, используя разные кривые давления пара каждого; кривые могут перекрываться в азеотропной точке, но вряд ли останутся идентичными дальше по оси давления по обе стороны от азеотропной точки. Когда смещение достаточно велико, две точки кипения больше не перекрываются, и поэтому азеотропная полоса исчезает.
Этот метод может устранить необходимость добавления других химикатов при перегонке, но у него есть два потенциальных недостатка.
При отрицательном давлении необходима мощность для источника вакуума, а пониженные температуры кипения дистиллятов требуют, чтобы конденсатор работал в более прохладном месте, чтобы предотвратить попадание паров дистиллята в источник вакуума. Повышенные требования к охлаждению часто требуют дополнительной энергии и, возможно, нового оборудования или замены охлаждающей жидкости.
В качестве альтернативы, если требуется положительное давление, нельзя использовать стандартную стеклянную посуду, необходимо использовать энергию для создания давления, и существует более высокая вероятность возникновения побочных реакций при дистилляции, таких как разложение, из-за более высоких температур, необходимых для кипения.
Однонаправленная дистилляция будет зависеть от изменения давления в одном направлении, положительном или отрицательном.
Дистилляция с переменным давлением по существу аналогична однонаправленной дистилляции, используемой для разрушения азеотропных смесей, но здесь можно использовать как положительное, так и отрицательное давление .
Это улучшает селективность дистилляции и позволяет химику оптимизировать дистилляцию, избегая экстремальных значений давления и температуры, приводящих к потере энергии. Это особенно важно в коммерческих приложениях.
Одним из примеров применения дистилляции под давлением является промышленная очистка этилацетата после его каталитического синтеза из этанола .

Крупномасштабные промышленные применения дистилляции включают как периодическую, так и непрерывную фракционную, вакуумную, азеотропную, экстрактивную и паровую дистилляцию. Наиболее широко промышленное применение непрерывной фракционной дистилляции в стационарном состоянии наблюдается на нефтеперерабатывающих заводах , нефтехимических и химических заводах и заводах по переработке природного газа .
Для контроля и оптимизации такой промышленной дистилляции разработан стандартизированный лабораторный метод ASTM D86. Этот метод испытаний распространяется на атмосферную перегонку нефтепродуктов с использованием лабораторной перегонной установки периодического действия для количественного определения характеристик диапазона кипения нефтепродуктов.
Промышленная дистилляция [35] [43] обычно проводится в больших вертикальных цилиндрических колоннах, известных как дистилляционные башни или дистилляционные колонны, с диаметром примерно от 0,65 до 16 метров (от 2 футов 2 дюйма до 52 футов 6 дюймов) и высотой примерно от 6 футов 6 дюймов. до 90 метров (от 20 до 295 футов) или более. Когда технологическое сырье имеет разнообразный состав, как при перегонке сырой нефти , выпуски жидкости через определенные промежутки вверх по колонне позволяют отводить разные фракции или продукты, имеющие разные точки кипения или диапазоны кипения. Самые «легкие» продукты (с самой низкой температурой кипения) выходят из верхней части колонны, а самые «тяжелые» продукты (с самой высокой температурой кипения) выходят из нижней части колонны и часто называются кубовыми отходами.
Промышленные башни используют рециркуляцию для достижения более полного разделения продуктов. Рефлюкс относится к части сконденсированного жидкого продукта из дистилляционной или ректификационной колонны, которая возвращается в верхнюю часть колонны, как показано на схематической диаграмме типичной крупномасштабной промышленной дистилляционной колонны. Внутри колонны нисходящая флегма обеспечивает охлаждение и конденсацию восходящих паров, тем самым повышая эффективность дистилляционной колонны. Чем больше рециркуляции обеспечивается для данного количества теоретических тарелок , тем лучше в башне отделяется низкокипящие материалы от более высококипящих материалов. Альтернативно, чем больше флегмы обеспечивают для данного желаемого разделения, тем меньшее количество теоретических тарелок требуется. Инженеры-химики должны выбрать, какое сочетание скорости флегмы и количества тарелок является экономически и физически целесообразным для продуктов, очищаемых в ректификационной колонне.
Такие промышленные ректификационные колонны также используются при криогенном разделении воздуха с получением жидкого кислорода , жидкого азота и аргона высокой чистоты . Дистилляция хлорсиланов также позволяет производить кремний высокой чистоты для использования в качестве полупроводников .
Конструкция и работа ректификационной колонны зависит от сырья и желаемых продуктов. Учитывая простую подачу бинарных компонентов, можно использовать аналитические методы, такие как метод МакКейба-Тиле [35] [44] или уравнение Фенске [35] . Для многокомпонентного корма имитационные модели используются как при проектировании, так и при эксплуатации. Более того, эффективность устройств для контакта пара и жидкости (называемых «тарелками» или «тарелями»), используемых в дистилляционных колоннах, обычно ниже, чем эффективность теоретической равновесной ступени со 100% эффективной эффективностью . Следовательно, для дистилляционной колонны требуется больше тарелок, чем количество теоретических стадий равновесия пара и жидкости. Для оценки эффективности лотков было предложено множество моделей.
В современных промышленных целях в колонне вместо тарелок используется насадочный материал, когда требуются низкие перепады давления в колонне. Другими факторами, благоприятствующими упаковке, являются: вакуумные системы, колонны меньшего диаметра, агрессивные системы, системы, склонные к пенообразованию, системы, требующие низкой задержки жидкости, и периодическая перегонка. И наоборот, факторами, благоприятствующими тарельчатым колоннам , являются: наличие твердых частиц в сырье, высокие скорости жидкости, большие диаметры колонн, сложные колонны, колонны с широким диапазоном состава сырья, колонны с химической реакцией, абсорбционные колонны, колонны, ограниченные допуском по весу фундамента, низкие скорость жидкости, большой диапазон регулирования и те процессы, которые подвержены скачкам процесса.
Этот набивочный материал может представлять собой случайную или разгруженную насадку (шириной 25–76 миллиметров (1–3 дюйма), например, кольца Рашига или структурированный листовой металл . Жидкости имеют тенденцию смачивать поверхность насадки, и пары проходят через эту смоченную поверхность, где происходит массоперенос . В отличие от традиционной тарельчатой дистилляции, в которой каждая тарелка представляет собой отдельную точку равновесия пар-жидкость, кривая равновесия пар-жидкость в насадочной колонне является непрерывной. Однако при моделировании насадочной колонны полезно рассчитать ряд «теоретических стадий», чтобы обозначить эффективность разделения насадочной колонны по сравнению с более традиционными тарелками. Упаковки разной формы имеют разную площадь поверхности и пустое пространство между упаковками. Оба эти фактора влияют на производительность упаковки.
Другим фактором, помимо формы и площади поверхности насадки, который влияет на характеристики случайной или структурированной насадки, является распределение жидкости и пара, попадающих в слой насадки. Количество теоретических стадий , необходимых для данного разделения, рассчитывается с использованием определенного соотношения пара и жидкости. Если жидкость и пар неравномерно распределены по поверхностной площади башни при входе в насадочный слой, соотношение жидкости и пара в насадочном слое будет неправильным и требуемое разделение не будет достигнуто. Кажется, что упаковка работает неправильно. Высота , эквивалентная теоретической пластине (HETP), будет больше ожидаемой. Проблема не в самой насадке, а в неправильном распределении жидкостей, попадающих в насадочный слой. Неправильное распределение жидкости чаще является проблемой, чем пар. Конструкция распределителей жидкости, используемых для подачи сырья и орошения в слой насадки, имеет решающее значение для обеспечения максимальной эффективности насадки. Методы оценки эффективности распределителя жидкости для равномерного распределения жидкости, поступающей в насадочный слой, можно найти в ссылках. [46] [47] Значительная работа была проделана по этой теме компанией Fractionation Research, Inc. (широко известной как FRI). [48]
Целью многокорпусной дистилляции является повышение энергоэффективности процесса для использования при опреснении или, в некоторых случаях, на одной стадии производства сверхчистой воды . Число эффектов обратно пропорционально количеству кВт·ч/м 3 восстановленной воды и относится к объему восстановленной воды на единицу энергии по сравнению с одноступенчатой дистилляцией. Один эффект составляет примерно 636 кВт·ч/м 3 :
Существует много других типов процессов многокорпусной дистилляции, в том числе процесс, называемый просто многокорпусной дистилляцией (MED), в котором используются несколько камер с промежуточными теплообменниками.
Растительные материалы, содержащие углеводы , подвергаются ферментации, при этом образуется разбавленный раствор этанола. Такие спиртные напитки, как виски и ром , получают путем перегонки разбавленных растворов этанола. В конденсате собираются другие компоненты, кроме этанола, включая воду, сложные эфиры и другие спирты, которые и определяют вкус напитка. Некоторые из этих напитков затем хранят в бочках или других контейнерах, чтобы они приобрели больше вкусовых соединений и характерных вкусов.
Как уже упоминалось, текстовые свидетельства шумеро-вавилонской дистилляции обнаружены в группе аккадских табличек с описанием парфюмерных операций, датированных ок. 1200 г. до н.э.
Самым ранним возможным периодом, по-видимому, является династия Восточная Хань... наиболее вероятный период начала настоящей дистилляции спиртных напитков для питья в Китае приходится на времена династий Цзинь и Южная Сун.