1,3-Дифосфа-2,4-диборетаны , или B 2 P 2 , представляют собой класс 4-членных циклических соединений чередующихся атомов бора и фосфора . Они часто встречаются в виде димеров при синтезе борафосфенов (RB=PR'). [1] Соединения могут проявлять локализованный синглетный бирадикальный характер (дирадикалоид) между атомами бора в растворе и твердом состоянии. [2]
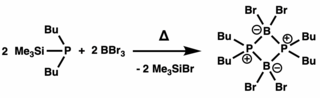
Первый предложенный синтез дифосфадиборетанового соединения был осуществлен с помощью димеризации фосфиноарилборанов в 1961 году. [3] Одновременно было установлено, что дифосфадиборетан образуется в результате реакции с фосфиносиланами и галогенидами бора. [4] [5] Последующая термолизная обработка образовала борафосфены путем расщепления связей σ P-Si. Димеризация этих соединений весьма благоприятна (до 90 ккал моль −1 ), что приводит к выделенным дифосфадиборетанам. [1] Также были обнаружены альтернативные пути синтеза с использованием легко уходящих групп , включая элиминирование галогенида водорода и органилфосфана для получения предшественников мономеров. Было также обнаружено, что обработка галогенидами бора с фосфидами лития приводит к мономерам, которые затем димеризуются в дифосфадиборетаны. [6]
В 2002 году был осуществлен прямой синтез дифосфадиборетандиила, производного дифосфадиборетана, с использованием 1,2-дихлордиборана и реагента фосфида лития. [2]

В 2021 году было обнаружено, что фосфинирование диборина с использованием дифосфата медленно приводит к образованию дифосфадиборетана в растворе. [7]


Дифосфадиборетаны могут быть выделены в виде отдельных кристаллов, пригодных для рентгеновской кристаллографии . [1] [5] [6] [7] Структура оказывается плоской с почти квадратной геометрией. Расстояние BB находится в диапазоне 2,57-2,71 Å, что указывает на длинную одинарную связь BB. Атомы фосфора принимают пирамидальную геометрию, которая предпочтительнее плоской геометрии и предотвращает π-связь с атомами бора. [2] [6]
Производные дифосфадиборетандиила имеют более широкий структурный диапазон, принимая планарную и бицикло[1.1.0] геометрию, аналогичную дифосфацилобутандиилам. [8] Эти геометрии можно модулировать, изменяя заместители на атомах бора или фосфора. Это преобразование сопровождается удлинением и укорочением связи BB, соответственно. Добавление более стерических защитных групп на атомах бора и менее стерических групп на атомах фосфора благоприятствует структуре бицикло[1.1.0]. Последнее обусловлено уменьшением 1,3-диаксиального напряжения . Копланарное π-связывание с атомом бора и добавление ароматических групп к кольцу благоприятствует структуре бицикло[1.1.0] с длиной связи BB, сокращенной до 1,83 Å. [1] [8]

В плоских дифосфадиборетандиильных структурах можно считать, что существенно длинная связь BB подвергается гомолитическому расщеплению с образованием локализованного синглетного дирадикалоида между атомами бора. [8] Энергия синглетного состояния может быть на 20-35 ккал моль −1 более стабилизирована, чем триплетное состояние . [9] Обнаружено, что добавление π-доноров к атому бора увеличивает синглет-триплетный зазор, в то время как π-акцепторы уменьшают его. Структура бицикло[1.1.0] с более короткой связью BB считается менее дирадикальной и более закрытой системой . [8]
HOMO этих дифосфадиборетандиилов состоит из π-орбитали с сильным борным p-орбитальным характером. [2] Эта орбиталь стабилизируется наличием π-перекрытия между транс -атомами бора (взаимодействия через пространство), а также вкладами через связь от σ* PR-орбиталей. Из-за наличия взаимодействия через пространство вычислительные исследования определили, что эти соединения имеют значительно меньший бирадикальный характер, чем традиционные органические бирадикалы. [10] [11] LUMO является антисвязывающей π* BB-орбиталью. [7]

Было показано, что дифосфадиборетаны ведут себя как лиганды к металл-карбонильным комплексам , образуя бор-моноядерные, бор-биядерные, η 3 и η 4 архитектуры с замещением лигандов CO. [12] Если используются стерические, аминосодержащие заместители на боре, то происходит реакция циклореверсии. Это приводит к получению металл-стабилизированного борафосфена. Сообщалось также о клеточных соединениях (B 2 P 2 M, M = Pd, Pt) с η 2 координацией к атомам P. [13]

Синтез дифосфадиборетана из диборина дает соединение, богатое двумя электронами, по сравнению с дифосфадиборетандиилами. [7] Эти электроны могут быть легко окислены , давая соединение радикального катиона и соединение дифосфодиборетандиила. Обнаружено, что радикальный катион проявляет триплетное состояние с помощью электронного парамагнитного резонанса , сопровождающееся укорочением связи BB (2,63 Å) и небольшим возмущением плоской квадратной структуры. Обнаружено, что соединение дифосфадиборетандиила имеет связь BB 2,12 Å и переход к структуре бицикло[1.1.0]. Анализ орбиталей естественных связей соединения фосфадиборетандиила указывает на изогнутую связь BB с небольшой энергией стабилизации 3 ккал моль −1 по сравнению с плоской структурой.

Дифосфадиборетандиилы проявляют реакционную способность, подобную радикалам , ведя себя как дирадикальные промежуточные соединения. [8] Было показано, что соединения выполняют хлоридную абстракцию из дейтерированного хлороформа , транс -присоединение триметилоловогидрида и образование бицикло[1.1.1] структуры с селеном . Реакционная способность проявляется по отношению к бромтрихлорметану, где радикальная активность вызывает образование борсодержащего спиросоединения из трет- бутильной группы. Это циклическое образование сохраняет структуру кольца дифосфадиборетана.
