В химической номенклатуре дескриптор — это нотационная приставка, помещаемая перед систематическим названием вещества , которая описывает конфигурацию или стереохимию молекулы . [1] Некоторые перечисленные дескрипторы представляют лишь исторический интерес и больше не должны использоваться в публикациях , поскольку не соответствуют современным рекомендациям ИЮПАК . Стереодескрипторы часто используются в сочетании с локантами для четкой и однозначной идентификации химической структуры .
Дескрипторы, обычно располагаемые в начале систематического названия, при алфавитной сортировке не учитываются.
См.: цис-транс-изомерия.


Дескрипторы цис ( лат . по эту сторону ) [2] и транс (лат. над, за пределами ) [3] используются в различных контекстах для описания химических конфигураций: [4] [5]
В органической структурной химии конфигурация двойной связи может быть описана с помощью цис и транс , если она имеет простую схему замещения всего с двумя остатками. Положение двух остатков относительно друг друга в разных точках кольцевой системы или более крупной молекулы также можно описать с помощью цис и транс , если конфигурация структуры жесткая и не допускает простой инверсии.
В неорганической комплексной химии дескрипторы цис и транс используются для характеристики позиционных изомеров в октаэдрических комплексах с конфигурацией A 2 B 4 X или плоских квадратных комплексах с конфигурацией A 2 B 2 X.
Типографское представление цис и транс выделено курсивом и строчными буквами.
Цис / транс- номенклатура не является однозначной для более сильнозамещенных двойных связей и в настоящее время в основном заменена номенклатурой ( E ) /( Z ). [6]
См.: обозначение E – Z.
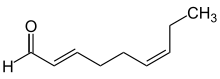
Дескрипторы ( E ) (от немецкого entgegen, напротив) и ( Z ) (от немецкого zusammen, вместе) используются для четкого описания схемы замещения алкенов, кумуленов или других систем двойных связей, таких как оксимы. [7]
Присвоение ( E ) или ( Z ) основано на взаимном положении двух заместителей наивысшего приоритета, находящихся на каждой стороне двойной связи, тогда как приоритет основан на номенклатуре CIP. Номенклатура ( E )/( Z ) может применяться к любым системам двойных связей (включая гетероатомы), но не к замещенным кольцевым системам. Дескрипторы ( E ) и ( Z ) всегда пишутся с заглавной буквы, выделяются курсивом и заключаются в круглые скобки, которые устанавливаются как обычно, как дополнительные локанты или запятые.
См.: Схема замены арена.
Аббревиатура о – (сокращение от орто , от греческого orthós – вертикальный, прямой), [8] м – ( мета , по-гречески (приблизительно) между) [9] и п – ( пара , от греческого пара – примыкающий, к сторона) [10] описывают три возможных позиционных изомера двух заместителей в бензольном кольце . Обычно это два независимых одиночных заместителя, но в случае конденсированных кольцевых систем также упоминается орто -слияние, если только в названии не учтена схема замещения, как в [2.2]парациклофане . В действующей систематической номенклатуре о- , м- и п- часто заменяют использованием локантов ( 1,2-диметилбензол вместо о -ксилола).
о- , м- и п- (записываются орто- , мета- и пара- ) пишутся строчными буквами и курсивом.
экзо (от греч. снаружи) [11] или эндо (от греч. endon = внутри) [12] обозначает относительную конфигурацию мостиковых бициклических соединений. Положение заместителя в основном кольце относительно кратчайшего мостика имеет решающее значение для отнесения экзо или эндо (согласно ИЮПАК: мостик с высшими локантными цифрами [13] в мостиковой кольцевой системе). Заместителю, подлежащему классификации, присваивается дескриптор exo , если смотреть на мостик. Он настроен на эндоконфигурацию , если смотреть в сторону от моста. Если два разных заместителя расположены у одного и того же атома С, то отнесение экзо / эндо осуществляется на основе заместителя с более высоким приоритетом согласно правилам CIP.
Если мостиковая бициклическая система несет заместитель у самого короткого мостика, экзо- или эндо- дескриптор не может быть использован для его назначения. Такие изомеры классифицируются по обозначениям син / анти . [13] Если назначаемый заместитель направлен в сторону кольца с наибольшим числом сегментов, это синконфигурация (от греческого син = вместе). [14] В противном случае ему приписывается антидескриптор ( греч. anti = против). [15] Если оба кольца имеют одинаковое количество сегментов, выбирается кольцо с наиболее значимым заместителем в соответствии с правилами CIP.

Использование син и анти для обозначения конфигурации двойных связей в настоящее время устарело, особенно в случае альдоксимов и гидразонов , полученных из альдегидов . Здесь соединения были обозначены как синконфигурированные , когда альдегид H и O (оксима) или N (гидразона) были цис- выровнены. Эти соединения теперь описываются номенклатурой ( E )/( Z ). Поэтому альдоксимы и гидразоны, классифицированные как син , в настоящее время описываются как ( E ) конфигурации. [14]
Когда речь идет о диастереомерах, син и анти используются для описания групп на одном и том же или противоположных сайтах в зигзагообразной проекции, см. Диастереомер # Син / анти.
син и анти всегда пишутся маленьким курсивом, локанты (если они используются) ставятся перед словом и разделяются дефисом.
Термины fac (от лат. facies) [16] и mer (от meridonal) [17] могут обозначать расположение трех одинаковых лигандов вокруг центрального атома в октаэдрических комплексах. Сегодня эта номенклатура считается устаревшей, но все еще допустима. [18] [19] Приставка fac описывает ситуацию, когда три идентичных лиганда занимают три вершины треугольной поверхности октаэдра. В мерной конфигурации три лиганда охватывают плоскость, в которой расположен центральный атом.
fac и mer начинаются с префикса мелким шрифтом и курсивом перед сложным именем.
Префиксы n (нормальный), iso (от греческого ísos = равный), [20] neo (греческий néos = молодой, новый) [21] и цикло (греческий kyklos = круг) [22] в основном используются для описания расположения атомы, обычно атомы углерода в углеродном скелете. n , iso и neo больше не используются в систематической номенклатуре, но по-прежнему часто используются в тривиальных названиях и в лабораторном жаргоне.
Префикс n описывает углеродный скелет с прямой цепью без разветвлений, тогда как iso описывает разветвленный скелет без указания каких-либо дополнительных подробностей. В более общем смысле изо представляет собой соединение, изомерное n- соединению (соединение, в котором отдельные атомы или атомные группы перегруппированы).
neo — неспецифический термин для «новых», обычно синтетически полученных веществ или изомеров давно известных n- соединений или природных веществ (например, неоментола, полученного из ментола , или неоабиетиновой кислоты из абиетиновой кислоты ). Согласно IUPAC neo рекомендуется использовать только в неопентане или неопентильном остатке. [23] [24]
цикло — часто используемый префикс для всех циклических и гетероциклических соединений. Во многих собственных именах химических веществ цикло используется не как префикс, а непосредственно как часть названия, например в циклогексане или циклооктатетраене.
В то время как n , iso и neo пишутся маленькими буквами курсивом, для цикло это характерно только для неорганических соединений. [25] В органических соединениях слово «цикло» часто используется в качестве компонента названия, не отделяется дефисом, а также учитывается при сортировке по алфавиту.
Префиксы sec и tert используются для обозначения заместительного окружения в молекуле. Таким образом, описывается не точное положение заместителя, а только характер замещения соседнего атома (обычно атома углерода). В н -бутаноле ОН-группа присоединена к первичному атому углерода, в втор -бутаноле — к вторичному атому углерода, а в трет -бутаноле — к третичному атому углерода.
Термины втор- и трет считаются устаревшими и их следует использовать только для незамещенных втор-бутокси, втор-бутила [26] [27] или трет-бутила. [28] [27] Существуют различные варианты написания, такие как «втор-бутил», «в-бутил», «sBu» или «автобус», которые также считаются устаревшими. [29] [30]

Приставка «спиро», за которой следует дескриптор Фон-Байера, описывает в номенклатуре органических соединений кольцевые системы, связанные только одним общим атомом, спироатомом. Если в молекуле присутствует несколько спироатомов, к приставке «спиро» добавляется приставка («диспиро», «триспиро» и т. д.), соответствующая числу спироатомов. Обычно «спиро» устанавливается как обычно. [31]
Термин катена используется в неорганической номенклатуре [32] для описания линейных, цепочечных полимеров, состоящих из идентичных многоатомных звеньев. [33] Одним из примеров являются катенатрифосфазены. [34] [35] Родственными соединениями в органической химии являются катенаны .
Обозначение sn означает стереоспецифическую нумерацию и указывает на особый способ нумерации атомов углерода в молекуле на основе глицерина.
См.: Правила приоритета Кана – Ингольда – Прелога.

Стереохимические дескрипторы ( R ) (от лат. rectus = правый) и ( S ) (от лат. sinister = левый) [36] используются для описания абсолютной конфигурации стереоцентра (обычно хирального атома углерода). [37] Для этой цели всем заместителям в стереоцентре присваивается приоритет в соответствии с правилами CIP, а заместитель с наименьшим приоритетом («D») указывается назад (от направления взгляда). Стереоцентр ( S ) конфигурируется, если оставшиеся заместители описывают круг, нисходящий по приоритету («А» → «В» → «С») влево. Конфигурация ( R ) присваивается стереоцентру, если направление вращения направлено вправо.
Если одна молекула содержит несколько стереоцентров, перед дескриптором необходимо поставить локант (например, в (1R , 2S ) -2-амино-1-фенилпропан-1-оле — систематическое обозначение норэфедрина ) . Если все стереоцентры настроены одинаково, наименование локантов можно опустить в пользу написания «all- R » или «(all- S )».
Типографически ( R ) и ( S ) выделяются прописными буквами и курсивом; часто предшествующие локанты, заключающие круглые скобки и запятые, с другой стороны, как обычно.
Дескрипторы ( r ) и ( s ) используются для описания абсолютной конфигурации псевдоасимметричных центров. [38] Псевдоасимметрия возникает, когда к одному атому углерода присоединяются четыре разных заместителя, два из которых различаются только своей абсолютной стереохимической конфигурацией. Примерами таковых являются мезосоединения, такие как тропановые алкалоиды; исходное соединение — тропин , систематическое название которого — (1R , 3r , 5S ) -8-метил-8-азабицикло[3.2.1]октан-3-ол. В этой структуре атом C3 — углерод, к которому присоединена гидроксильная группа , — псевдоасимметричен; поэтому стереохимический дескриптор в названии системы пишется курсивом в нижнем регистре, а не в верхнем регистре, как для обычных хиральных атомов.
См.: Проекция Фишера.
Стереоскрипторы D - (от лат. dexter, справа) и L - (лат. laevus, слева) используются для описания конфигурации α-аминокислот и сахаров. [39] Во-первых, трехмерную молекулу необходимо преобразовать в определенные обозначения как двумерное изображение («проекция Фишера»). [40] Для этого атом C с наивысшим приоритетом в соответствии с обычными правилами номенклатуры располагается сверху, а дополнительная углеродная цепь располагается вертикально снизу. Для присвоения D- или L- используется хиральный атом С, наиболее удаленный от группы с наивысшим приоритетом . Если остаток, расположенный при этом атоме углерода (обычно ОН-группа), направлен влево, молекула происходит из L -ряда. Если остаток указывает вправо, используется дескриптор D- . [41]
Дескрипторы D- и L- пишутся маленькими заглавными буквами и отделяются дефисом от остального имени. [42]
Иногда упомянутые выше маленькие заглавные D- и L- стереодескрипторы ошибочно путают с устаревшими курсивными d- и l- стереодескрипторами, которые эквивалентны правовращающему и левовращающему оптическому вращению , т.е. (+)- и (-)- стереодескрипторы соответственно.