
Енамин — ненасыщенное соединение , полученное конденсацией альдегида или кетона со вторичным амином . [1] [2] Енамины являются универсальными промежуточными продуктами. [3] [4]
Слово «енамин» происходит от аффикса эн- , используемого в качестве суффикса слова алкен , и корня амина . Это можно сравнить с енолом , который представляет собой функциональную группу, содержащую как алкен ( ен- ), так и спирт (-ол ) . Енамины считаются азотистыми аналогами енолов. [6]
Если один или оба заместителя азота представляют собой атом водорода, это таутомерная форма имина . Обычно это перегруппировывается в имин; однако есть несколько исключений (например, анилин ). Енамин-иминную таутомерию можно считать аналогом кето-енольной таутомерии . В обоих случаях атом водорода меняет свое положение между гетероатомом (кислорода или азота) и вторым атомом углерода.
Енамины являются одновременно хорошими нуклеофилами и хорошими основаниями. Их поведение как нуклеофилов на основе углерода объясняется следующими резонансными структурами.
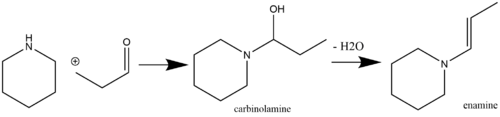
Енамины являются лабильными и, следовательно, химически полезными фрагментами, которые можно легко получить из коммерчески доступных исходных реагентов. Распространенным путем получения енамина является кислотно-катализируемая нуклеофильная реакция кетонов [7] или альдегидов [8] , содержащих α-водород, со вторичными аминами. Кислотный катализ не всегда требуется, если pK aH реагирующего амина достаточно высока (например, пирролидин , имеющий pK aH 11,26). Однако если pK aH реагирующего амина низок, то необходим кислотный катализ как на стадиях присоединения, так и на стадиях дегидратации [9] (обычные дегидратирующие агенты включают MgSO 4 и Na 2 SO 4 ). [10] Первичные амины обычно не используются для синтеза енаминов из-за преимущественного образования более термодинамически стабильных видов имина. [11] Самоконденсация метилкетона является побочной реакцией, которой можно избежать, добавив в реакционную смесь TiCl 4 [12] (который действует как поглотитель воды ). [13] [14] Пример реакции альдегида со вторичным амином с образованием енамина через промежуточный карбиноламин показан ниже:
Несмотря на то, что енамины более нуклеофильны, чем их енольные аналоги, они все же могут реагировать избирательно, что делает их полезными для реакций алкилирования. Нуклеофил енамина может атаковать галогеналканы с образованием промежуточной алкилированной иминиевой соли, которая затем гидролизуется с регенерацией кетона (исходного материала в синтезе енамина). Эта реакция была впервые предложена Гилбертом Сторком , и иногда ее называют по имени ее изобретателя ( енаминное алкилирование Сторка ). Аналогично, эту реакцию можно использовать как эффективный способ ацилирования . В этой реакции можно использовать различные алкилирующие и ацилирующие агенты, включая бензильные и аллилгалогениды. [15]

В реакции, очень похожей на алкилирование енамина, енамины могут ацилироваться с образованием конечного дикарбонильного продукта. Исходный материал енамина подвергается нуклеофильному присоединению к ацилгалогенидам с образованием промежуточной иминиевой соли, которая может гидролизоваться в присутствии кислоты. [16]

Сильные основания, такие как LiNR 2 , можно использовать для депротонирования иминов и образования металлоенаминов. Металлоенамины могут оказаться синтетически полезными из-за их нуклеофильности (они более нуклеофильны, чем еноляты). Таким образом, они лучше реагируют с более слабыми электрофилами (например, их можно использовать для открытия эпоксидов . [17] ). Самое главное, эти реакции позволили провести асимметричное алкилирование кетонов посредством превращения в хиральные промежуточные металлоенамины. [18]
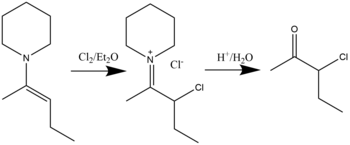
Соединения β-галогениммония можно синтезировать реакцией галогенирования енаминов галогенидами в растворителе диэтиловом эфире . Гидролиз приведет к образованию α-галогенкетонов. [19] Было показано, что хлорирование, бромирование и даже йодирование возможно. Общая реакция показана ниже:
Енамин можно эффективно перекрестно сочетать с енолсиланами путем обработки цериево-аммиачной селитрой . Об этих реакциях сообщила группа Нарасака в 1975 году, что позволило получить стабильные енамины, а также один пример 1,4-дикетона (полученного из реагента морфолин -амина). [20] Позже эти результаты были использованы группой Макмиллана при разработке органокализатора , который использовал субстраты Нарасака для энантиоселективного производства 1,4 дикарбонилов с хорошими выходами. [21] Окислительная димеризация альдегидов в присутствии аминов протекает через образование енамина с последующим окончательным образованием пиррола . [22] Этот метод симметричного синтеза пиррола был разработан в 2010 году группой Jia как ценный новый путь синтеза пирролсодержащих природных продуктов. [23]
Химия енаминов была использована с целью создания однореакторной энантиоселективной версии кольца Робинсона . Аннуляция Робинсона, опубликованная Робертом Робинсоном в 1935 году, представляет собой реакцию, катализируемую основаниями, в которой кетон и метилвинилкетон ( обычно сокращенно MVK) объединяются с образованием конденсированной кольцевой системы циклогексенона . Эта реакция может катализироваться пролином , протекая через хиральные промежуточные енаминовые соединения, которые обеспечивают хорошую стереоселективность. [24] Это важно, в частности, в области синтеза природных продуктов, например, для синтеза кетона Виланда-Мишера – жизненно важного строительного блока для более сложных биологически активных молекул. [25] [26]
Енамины действуют как нуклеофилы, которым для реакционной способности требуется меньшая кислотно-основная активация, чем их енолятным аналогам. Также было показано, что они обладают большей селективностью и меньшим количеством побочных реакций. Существует градиент реакционной способности между различными типами енаминов: кетоновые енамины обладают большей реакционной способностью, чем их альдегидные аналоги. [27] Циклические кетоны-енамины следуют тенденции реакционной способности, при которой пятичленное кольцо является наиболее реакционноспособным из-за его максимально плоской конформации по азоту, следуя тенденции 5>8>6>7 (семичленное кольцо является наименее реакционноспособным). Эта тенденция объясняется количеством p-символа на орбитали неподеленной пары азота - более высокий p-символ соответствует большей нуклеофильности, поскольку p-орбиталь допускает донорство на π-орбитали алкена. Аналогично, если неподеленная пара N участвует в стереоэлектронных взаимодействиях с аминогруппой, неподеленная пара выйдет из плоскости (будет пирамидализоваться ) и поставит под угрозу донорство соседней связи π CC. [28] [29]

Существует много способов модулировать реакционную способность енамина в дополнение к изменению стерических/электронных свойств азотного центра, включая изменение температуры, растворителя, количества других реагентов и типа электрофила. Настройка этих параметров позволяет осуществлять преимущественное образование E/Z-енаминов, а также влияет на образование более/менее замещенного енамина из исходного кетонового материала. [30]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ); Коллективный том , том. 5, с. 1014