Иммунный ответ — это физиологическая реакция, возникающая внутри организма при воспалении с целью защиты от экзогенных факторов. К ним относятся широкий спектр различных токсинов , вирусов , внутри- и внеклеточных бактерий , простейших , гельминтов и грибов , которые могут вызвать серьезные проблемы для здоровья организма-хозяина, если их не вывести из организма. [1]
Кроме того, существуют и другие формы иммунного ответа. Например, безобидные экзогенные факторы (такие как пыльца и компоненты пищи) могут спровоцировать аллергию ; латекс и металлы также являются известными аллергенами. Трансплантированная ткань (например, кровь) или орган может вызвать реакцию «трансплантат против хозяина» . У беременных женщин может наблюдаться тип иммунной реактивности, известный как резус-болезнь . Эти особые формы иммунного ответа классифицируются как гиперчувствительность . Другой особой формой иммунного ответа является противоопухолевый иммунитет .
В целом существует две ветви иммунного ответа: врожденная и адаптивная , которые работают вместе для защиты от патогенов. Обе ветви задействуют гуморальный и клеточный компоненты.
Врожденная ветвь — первая реакция организма на захватчика — как известно, представляет собой неспецифическую и быструю реакцию на любой вид патогена. Компоненты врожденного иммунного ответа включают физические барьеры, такие как кожа и слизистые оболочки, иммунные клетки, такие как нейтрофилы , макрофаги и моноциты , а также растворимые факторы, включая цитокины и комплемент . [2] С другой стороны, адаптивная ветвь — это иммунный ответ организма, направленный против специфических антигенов , и поэтому для активации задействованных компонентов требуется больше времени. Адаптивная ветвь включает такие клетки, как дендритные клетки , Т-клетки и В-клетки , а также антитела , также известные как иммуноглобулины, которые напрямую взаимодействуют с антигеном и являются очень важным компонентом для сильного ответа против захватчика. [1]
Первый контакт организма с определенным антигеном приведет к образованию эффекторных Т- и В-клеток, которые представляют собой активированные клетки, защищающие от патогена. Производство этих эффекторных клеток в результате первого воздействия называется первичным иммунным ответом. Т-клетки памяти и В-клетки памяти также вырабатываются в случае повторного попадания того же патогена в организм. Если организм действительно подвергнется повторному воздействию того же патогена, сработает вторичный иммунный ответ, и иммунная система сможет отреагировать как быстро, так и сильно благодаря клеткам памяти от первого воздействия. [3] Вакцины вводят ослабленный, убитый или фрагментированный микроорганизм, чтобы вызвать первичный иммунный ответ. Это сделано для того, чтобы в случае воздействия настоящего патогена организм мог полагаться на вторичный иммунный ответ для быстрой защиты от него. [4]
Врожденный иммунный ответ — это первая реакция организма на чужеродных захватчиков. Этот иммунный ответ эволюционно консервативен у многих различных видов, причем все многоклеточные организмы имеют ту или иную вариацию врожденного ответа. [5] Врожденная иммунная система состоит из физических барьеров, таких как кожа и слизистые оболочки , различных типов клеток, таких как нейтрофилы , макрофаги и моноциты , а также растворимых факторов, включая цитокины и комплемент. [2] В отличие от адаптивного иммунного ответа , врожденный ответ не специфичен для какого-либо одного инородного захватчика и, как следствие, быстро избавляет организм от патогенов. [ нужна цитата ]
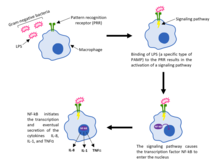
Патогены распознаются и обнаруживаются с помощью рецепторов распознавания образов (PRR). Эти рецепторы представляют собой структуры на поверхности макрофагов, которые способны связывать чужеродных захватчиков и, таким образом, инициировать передачу сигналов внутри иммунной клетки. В частности, PRR идентифицируют молекулярные паттерны, связанные с патогенами (PAMP) , которые являются неотъемлемыми структурными компонентами патогенов. Примеры PAMP включают клеточную стенку пептидогликана или липополисахариды (LPS), которые оба являются важными компонентами бактерий и, следовательно, эволюционно консервативны у многих различных видов бактерий. [6]
Когда чужеродный патоген обходит физические барьеры и попадает в организм, PRR на макрофагах распознают специфические PAMP и связываются с ними. Это связывание приводит к активации сигнального пути , который позволяет транскрипционному фактору NF-κB проникнуть в ядро макрофага и инициировать транскрипцию и, в конечном итоге, секрецию различных цитокинов , таких как IL-8 , IL-1 и TNFα . [5] Высвобождение этих цитокинов необходимо для проникновения нейтрофилов из кровеносных сосудов в инфицированную ткань. Как только нейтрофилы попадают в ткань, они, подобно макрофагам, способны фагоцитировать и убивать любые патогены или микробы. [ нужна цитата ]
Комплемент , еще один компонент врожденной иммунной системы, состоит из трех путей, которые активируются разными способами. Классический путь запускается, когда IgG или IgM связываются с антигеном-мишенью либо на клеточной мембране патогена, либо на антигенсвязанном антителе. Альтернативный путь активируется чужеродными поверхностями, такими как вирусы, грибы, бактерии, паразиты и т. д., и способен к автоактивации за счет «тиковера» C3. Лектиновый путь запускается, когда маннозосвязывающий лектин (MBL) или фиколин , известный как специфические рецепторы распознавания образов, связывается с патоген-ассоциированными молекулярными узорами на поверхности вторгающихся микроорганизмов, таких как дрожжи , бактерии, паразиты и вирусы. [7] Каждый из трех путей гарантирует, что комплемент по-прежнему будет функционировать, если один из путей перестанет работать или инородный захватчик сможет уклониться от одного из этих путей ( принцип глубокоэшелонированной защиты ). [5] Хотя пути активируются по-разному, общая роль системы комплемента заключается в опсонизации патогенов и индукции ряда воспалительных реакций , которые помогают бороться с инфекцией . [ нужна цитата ]
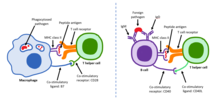
Адаптивный иммунный ответ является второй линией защиты организма . Клетки адаптивной иммунной системы чрезвычайно специфичны, поскольку на ранних стадиях развития В- и Т-клетки развивают антигенные рецепторы, специфичные только к определенным антигенам . Это чрезвычайно важно для активации В- и Т-клеток. В- и Т-клетки являются чрезвычайно опасными клетками, и если они способны атаковать без прохождения строгого процесса активации, неисправная В- или Т-клетка может начать уничтожать собственные здоровые клетки хозяина. [8] Активация наивных Т-хелперов происходит, когда антигенпрезентирующие клетки (APC) представляют чужеродный антиген через молекулы MHC класса II на своей клеточной поверхности. Эти APC включают дендритные клетки , B-клетки и макрофаги , которые специально оснащены не только MHC класса II, но также и костимулирующими лигандами, которые распознаются костимулирующими рецепторами на Т-хелперных клетках. Без костимулирующих молекул адаптивный иммунный ответ был бы неэффективным, и Т-клетки стали бы анергическими . Несколько подгрупп Т-клеток могут быть активированы определенными АПК, и каждая Т-клетка специально оснащена для борьбы с каждым уникальным микробным патогеном. Тип активированных Т-клеток и тип генерируемого ответа частично зависят от контекста, в котором APC впервые столкнулся с антигеном. [9] Как только Т-хелперы активированы, они способны активировать наивные В-клетки в лимфатическом узле . Однако активация B-клеток представляет собой двухэтапный процесс. Во-первых, рецепторы B-клеток, которые представляют собой антитела иммуноглобулина M (IgM) и иммуноглобулина D (IgD), специфичные для конкретной B-клетки, должны связываться с антигеном, что затем приводит к внутренней обработке, так что он презентируется на молекулах MHC класса II. В-клетки. Как только это происходит, Т-хелперная клетка, которая способна идентифицировать антиген, связанный с MHC, взаимодействует с его костимулирующей молекулой и активирует B-клетку. В результате В-клетка становится плазматической клеткой , которая секретирует антитела, действующие как опсонин против захватчиков. [ нужна цитата ]
Специфичность адаптивной ветви обусловлена тем, что все В- и Т-клетки различны. Таким образом, существует разнообразное сообщество клеток, готовое распознавать и атаковать весь спектр захватчиков. [8] Однако компромисс заключается в том, что адаптивный иммунный ответ гораздо медленнее, чем врожденный ответ организма, поскольку его клетки чрезвычайно специфичны, и требуется активация, прежде чем он сможет действительно действовать. Помимо специфичности, адаптивный иммунный ответ известен еще и иммунологической памятью . После встречи с антигеном иммунная система вырабатывает Т- и В-клетки памяти, которые обеспечивают более быстрый и устойчивый иммунный ответ в случае, если организм когда-либо снова встретит тот же антиген. [8]

В зависимости от экзогенных потребностей выделяют несколько типов иммунного ответа (ИР). В этой парадигме клеточные и молекулярные компоненты иммунной системы (как врожденной, так и адаптивной) и неиммунной системы организованы таким образом, чтобы оптимально реагировать на различные воздействия экспозомов.
В настоящее время классифицируют несколько типов ИР. [10] [11]
ИР 1 типа вызывают вирусы, внутриклеточные бактерии, паразиты. Действующими лицами здесь являются врожденные лимфоидные клетки 1-й группы (ILC1), NK-клетки, клетки Th1, макрофаги, опсонизирующие изотипы IgG.
ИР 2 типа вызывают токсины и многоклеточные паразиты. Ключевыми игроками здесь являются ILC2, эпителиальные клетки , Th2-лимфоциты, эозинофилы, базофилы, тучные клетки, IgE.
IR типа 3 нацелен на внеклеточные бактерии и грибы, рекрутируя ILC3, Th17, нейтрофилы, опсонизируя изотипы IgG.
Дополнительные виды ИР могут наблюдаться при неинфекционных патологиях. [12]
Все виды ИР имеют сенсорную (ILC, NK-клетки), адаптивную (Т- и В-клетки) и эффекторную ( нейтрофилы , эозинофилы , базофилы , тучные клетки ) части. [11]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )[ нужна страница ]{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) CS1 maint: другие ( ссылка )[ нужна страница ]{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )[ нужна страница ]