
Феноксигербициды (или « фенокси ») представляют собой два семейства химических веществ, которые были разработаны как коммерчески важные гербициды и широко используются в сельском хозяйстве . Они разделяют структуру части феноксиуксусной кислоты .
Первая открытая группа действует, имитируя индолуксусную кислоту гормона роста ауксина (IAA). [1] При опрыскивании широколистных растений они вызывают быстрый, неконтролируемый рост («растет до смерти»). Таким образом, при применении к однодольным культурам, таким как пшеница или кукуруза (кукуруза), они избирательно уничтожают широколистные сорняки, оставляя посевы относительно незатронутыми.
Представленные в 1946 году, эти гербициды получили широкое распространение в сельском хозяйстве к середине 1950-х годов. Наиболее известными феноксигербицидами являются (4-хлор-2-метилфенокси)уксусная кислота ( MCPA ), 2,4-дихлорфеноксиуксусная кислота (2,4-D) и 2,4,5-трихлорфеноксиуксусная кислота (2,4,5- Т). [2] Аналоги каждого из этих трех соединений с дополнительной метильной группой, присоединенной рядом с карбоновой кислотой , впоследствии были коммерциализированы как мекопроп , дихлорпроп и фенопроп . Добавление метильной группы создает в этих молекулах хиральный центр, и биологическая активность обнаруживается только у (2R)-изомера (показано для дихлорпропа). [3]
Другие члены этой группы включают 4-(2,4-дихлорфенокси)масляную кислоту ( 2,4-DB ) и 4-(4-хлор-2-метилфенокси)масляную кислоту ( MCPB ), которые действуют как пропестициды для 2,4- D и MCPA соответственно: то есть они преобразуются в растениях в эти активные ингредиенты. [4] Все ауксиновые гербициды сохраняют активность при применении в виде солей и эфиров , поскольку они также способны производить исходную кислоту in situ .

Использование гербицидов в сельском хозяйстве США составлено Геологической службой США. По состоянию на 2019 год [обновлять]наиболее часто используемым из ауксинов был 2,4-Д. В том году было распылено 45 000 000 фунтов (20 000 000 кг) [5] по сравнению с 2 000 000 фунтов (910 000 кг) следующего наиболее интенсивно применяемого MCPA. [6] Другой ауксин, который сейчас используется в количествах, сопоставимых с 2,4-Д, — это дикамба , показатель которого в 2019 году составил 30 000 000 фунтов (14 000 000 кг). [7] Это бензойная кислота , а не феноксиуксусная кислота, использование которой быстро растет с 2016 года, поскольку выращиваются генетически модифицированные культуры , устойчивые к ней. [8]
В 1970-х годах агрохимические компании работали над разработкой новых гербицидов, дополняющих ауксины. Целью было найти материалы, которые могли бы избирательно бороться с травяными сорняками в широколиственных культурах, таких как хлопок и соя .

В 1973 году компания Hoechst AG подала патенты на новый класс соединений — арилоксфеноксипропионаты, которые показали такую селективность и привели к коммерциализации диклофопа. Затем японская компания Ishihara Sangyo Kaisha (ISK) обнаружила улучшенную биологическую активность у аналога хлоразифопа, в котором арилокси-часть диклофопа была заменена пиридиновым кольцом, содержащим те же два хлорсодержащих заместителя. Эта область исследований стала очень конкурентной, и в течение трех недель друг от друга в 1977 году ISK, Dow Chemicals и Imperial Chemical Industries (ICI) подали патенты, охватывающие другую группу аналогов, с трифторметильной (CF 3 ) группой вместо одной из Атомы хлора в пиридине. Впоследствии ISK и ICI перекрестно лицензировали свою интеллектуальную собственность и впервые продали флуазифоп как его бутиловый эфир в 1981 году под торговой маркой Fusilade, в то время как Dow продавала галоксифоп как его метиловый эфир. [9] Все эти соединения имеют дополнительную связанную с кислородом ароматическую группу в пара-положении фенильного кольца с его группой OCH(CH 3 )COOH и как класс называются «фопами», имея в виду их общий фенокси-фенокси [sic ] особенность. [10]
Эта группа гербицидов действует путем ингибирования ацетил-КоА-карбоксилазы растений (АССаза), механизм действия которого совершенно иной , чем у ауксинов. [11] [12] Их селективность в отношении трав возникает потому, что они нацелены на изоформу фермента, присутствующую только в пластидах этих видов , что делает их неэффективными в отношении широколистных сорняков и других организмов, включая млекопитающих. [13] При применении в виде сложного эфира метаболизм в целевом растении приводит к образованию исходной кислоты, которая отвечает за гербицидное действие. [9] [14] Это совпадение, что именно (2R) стереоизомер связывается с АССазой растения, точно так же, как этот изомер отвечает за активность дихлорпропа в качестве ауксина.
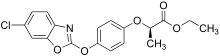

Соли и эфиры этого класса гербицидов активны благодаря их способности метаболизироваться до соответствующей исходной кислоты. Например, этил феноксапроп-П [15] был представлен компанией Bayer Crop Science , а этил квизалофоп-П компанией Nissan Chemical Corporation в 1989 году. [16] В 1990 году компания Dow представила бутил цигалофоп-П для борьбы с сорняками в рисе. [17] Бутил флюазифоп-П [18] до сих пор широко используется в США. В 2018 году было внесено 200 000 фунтов (91 000 кг) — почти исключительно при выращивании сои. [19] Буква «P» в названии этих материалов указывает на их использование в настоящее время в виде отдельных энантиомеров .
Камминс и др. , 1999, 2009 и 2013 обнаружили, что механизм устойчивости Alopecurus myocuroides к феноксапропу-P-этилу снижает концентрацию перекиси водорода в месте применения, в то время как дикий тип реагирует увеличением. [20]