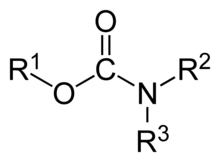
В органической химии карбамат — это категория органических соединений с общей формулой R 2 NC(O)OR и структурой >N−C(=O)−O− , которые формально получены из карбаминовой кислоты ( NH 2 COOH ). Термин включает органические соединения (например, эфир этилкарбамат ), формально полученные путем замены одного или нескольких атомов водорода другими органическими функциональными группами ; а также соли с карбаматным анионом H 2 NCOO − (например, карбамат аммония ). [1]
Полимеры, повторяющиеся звенья которых соединены карбаматными группами −NH−C(=O)−O−, являются важным семейством пластиков , полиуретанов . См. § Этимология для пояснения.
В то время как карбаминовые кислоты нестабильны, многие эфиры и соли карбаматов стабильны и хорошо известны. [2]
В водных растворах карбаматный анион медленно приходит в равновесие с аммонием NH+
4катион и карбонат CO2−
3или бикарбонат HCO−
3анионы: [3] [4] [5]
Карбамат кальция растворим в воде, а карбонат кальция — нет. Добавление соли кальция к раствору карбамата/карбоната аммония немедленно осаждает некоторое количество карбоната кальция, а затем медленно осаждает больше по мере гидролиза карбамата. [3]
Соль карбамата аммония образуется при обработке аммиака диоксидом углерода : [6]
Эфиры карбамата также возникают в результате алкоголиза карбамоилхлоридов : [1]
Альтернативно, карбаматы могут быть образованы из хлорформиатов и аминов : [7]
Карбаматы могут быть образованы в результате перегруппировки Курциуса , где образовавшиеся изоцианаты реагируют со спиртом. [7]
В природе углекислый газ может связываться с нейтральными аминогруппами, образуя карбамат, эта посттрансляционная модификация известна как карбамилирование. Известно, что эта модификация происходит на нескольких важных белках; см. примеры ниже. [8]
N-концевые аминогруппы остатков валина в α- и β-цепях дезоксигемоглобина существуют в виде карбаматов. Они помогают стабилизировать белок, когда он становится дезоксигемоглобином, и увеличивают вероятность высвобождения оставшихся молекул кислорода , связанных с белком. Этот стабилизирующий эффект не следует путать с эффектом Бора (косвенным эффектом, вызванным диоксидом углерода). [9]
ε-аминогруппы остатков лизина в уреазе и фосфотриэстеразе также содержат карбамат. Карбамат, полученный из аминоимидазола, является промежуточным продуктом в биосинтезе инозина . Карбамоилфосфат образуется из карбоксифосфата, а не из CO 2 . [10]
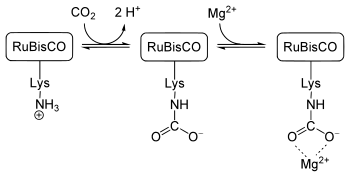
Возможно, наиболее распространенным карбаматом является тот, который участвует в захвате CO 2 растениями. Этот процесс необходим для их роста. Фермент рибулозо-1,5-бисфосфаткарбоксилаза/оксигеназа (RuBisCO) фиксирует молекулу углекислого газа как фосфоглицерат в цикле Кальвина . В активном центре фермента ион Mg 2+ связывается с остатками глутамата и аспартата, а также с карбаматом лизина. Карбамат образуется, когда незаряженная боковая цепь лизина около иона реагирует с молекулой углекислого газа из воздуха ( не с молекулой углекислого газа субстрата), что затем делает ее заряженной и, следовательно, способной связывать ион Mg 2+ . [11]
Хотя соль карбамата аммония обычно не выделяют как таковую, ее производят в больших масштабах в качестве промежуточного продукта при производстве товарной химической мочевины из аммиака и диоксида углерода . [1]
Полиуретаны содержат несколько карбаматных групп как часть своей структуры. «Уретан» в названии «полиуретан» относится к этим карбаматным группам; термин «уретановые связи» описывает, как полимеризуются карбаматы . [Требуется ссылка] Напротив, вещество, обычно называемое «уретаном», этилкарбамат , не является ни компонентом полиуретанов, ни используется в их производстве. [Требуется ссылка] Уретаны обычно образуются в результате реакции спирта с изоцианатом . [ Требуется ссылка] Обычно уретаны, полученные неизоцианатным путем, называются карбаматами . [Требуется ссылка]
Полиуретановые полимеры имеют широкий спектр свойств и коммерчески доступны в виде пен, эластомеров и твердых веществ. Обычно полиуретановые полимеры производятся путем объединения диизоцианатов, например, толуолдиизоцианата , и диолов , где карбаматные группы образуются в результате реакции спиртов с изоцианатами : [ 12]
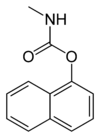
Так называемые карбаматные инсектициды имеют функциональную группу карбаматного эфира. В эту группу входят алдикарб ( Темик ), карбофуран (Фурадан), карбарил (Севин), этиенокарб , фенобукарб , оксамил и метомил . Эти инсектициды убивают насекомых, обратимо инактивируя фермент ацетилхолинэстеразу (ингибирование АХЭ) [13] ( способ действия IRAC 1a). [14] Органофосфатные пестициды также ингибируют этот фермент, хотя и необратимо, и вызывают более тяжелую форму холинергического отравления [15] (аналогичный IRAC MoA 1b). [14]
Феноксикарб имеет карбаматную группу, но действует как имитатор ювенильного гормона , а не инактивирует ацетилхолинэстеразу. [16]
Репеллент от насекомых икаридин представляет собой замещенный карбамат. [17]
Помимо их обычного использования в качестве артроподоцидов/инсектицидов, они также являются нематоцидами . [18] Одним из таких является Оксамил . [18]
За последние десятилетия продажи резко упали. [18]
Среди мутаций эстераз резистентность к карбамату чаще всего связана с десенсибилизацией ацетилхолинэстеразы (АХЭ), тогда как резистентность к органофосфату чаще всего связана с метаболизмом карбоксилэстеразы . [19]
В то время как ингибиторы ацетилхолинэстеразы карбамата обычно называют «карбаматными инсектицидами» из-за их в целом высокой селективности к ферментам ацетилхолинэстеразы насекомых по сравнению с версиями млекопитающих, наиболее мощные соединения, такие как алдикарб и карбофуран, все еще способны ингибировать ферменты ацетилхолинэстеразы млекопитающих при достаточно низких концентрациях, что создает значительный риск отравления для людей, особенно при использовании в больших количествах в сельскохозяйственных целях. Другие ингибиторы ацетилхолинэстеразы на основе карбамата известны еще более высокой токсичностью для людей, и некоторые из них, такие как T-1123 и EA-3990, были исследованы на предмет потенциального военного использования в качестве нервно-паралитических агентов . Однако, поскольку все соединения этого типа имеют четвертичную аммониевую группу с постоянным положительным зарядом, они плохо проникают через гематоэнцефалический барьер , а также стабильны только в виде кристаллических солей или водных растворов, и поэтому не считались имеющими подходящие свойства для использования в качестве оружия. [20] [21]
Иодопропинилбутилкарбамат — консервант для древесины и красок, используемый в косметике. [22]
Некоторые из наиболее распространенных защитных групп аминов, такие как BOC , [23] FMOC , [24] бензилхлорформиат [25] и трихлорэтилхлорформиат [26], являются карбаматами.
Уретан ( этилкарбамат ) когда-то производился в коммерческих целях в Соединенных Штатах в качестве химиотерапевтического агента и для других медицинских целей. Он оказался токсичным и в значительной степени неэффективным. [27] Иногда его используют в ветеринарии в сочетании с другими препаратами для анестезии . [28]
Кроме того, некоторые карбаматы используются в фармакотерапии человека , например, ингибиторы ацетилхолинэстеразы неостигмин и ривастигмин , химическая структура которых основана на природном алкалоиде физостигмине . Другими примерами являются мепробамат и его производные, такие как каризопродол , фелбамат , мебутамат , фенпробамат и тибамат , класс анксиолитиков и миорелаксантов , широко применявшихся в 1960-х годах до появления бензодиазепинов, и до сих пор в некоторых случаях используемых в настоящее время. Карбахол в основном используется для различных офтальмологических целей. [29]
Ингибитор протеазы дарунавир для лечения ВИЧ также содержит карбаматную функциональную группу. [30]
Эфедроксан , аналог аминорекса , используемый в качестве стимулятора , также попадает в категорию карбаматов. [31]
Помимо ингибирования человеческой ацетилхолинэстеразы [32] (хотя и в меньшей степени, чем фермент насекомых), карбаматные инсектициды также воздействуют на человеческие рецепторы мелатонина. [33] Влияние карбаматов на здоровье человека хорошо документировано в списке известных соединений, нарушающих эндокринную систему. [34] Клинические эффекты воздействия карбамата могут варьироваться от слегка токсичных до высокотоксичных в зависимости от различных факторов, включая такие, как доза и путь воздействия, при этом проглатывание и вдыхание приводят к наиболее быстрым клиническим эффектам. [34] Клиническими проявлениями интоксикации карбаматом являются мускариновые признаки, никотиновые признаки и, в редких случаях, признаки поражения центральной нервной системы. [34]
В карбамате ( 1 ), ROC(=O)NR 2 , есть два атома кислорода , и один или оба из них могут быть концептуально заменены серой . Аналоги карбаматов, в которых только один из атомов кислорода заменен серой, называются тиокарбаматами ( 2 и 3 ). Карбаматы, в которых оба атома кислорода заменены серой, называются дитиокарбаматами ( 4 ), RSC(=S)NR 2 . [35]
Существует два различных структурно-изомерных типа тиокарбамата:
O -тиокарбаматы могут изомеризоваться в S -тиокарбаматы, например, в перегруппировке Ньюмена-Кварта . [37]
Этимология слов «уретан» и «карбамат» очень похожа, но не одинакова. Слово «уретан» было впервые придумано в 1833 году французским химиком Жаном-Батистом Дюма. [38] [39] Дюма утверждает: «Уретан. Новый эфир, приведенный в контакт с жидким и концентрированным аммиаком, оказывает на это вещество столь сильную реакцию, что смесь кипит, а иногда даже производит своего рода взрыв. Если аммиак в избытке, весь эфир исчезает. Он образует гидрохлорат аммония и новое вещество, наделенное интересными свойствами». [39] Дюма, по-видимому, называет это соединение уретаном. Однако позднее Дюма заявляет: «В ожидании мнения, которое установится относительно природы этого тела, я предлагаю обозначить названиями уретан и оксаметан два материала, которые я только что изучил и которые я рассматриваю как типы нового семейства среди азотистых веществ . Эти названия, которые, на мой взгляд, ничего не предрешают в вопросе спирта и эфиров, по крайней мере будут иметь то преимущество, что удовлетворят химиков, которые все еще отказываются принять нашу теорию». [39] Слово уретан происходит от слов «мочевина» и «эфир» с суффиксом «-ан» в качестве общего химического суффикса, что делает его специфическим для структуры связи R2NC(=O)OR' (R' не = H). [40]
Использование слова «карбамат», по-видимому, появилось позже, и его можно проследить, по крайней мере, до 1849 года в описании работы Дюма Генри Медлоком. [41] Медлок утверждает: «Хорошо известно, что действие аммиака на хлоркарбонат (фосген) этила приводит к образованию вещества, которое Дюма, первооткрыватель, назвал уретаном, и которое мы теперь привыкли считать эфиром карбаминовой кислоты». [41] Это говорит о том, что вместо того, чтобы продолжать следовать правилу наименования семейства уретанов, придуманному Дюма, они изменили правило наименования на этиловый эфир карбаминовой кислоты. Карбамат происходит от слов «карбамид», также известного как мочевина, и «-ат» — суффикса, который указывает на соль или эфир кислоты. [42] [43]
Оба слова имеют корни, происходящие от мочевины. Карбамат менее специфичен, поскольку суффикс -ate неоднозначен как для соли, так и для эфира карбаминовой кислоты. Однако суффикс -ate также более специфичен, поскольку он предполагает, что карбаматы должны быть получены из кислоты карбамата или карбаминовых кислот . Хотя уретан имеет ту же химическую структуру, что и фрагмент эфира карбамата, уретан, не полученный из карбаминовой кислоты, не является эфиром карбамата. Другими словами, любой синтез фрагмента R2NC(=O)OR' (R' не = H), который не происходит от карбаминовых кислот, не является эфиром карбамата, а вместо этого уретаном. Более того, эфиры карбамата являются уретанами, но не все уретаны являются эфирами карбамата. Это дополнительно предполагает, что полиуретаны не являются просто поликарбаматными эфирами, поскольку полиуретаны обычно не синтезируются с использованием карбаминовых кислот.
ИЮПАК утверждает: «Эти сложные эфиры часто называют уретанами или уретаны, что строго правильно только для этиловых эфиров». [44] Но также утверждает: «Альтернативный термин для соединений R2NC(=O)OR' (R' не = H), эфиры карбаминовых кислот, R,NC(=O)OH, в строгом использовании ограниченном этиловыми эфирами, но широко используемом в общем смысле». [45] ИЮПАК приводит эти утверждения без ссылок.
{{cite book}}: CS1 maint: другие ( ссылка )