
В химии полярность — это разделение электрического заряда, приводящее к тому, что молекула или ее химические группы имеют электрический дипольный момент с отрицательно заряженным концом и положительно заряженным концом.
Полярные молекулы должны содержать одну или несколько полярных связей из-за разницы в электроотрицательности между связанными атомами. Молекулы, содержащие полярные связи, не имеют молекулярной полярности, если диполи связи компенсируют друг друга симметрией.
Полярные молекулы взаимодействуют посредством диполь-дипольных межмолекулярных сил и водородных связей . Полярность лежит в основе ряда физических свойств, включая поверхностное натяжение , растворимость , а также температуры плавления и кипения.
Не все атомы притягивают электроны с одинаковой силой. Величина «тяги», которую атом оказывает на свои электроны, называется его электроотрицательностью . Атомы с высокой электроотрицательностью, такие как фтор , кислород и азот , оказывают большее притяжение на электроны, чем атомы с более низкой электроотрицательностью, такие как щелочные металлы и щелочноземельные металлы . В связи это приводит к неравному распределению электронов между атомами, поскольку электроны будут притягиваться ближе к атому с более высокой электроотрицательностью.
Поскольку электроны имеют отрицательный заряд, неравное распределение электронов внутри связи приводит к образованию электрического диполя : разделению положительного и отрицательного электрического заряда. Поскольку количество заряда, разделенного в таких диполях, обычно меньше фундаментального заряда , их называют частичными зарядами , обозначаемыми как δ+ ( дельта плюс) и δ− (дельта минус). Эти символы были введены сэром Кристофером Ингольдом и Эдит Хильдой (Ашервуд) Ингольд в 1926 году. [1] [2] Дипольный момент связи рассчитывается путем умножения количества разделенного заряда на расстояние между зарядами.
Эти диполи внутри молекул могут взаимодействовать с диполями в других молекулах, создавая диполь-дипольные межмолекулярные силы .
Связи могут находиться между двумя крайностями — полностью неполярными или полностью полярными. Полностью неполярная связь возникает, когда электроотрицательности идентичны и, следовательно, обладают разностью, равной нулю. Полностью полярную связь правильнее называть ионной связью , и она возникает, когда разность электроотрицательностей достаточно велика, чтобы один атом фактически забрал электрон у другого. Термины «полярный» и «неполярный» обычно применяются к ковалентным связям , то есть связям, где полярность не полная. Чтобы определить полярность ковалентной связи с помощью численных средств, используется разность электроотрицательностей атомов.
Полярность связи обычно делится на три группы, которые в общих чертах основаны на разнице электроотрицательности между двумя связанными атомами. Согласно шкале Полинга :
Полинг основал эту схему классификации на частичном ионном характере связи, который является приблизительной функцией разницы в электроотрицательности между двумя связанными атомами. Он подсчитал, что разница в 1,7 соответствует 50% ионному характеру, так что большая разница соответствует связи, которая является преимущественно ионной. [3]
В качестве квантово-механического описания Полинг предположил, что волновая функция для полярной молекулы AB является линейной комбинацией волновых функций для ковалентных и ионных молекул: ψ = aψ(A:B) + bψ(A + B − ). Степень ковалентности и ионности зависит от значений квадратов коэффициентов a 2 и b 2 . [4]
Дипольный момент связи [5] использует идею электрического дипольного момента для измерения полярности химической связи внутри молекулы . Он возникает всякий раз, когда происходит разделение положительных и отрицательных зарядов.
Диполь связи μ определяется по формуле:
Диполь связи моделируется как δ + — δ – с расстоянием d между частичными зарядами δ + и δ – . Это вектор, параллельный оси связи, направленный от минуса к плюсу, [6], как это принято для векторов электрического дипольного момента .
Химики часто рисуют вектор, направленный от плюса к минусу. [7] Этот вектор можно физически интерпретировать как движение, совершаемое электронами, когда два атома находятся на расстоянии d друг от друга и взаимодействуют; электроны будут перемещаться из своих свободных положений, чтобы локализоваться больше вокруг более электроотрицательного атома.
Единицей СИ для электрического дипольного момента является кулон-метр. Это слишком много, чтобы быть практичным в молекулярном масштабе. Дипольные моменты связи обычно измеряются в дебаях , представленных символом D, который получается путем измерения заряда в единицах 10−10 статкулонов и расстояния d в ангстремах . Исходя из коэффициента преобразования 10−10 статкулонов , составляющего 0,208 единиц элементарного заряда, поэтому 1,0 дебай получается из электрона и протона, разделенных 0,208 Å. Полезный коэффициент преобразования составляет 1 D = 3,335 64 × 10 −30 С м. [8]
Для двухатомных молекул существует только одна (одинарная или множественная) связь, поэтому дипольный момент связи является молекулярным дипольным моментом с типичными значениями в диапазоне от 0 до 11 D. С одной стороны, симметричная молекула, такая как бром , Br
2, имеет нулевой дипольный момент, в то время как вблизи другой крайности, газообразная фаза бромида калия , KBr, которая является высокоионной, имеет дипольный момент 10,41 D. [9] [ нужна страница ] [10] [ нужна проверка ]
Для многоатомных молекул существует более одной связи. Полный молекулярный дипольный момент может быть аппроксимирован как векторная сумма индивидуальных дипольных моментов связей. Часто диполи связей получаются обратным процессом: известный полный диполь молекулы может быть разложен на диполи связей. Это делается для передачи дипольных моментов связей молекулам, которые имеют те же связи, но для которых полный дипольный момент еще не известен. Векторная сумма переданных диполей связей дает оценку полного (неизвестного) диполя молекулы.
Молекула состоит из одной или нескольких химических связей между молекулярными орбиталями разных атомов. Молекула может быть полярной либо в результате полярных связей из-за различий в электроотрицательности, как описано выше, либо в результате асимметричного расположения неполярных ковалентных связей и несвязывающих пар электронов, известных как полная молекулярная орбиталь .
Хотя молекулы можно описать как «полярные ковалентные», «неполярные ковалентные» или «ионные», это часто относительный термин, поскольку одна молекула просто более полярна или более неполярна , чем другая. Однако для таких молекул типичны следующие свойства.
При сравнении полярной и неполярной молекулы с близкими молярными массами, полярная молекула в целом имеет более высокую температуру кипения, поскольку диполь-дипольное взаимодействие между полярными молекулами приводит к более сильному межмолекулярному притяжению. Одной из распространенных форм полярного взаимодействия является водородная связь , которая также известна как Н-связь. Например, вода образует Н-связи и имеет молярную массу M = 18 и температуру кипения +100 °C по сравнению с неполярным метаном с M = 16 и температурой кипения –161 °C.
Из-за полярной природы самой молекулы воды, другие полярные молекулы, как правило, способны растворяться в воде. Большинство неполярных молекул нерастворимы в воде ( гидрофобны ) при комнатной температуре. Многие неполярные органические растворители , такие как скипидар , способны растворять неполярные вещества.
Полярные соединения, как правило, имеют более высокое поверхностное натяжение , чем неполярные соединения. [ необходима цитата ]
Полярные жидкости имеют тенденцию подниматься против силы тяжести в трубке малого диаметра. [ необходима цитата ]
Полярные жидкости имеют тенденцию быть более вязкими , чем неполярные жидкости. [ необходима цитата ] Например, неполярный гексан гораздо менее вязкий, чем полярная вода. Однако размер молекулы является гораздо более сильным фактором вязкости, чем полярность, где соединения с более крупными молекулами более вязкие, чем соединения с более мелкими молекулами. [ необходима цитата ] Таким образом, вода (маленькие полярные молекулы) менее вязкая, чем гексадекан (большие неполярные молекулы).

Полярная молекула имеет чистый диполь в результате противоположных зарядов (т. е. имеющих частичные положительные и частичные отрицательные заряды) из полярных связей, расположенных асимметрично. Вода (H 2 O) является примером полярной молекулы, поскольку она имеет небольшой положительный заряд с одной стороны и небольшой отрицательный заряд с другой. Диполи не компенсируют друг друга, что приводит к чистому диполю. Дипольный момент воды зависит от ее состояния. В газовой фазе дипольный момент составляет ≈ 1,86 дебая (D) [11] , тогда как жидкая вода (≈ 2,95 D) [12] и лед (≈ 3,09 D) [13] выше из-за различных водородно-связанных сред. Другие примеры включают сахара (например, сахарозу ), которые имеют много полярных кислородно-водородных (−OH) групп и в целом являются высокополярными.
Если дипольные моменты связи молекулы не компенсируются, молекула является полярной. Например, молекула воды (H 2 O) содержит две полярные связи O−H в изогнутой (нелинейной) геометрии. Дипольные моменты связи не компенсируются, так что молекула образует молекулярный диполь с отрицательным полюсом на кислороде и положительным полюсом посередине между двумя атомами водорода. На рисунке каждая связь соединяет центральный атом O с отрицательным зарядом (красный) с атомом H с положительным зарядом (синий).
Молекула фтороводорода , HF, полярна благодаря полярным ковалентным связям – в ковалентной связи электроны смещены в сторону более электроотрицательного атома фтора.

Аммиак , NH 3 , представляет собой молекулу, три связи N−H которой имеют лишь незначительную полярность (в сторону более электроотрицательного атома азота). Молекула имеет два неподеленных электрона на орбитали, которая направлена в сторону четвертой вершины приблизительно правильного тетраэдра, как предсказывает теория VSEPR . Эта орбиталь не участвует в ковалентной связи; она богата электронами, что приводит к мощному диполю по всей молекуле аммиака.

В молекулах озона (O 3 ) две связи O−O неполярны (нет разницы в электроотрицательности между атомами одного и того же элемента). Однако распределение других электронов неравномерно — поскольку центральный атом должен делить электроны с двумя другими атомами, но каждый из внешних атомов должен делить электроны только с одним другим атомом, центральный атом более лишен электронов, чем другие (центральный атом имеет формальный заряд +1, в то время как внешние атомы имеют формальный заряд − 1 ⁄ 2 ). Поскольку молекула имеет изогнутую геометрию, результатом является диполь по всей молекуле озона.
Молекула может быть неполярной либо при равном распределении электронов между двумя атомами двухатомной молекулы, либо из-за симметричного расположения полярных связей в более сложной молекуле. Например, трифторид бора (BF 3 ) имеет тригональное плоское расположение трех полярных связей под углом 120°. Это приводит к отсутствию общего диполя в молекуле.

Углекислый газ (CO2 ) имеет две полярные связи C=O, но геометрия CO2 линейна , так что дипольные моменты двух связей компенсируются, и нет чистого молекулярного дипольного момента; молекула неполярна.
Примерами бытовых неполярных соединений являются жиры, масла и бензин.
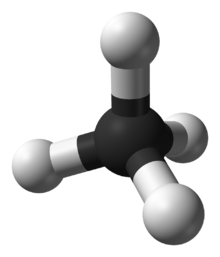
В молекуле метана (CH 4 ) четыре связи C−H расположены тетраэдрически вокруг атома углерода. Каждая связь имеет полярность (хотя и не очень сильную). Связи расположены симметрично, поэтому в молекуле нет общего диполя. Двухатомная молекула кислорода (O 2 ) не имеет полярности в ковалентной связи из-за равной электроотрицательности, поэтому в молекуле нет полярности.
Большие молекулы, которые имеют один конец с присоединенными полярными группами, а другой конец с неполярными группами, описываются как амфифилы или амфифильные молекулы. Они являются хорошими поверхностно-активными веществами и могут способствовать образованию стабильных эмульсий или смесей воды и жиров. Поверхностно-активные вещества снижают поверхностное натяжение между маслом и водой, адсорбируясь на границе раздела жидкость-жидкость.
Определение точечной группы — полезный способ предсказать полярность молекулы. В общем случае молекула не будет обладать дипольным моментом, если отдельные дипольные моменты связей молекулы компенсируют друг друга. Это происходит потому, что дипольные моменты являются евклидовыми векторными величинами с величиной и направлением, и два равных вектора, которые противоположны друг другу, компенсируют друг друга.
Любая молекула с центром инверсии («i») или горизонтальной зеркальной плоскостью («σ h ») не будет обладать дипольными моментами. Аналогично, молекула с более чем одной осью вращения C n не будет обладать дипольным моментом, поскольку дипольные моменты не могут лежать более чем в одном измерении . Вследствие этого ограничения все молекулы с диэдральной симметрией (D n ) не будут обладать дипольным моментом, поскольку, по определению, точечные группы D имеют две или несколько осей C n .
Поскольку точечные группы C 1 , C s ,C ∞h C n и C n v не имеют центра инверсии, горизонтальных зеркальных плоскостей или нескольких осей C n , молекулы в одной из этих точечных групп будут иметь дипольный момент.
Вопреки распространенному заблуждению, электрическое отклонение струи воды от заряженного объекта не основано на полярности. Отклонение происходит из-за электрически заряженных капель в струе, которые индуцирует заряженный объект. Струя воды также может быть отклонена в однородном электрическом поле, которое не может оказывать силу на полярные молекулы. Кроме того, после того, как струя воды заземлена, она больше не может быть отклонена. Слабое отклонение возможно даже для неполярных жидкостей. [14]