В органической химии кольцевая деформация — это тип нестабильности, который возникает, когда связи в молекуле образуют аномальные углы . Деформация чаще всего обсуждается для небольших колец, таких как циклопропаны и циклобутаны , внутренние углы которых существенно меньше идеализированного значения примерно 109 °. Из-за их высокой деформации теплота сгорания этих маленьких колец повышена. [1] [2]
Кольцевая деформация возникает в результате сочетания угловой деформации , конформационной деформации или деформации Питцера (торсионное затмевающее взаимодействие) и трансаннулярной деформации , также известной как деформация Ван-дер-Ваальса или деформация Прелога . Простейшими примерами угловой деформации являются небольшие циклоалканы, такие как циклопропан и циклобутан.
Энергию деформации кольца можно объяснить энергией, необходимой для искажения связей и валентных углов, чтобы замкнуть кольцо. [3]
Считается, что энергия деформации кольца является причиной ускорения скорости изменения кольцевых реакций. Его взаимодействие с традиционными энергиями связи изменяет энтальпии соединений, влияя на кинетику и термодинамику реакций деформации кольца. [4]
Теория кольцевой деформации была впервые разработана немецким химиком Адольфом фон Байером в 1890 году. Раньше считалось, что единственными связями, которые существуют, были крутильная и стерическая; однако теория Байера стала основана на взаимодействии между двумя штаммами.
Теория Байера была основана на предположении, что соединения с кольцами плоские. Позже, примерно в то же время, Герман Заксе сформировал постулат о том, что составные кольца не являются плоскими и потенциально существуют в виде «кресла». Эрнст Мор позже объединил две теории, чтобы объяснить стабильность шестичленных колец и их частоту в природе, а также энергетические уровни других кольцевых структур. [5]
В алканах оптимальное перекрытие атомных орбиталей достигается при 109,5°. Наиболее распространенные циклические соединения имеют в кольце пять или шесть атомов углерода. [6] Адольф фон Байер получил Нобелевскую премию в 1905 году за открытие теории деформации Байера, которая объясняла относительную стабильность циклических молекул в 1885 году. [6]
Угловая деформация возникает, когда валентные углы отклоняются от идеальных валентных углов для достижения максимальной прочности связи в определенной химической конформации . Угловая деформация обычно влияет на циклические молекулы, которым не хватает гибкости ациклических молекул.
Угловая деформация дестабилизирует молекулу, что проявляется в более высокой реакционной способности и повышенной теплоте сгорания . Максимальная прочность связи является результатом эффективного перекрытия атомных орбиталей в химической связи . Количественной мерой угловой деформации является энергия деформации . Угловая деформация и деформация кручения в совокупности создают кольцевую деформацию, которая влияет на циклические молекулы. [6]
Нормированные энергии, позволяющие сравнивать деформации колец, получают путем измерения молярной теплоты сгорания в циклоалканах на метиленовую группу (СН 2 ). [6]
Значение 658,6 кДж на моль получено для ненапряженного длинноцепочечного алкана. [6]
Циклоалканы обычно имеют меньшую деформацию кольца, чем циклоалкены, что видно при сравнении циклопропана и циклопропена. [8]
Циклические алкены подвержены деформации, возникающей в результате искажения sp 2 -гибридизированных углеродных центров. Показательным является C 60 , где углеродные центры имеют пирамидальную форму. Это искажение повышает реакционную способность этой молекулы. Угловая деформация также является основой правила Бредта, которое предписывает, чтобы центральные углеродные центры не включались в алкены, поскольку образующийся алкен будет подвергаться экстремальной угловой деформации.
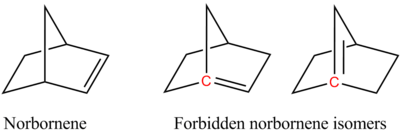
Маленькие транс-циклоалкены имеют настолько большую деформацию кольца, что не могут существовать в течение длительных периодов времени. [9] Например, самый маленький транс-циклоалкан, который был выделен, — это транс-циклооктен . Транс-циклогептен был обнаружен с помощью спектрофотометрии за минимальные периоды времени, а транс-циклогексен считается промежуточным продуктом в некоторых реакциях. Транс-циклоалкены меньшего размера не известны. Напротив, хотя небольшие цис-циклоалкены действительно имеют кольцевую деформацию, они имеют гораздо меньшую кольцевую деформацию, чем небольшие транс-циклоалкены. [9]
В общем, повышенный уровень ненасыщенности в алкенах приводит к более высокой деформации кольца. Увеличение ненасыщенности приводит к большей деформации кольца в циклопропене. [8] Таким образом, циклопропен представляет собой алкен, который имеет наибольшую деформацию кольца между двумя упомянутыми. Различные гибридизации и геометрия циклопропена и циклопропана способствуют увеличению деформации кольца. Циклоппен также имеет повышенную угловую деформацию, что также способствует большей деформации кольца. Однако эта тенденция не всегда работает для каждого алкана и алкена. [8]

В некоторых молекулах деформация кручения может способствовать кольцевой деформации в дополнение к угловой деформации. Одним из примеров такой молекулы является циклопропан . Углерод-углеродные связи циклопропана образуют углы 60 °, что далеко от предпочтительного угла 109,5 ° в алканах, поэтому угловая деформация больше всего способствует деформации кольца циклопропана. [10] Однако, как показано в проекции молекулы Ньюмана , атомы водорода затмеваются, что также вызывает некоторую деформацию кручения. [10]
В циклоалканах каждый углерод неполярно ковалентно связан с двумя атомами углерода и двумя атомами водорода. Углероды имеют sp 3- гибридизацию и должны иметь идеальные валентные углы 109,5°. Однако из-за ограничений циклической структуры идеальный угол достигается только в шестиуглеродном кольце — циклогексане в конформации кресла . Для других циклоалканов валентные углы отклоняются от идеальных.
Молекулы с высокой степенью деформации кольца состоят из трех, четырех и некоторых пятичленных колец, в том числе: циклопропаны , циклопропены , циклобутаны , циклобутены , [1,1,1] пропелланы , [2,2,2] пропелланы , эпоксиды. , азиридины , циклопентены и норборнены . Эти молекулы имеют валентные углы между атомами кольца, которые более острые, чем оптимальные тетраэдрические (109,5°) и тригональные плоские (120°) валентные углы , необходимые для их соответствующих связей sp 3 и sp 2 . Из-за меньших валентных углов связи имеют более высокую энергию и принимают больший p-характер, чтобы уменьшить энергию связей. Кроме того, кольцевые структуры циклопропанов/енов и циклклобутанов/енов обладают очень небольшой конформационной гибкостью. Таким образом, заместители атомов кольца существуют в затменной конформации в циклопропанах и между гош и затменной в циклобутанах, способствуя повышению энергии деформации кольца в виде ван-дер-ваальсова отталкивания.
моноциклы
Бициклики [12]
В бициклических системах деформация кольца может быть значительно выше . Например, бициклобутан C 4 H 6 известен как одно из наиболее напряженных соединений, которые можно выделить в больших масштабах; энергия его деформации оценивается в 63,9 ккал/моль ( 267 кДж/моль ) . [13] [14]
Циклоппропан имеет меньшую деформацию кольца, поскольку имеет наименьшее количество ненасыщенности; в результате увеличение степени ненасыщенности приводит к большей деформации кольца. [8] Например, циклопропен имеет большую степень деформации кольца, чем циклопропан, потому что он имеет больше ненасыщенности.
Потенциальная энергия и уникальная структура связи, содержащаяся в связях молекул с кольцевой деформацией, могут быть использованы для управления реакциями в органическом синтезе . Примерами таких реакций являются метатезисная полимеризация с раскрытием кольца , фотоиндуцированное раскрытие кольца циклобутенов и нуклеофильное раскрытие кольца эпоксидов и азиридинов .
Увеличение потенциальной энергии от деформации кольца также можно использовать для увеличения энергии, выделяемой взрывчатыми веществами, или повышения их чувствительности к ударам. [15] Например, ударная чувствительность взрывчатого вещества 1,3,3-тринитроазетидина может частично или в первую очередь объясняться деформацией его кольца. [15]