
Мембранный потенциал (также трансмембранный потенциал или мембранное напряжение ) — это разница электрического потенциала между внутренней и внешней частью биологической клетки . То есть существует разница в энергии, необходимой для перемещения электрических зарядов из внутренней во внешнюю клеточную среду и наоборот, пока не происходит приобретения кинетической энергии или образования излучения. Градиенты концентрации зарядов непосредственно определяют эту потребность в энергии. Для внешней части клетки типичные значения мембранного потенциала, обычно выраженные в милливольтах и обозначаемые как мВ , находятся в диапазоне от –80 мВ до –40 мВ.
Все клетки животных окружены мембраной, состоящей из липидного бислоя со встроенными в него белками . Мембрана служит одновременно изолятором и диффузионным барьером для движения ионов . Трансмембранные белки , также известные как белки -переносчики ионов или белки ионного насоса , активно проталкивают ионы через мембрану и создают градиенты концентрации на мембране, а ионные каналы позволяют ионам перемещаться через мембрану вниз по этим градиентам концентрации. Ионные насосы и ионные каналы электрически эквивалентны набору батарей и резисторов, вставленных в мембрану, и, следовательно, создают напряжение между двумя сторонами мембраны.
Почти все плазматические мембраны имеют электрический потенциал, причем внутренняя часть обычно отрицательная по отношению к внешней. [1] Мембранный потенциал выполняет две основные функции. Во-первых, он позволяет клетке функционировать как батарея, обеспечивая питание для работы различных «молекулярных устройств», встроенных в мембрану. [2] Во-вторых, в электрически возбудимых клетках , таких как нейроны и мышечные клетки , он используется для передачи сигналов между различными частями клетки. Сигналы генерируются путем открытия или закрытия ионных каналов в одной точке мембраны, вызывая локальное изменение мембранного потенциала. Это изменение электрического поля может быть быстро обнаружено соседними или более удаленными ионными каналами в мембране. Эти ионные каналы могут затем открываться или закрываться в результате изменения потенциала, воспроизводя сигнал.
В невозбудимых клетках и в возбудимых клетках в их исходном состоянии мембранный потенциал поддерживается на относительно стабильном значении, называемом потенциалом покоя . Для нейронов потенциал покоя определяется в пределах от –80 до –70 милливольт; то есть внутренняя часть ячейки имеет отрицательное базовое напряжение чуть меньше одной десятой вольта. Открытие и закрытие ионных каналов может вызвать отклонение от потенциала покоя. Это называется деполяризацией, если внутреннее напряжение становится менее отрицательным (скажем, от –70 мВ до –60 мВ) или гиперполяризацией, если внутреннее напряжение становится более отрицательным (скажем, от –70 мВ до –80 мВ). В возбудимых клетках достаточно большая деполяризация может вызвать потенциал действия , при котором мембранный потенциал быстро и значительно меняется в течение короткого времени (порядка от 1 до 100 миллисекунд), часто меняя свою полярность. Потенциалы действия генерируются путем активации определенных потенциалзависимых ионных каналов .
В нейронах факторы, влияющие на мембранный потенциал, разнообразны. Они включают в себя многочисленные типы ионных каналов, некоторые из которых являются химически управляемыми, а некоторые — потенциалзависимыми. Поскольку потенциалзависимые ионные каналы контролируются мембранным потенциалом, в то время как мембранный потенциал сам по себе находится под влиянием этих же ионных каналов, возникают петли обратной связи, которые обеспечивают сложную временную динамику, включая колебания и регенеративные события, такие как потенциалы действия.
Мембранный потенциал в клетке в конечном итоге зависит от двух факторов: электрической силы и диффузии. Электрическая сила возникает в результате взаимного притяжения частиц с противоположными электрическими зарядами (положительных и отрицательных) и взаимного отталкивания частиц с одинаковым типом заряда (положительных или обоих отрицательных). Диффузия возникает в результате статистической тенденции частиц перераспределяться из областей, где они высоко сконцентрированы, в области с низкой концентрацией.
Напряжение, которое является синонимом разницы электрических потенциалов , представляет собой способность пропускать электрический ток через сопротивление. Действительно, самое простое определение напряжения дается законом Ома : V=IR, где V — напряжение, I — ток, а R — сопротивление. Если в электрическую цепь включен источник напряжения, например батарея, то чем выше напряжение источника, тем большую силу тока он будет пропускать через доступное сопротивление. Функциональное значение напряжения заключается только в разности потенциалов между двумя точками цепи. Идея напряжения в одной точке бессмысленна. В электронике принято присваивать нулевое напряжение некоторому произвольно выбранному элементу схемы, а затем присваивать напряжения для других элементов, измеряемые относительно этой нулевой точки. Не имеет значения, какой элемент выбран в качестве нулевой точки — функция цепи зависит только от разностей, а не от напряжений как таковых . Однако в большинстве случаев по соглашению нулевой уровень чаще всего присваивается той части цепи, которая находится в контакте с землей.
Тот же принцип применим к напряжению в клеточной биологии. В электрически активной ткани разность потенциалов между любыми двумя точками можно измерить, вставив электрод в каждую точку, например, один внутри и один снаружи клетки, и подключив оба электрода к выводам того, что по сути является специализированным вольтметром. По соглашению, нулевое значение потенциала присваивается внешней стороне клетки, а знак разности потенциалов между внешней и внутренней частью определяется потенциалом внутренней части относительно внешнего нуля.
С математической точки зрения определение напряжения начинается с понятия электрического поля E , векторного поля, задающего величину и направление каждой точке пространства. Во многих ситуациях электрическое поле является консервативным полем , а это означает , что его можно выразить как градиент скалярной функции V , то есть E = –∇ V. Это скалярное поле V называется распределением напряжения. Определение допускает произвольную константу интегрирования, поэтому абсолютные значения напряжения не имеют смысла. В общем, электрические поля можно рассматривать как консервативные только в том случае, если магнитные поля не оказывают на них существенного влияния, но это условие обычно хорошо применимо и к биологическим тканям.
Поскольку электрическое поле представляет собой градиент распределения напряжения, быстрые изменения напряжения в небольшой области подразумевают сильное электрическое поле; и наоборот, если напряжение остается примерно одинаковым на большой области, электрические поля в этой области должны быть слабыми. Сильное электрическое поле, эквивалентное сильному градиенту напряжения, означает, что на любые заряженные частицы, находящиеся в этой области, действует сильная сила.
Электрические сигналы внутри биологических организмов, как правило, управляются ионами . [4] Наиболее важными катионами для потенциала действия являются натрий (Na + ) и калий (K + ). [5] Оба они являются одновалентными катионами, несущими один положительный заряд. Потенциалы действия также могут включать кальций (Ca 2+ ), [6] который представляет собой двухвалентный катион, несущий двойной положительный заряд. Хлорид - анион (Cl- ) играет важную роль в потенциалах действия некоторых водорослей , [7] , но играет незначительную роль в потенциалах действия большинства животных. [8]
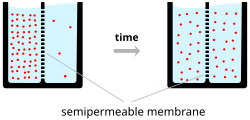
Ионы пересекают клеточную мембрану под двумя воздействиями: диффузией и электрическими полями . Простой пример, когда два раствора — A и B — разделены пористым барьером, показывает, что диффузия гарантирует, что они в конечном итоге смешаются в равные растворы. Такое смешивание происходит из-за разницы их концентраций. Область с высокой концентрацией будет диффундировать в область с низкой концентрацией. В целях расширения примера предположим, что раствор А содержит 30 ионов натрия и 30 ионов хлорида. Также пусть раствор Б содержит только 20 ионов натрия и 20 ионов хлорида. Если предположить, что барьер позволяет проходить через него ионам обоих типов, то будет достигнуто устойчивое состояние, при котором оба раствора будут содержать 25 ионов натрия и 25 ионов хлорида. Однако если пористый барьер избирательно пропускает ионы, то сама по себе диффузия не будет определять конечный результат. Возвращаясь к предыдущему примеру, построим теперь барьер, проницаемый только для ионов натрия. Теперь только натрию разрешено диффундировать через барьер от его более высокой концентрации в растворе A к более низкой концентрации в растворе B. Это приведет к большему накоплению ионов натрия, чем ионов хлорида в растворе B, и меньшему количеству ионов натрия, чем ионы натрия. хлорид-ионы в растворе А.
Это означает, что в растворе B имеется суммарный положительный заряд из-за более высокой концентрации положительно заряженных ионов натрия, чем отрицательно заряженных ионов хлорида. Аналогичным образом, в растворе А имеется суммарный отрицательный заряд из-за большей концентрации отрицательных ионов хлорида, чем положительных ионов натрия. Поскольку противоположные заряды притягиваются, а подобные отталкиваются, на ионы теперь также влияют электрические поля, а также силы диффузии. Следовательно, положительные ионы натрия с меньшей вероятностью попадут в теперь более положительный раствор B и останутся в теперь более отрицательном растворе A. Точка, в которой силы электрического поля полностью противодействуют силе диффузии, называется равновесным потенциалом. В этот момент чистый поток конкретного иона (в данном случае натрия) равен нулю.

Каждая клетка окружена плазматической мембраной , которая имеет структуру липидного бислоя , в который встроено множество типов крупных молекул. Поскольку плазматическая мембрана состоит из молекул липидов, она по своей природе обладает высоким электрическим сопротивлением, другими словами, низкой собственной проницаемостью для ионов. Однако некоторые молекулы, внедренные в мембрану, способны либо активно транспортировать ионы с одной стороны мембраны на другую, либо обеспечивать каналы, по которым они могут перемещаться. [9]
В электрической терминологии плазматическая мембрана функционирует как комбинированный резистор и конденсатор . Сопротивление возникает из-за того, что мембрана препятствует движению зарядов через нее. Емкость возникает из-за того, что липидный бислой настолько тонкий, что скопление заряженных частиц на одной стороне приводит к возникновению электрической силы, которая притягивает противоположно заряженные частицы к другой стороне. На емкость мембраны относительно не влияют внедренные в нее молекулы, поэтому она имеет более или менее инвариантную величину, оцениваемую в 2 мкФ/см 2 (общая емкость участка мембраны пропорциональна его площади). С другой стороны, проводимость чистого липидного бислоя настолько низка, что в биологических ситуациях в ней всегда доминирует проводимость альтернативных путей, обеспечиваемых встроенными молекулами. Таким образом, емкость мембраны более или менее постоянна, а вот сопротивление сильно варьируется.
Толщина плазматической мембраны оценивается примерно в 7-8 нанометров. Поскольку мембрана очень тонкая, для создания внутри нее сильного электрического поля не требуется очень большого трансмембранного напряжения. Типичные мембранные потенциалы в клетках животных составляют порядка 100 милливольт (то есть одна десятая вольта), но расчеты показывают, что это создает электрическое поле, близкое к максимальному, которое может выдержать мембрана. Разница, намного превышающая 200 милливольт, может вызвать пробой диэлектрика , то есть искрение на мембране.
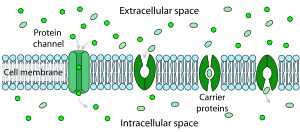
Сопротивление чистого липидного бислоя прохождению через него ионов очень велико, но структуры, встроенные в мембрану, могут значительно усиливать движение ионов, активно или пассивно , посредством механизмов, называемых облегченным транспортом и облегченной диффузией . Два типа структур, которые играют наибольшую роль, — это ионные каналы и ионные насосы , оба обычно образуются из скоплений белковых молекул. Ионные каналы обеспечивают проходы, по которым могут перемещаться ионы. В большинстве случаев ионный канал проницаем только для определенных типов ионов (например, натрия и калия, но не для хлорида или кальция), а иногда проницаемость варьируется в зависимости от направления движения ионов. Ионные насосы, также известные как переносчики ионов или белки-переносчики, активно транспортируют определенные типы ионов с одной стороны мембраны на другую, иногда используя для этого энергию, полученную в результате метаболических процессов.
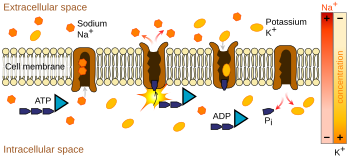
Ионные насосы представляют собой интегральные мембранные белки , которые осуществляют активный транспорт , т. е. используют клеточную энергию (АТФ) для «перекачки» ионов против градиента их концентрации. [10] Такие ионные насосы забирают ионы с одной стороны мембраны (снижая там их концентрацию) и высвобождают их с другой стороны (увеличивая там их концентрацию).
Ионный насос, наиболее соответствующий потенциалу действия, — это натриево-калиевый насос , который транспортирует три иона натрия из клетки и два иона калия внутрь. [11] [12] Как следствие, концентрация ионов калия K + внутри клетки концентрация натрия примерно в 30 раз больше, чем внешняя концентрация, тогда как концентрация натрия снаружи примерно в пять раз больше, чем внутри. [12] [13] [14] Аналогичным образом другие ионы имеют разные концентрации внутри и снаружи нейрона, например, кальций , хлорид и магний . [14]
Если бы количество ионов каждого типа было равным, натриево-калиевый насос был бы электрически нейтральным, но из-за обмена три к двум он обеспечивает чистое перемещение одного положительного заряда от внутриклеточного к внеклеточному за каждый цикл. тем самым способствуя положительной разности напряжений. Насос имеет три эффекта: (1) он повышает концентрацию натрия во внеклеточном пространстве и снижает во внутриклеточном пространстве; (2) повышает концентрацию калия во внутриклеточном пространстве и снижает во внеклеточном пространстве; (3) он придает внутриклеточному пространству отрицательное напряжение по отношению к внеклеточному пространству.
Натриево-калиевый насос работает относительно медленно. Если бы ячейка была инициализирована с одинаковыми концентрациями натрия и калия повсюду, насосу потребовались бы часы, чтобы установить равновесие. Насос работает постоянно, но его эффективность становится все менее эффективной по мере снижения концентрации натрия и калия, доступных для перекачки.
Ионные насосы влияют на потенциал действия только путем установления относительного соотношения внутриклеточных и внеклеточных концентраций ионов. Потенциал действия включает главным образом открытие и закрытие ионных каналов, а не ионных насосов. Если ионные насосы отключить, удалив их источник энергии или добавив ингибитор, такой как уабаин , аксон все равно может генерировать сотни тысяч потенциалов действия, прежде чем их амплитуды начнут значительно уменьшаться. [10] В частности, ионные насосы не играют существенной роли в реполяризации мембраны после потенциала действия. [5]
Еще одним функционально важным ионным насосом является натрий-кальциевый обменник . Этот насос работает концептуально аналогично натрий-калиевому насосу, за исключением того, что в каждом цикле он обменивает три Na + из внеклеточного пространства на один Ca ++ из внутриклеточного пространства. Поскольку чистый поток заряда направлен внутрь, этот насос фактически работает «под гору» и, следовательно, не требует какого-либо источника энергии, кроме напряжения на мембране. Его наиболее важным эффектом является выкачивание кальция наружу; он также обеспечивает приток натрия внутрь, тем самым противодействуя натрий-калиевому насосу, но, поскольку общие концентрации натрия и калия намного выше, чем концентрации кальция, этот эффект относительно неважен. Конечным результатом работы натрий-кальциевого обменника является то, что в состоянии покоя внутриклеточная концентрация кальция становится очень низкой.

Ионные каналы представляют собой интегральные мембранные белки с порами, через которые ионы могут перемещаться между внеклеточным пространством и внутренней частью клетки. Большинство каналов специфичны (селективны) для одного иона; например, большинство калиевых каналов характеризуются соотношением селективности в отношении калия по сравнению с натрием 1000:1, хотя ионы калия и натрия имеют одинаковый заряд и лишь незначительно различаются по своему радиусу. Пора канала обычно настолько мала, что ионы должны проходить через нее в порядке одного файла. [16] Поры каналов могут быть открытыми или закрытыми для прохождения ионов, хотя ряд каналов демонстрируют различные уровни субпроводимости. Когда канал открыт, ионы проникают через поры канала вниз по трансмембранному градиенту концентрации для этого конкретного иона. Скорость ионного потока через канал, т.е. амплитуда одноканального тока, определяется максимальной проводимостью канала и электрохимической движущей силой для этого иона, которая представляет собой разницу между мгновенным значением мембранного потенциала и значением обратного потенциала . [17]
Канал может иметь несколько различных состояний (соответствующих разным конформациям белка), но каждое такое состояние является либо открытым, либо закрытым. В целом закрытые состояния соответствуют либо сжатию поры, делающему ее непроходимой для иона, либо отдельной части белка, закупоривающей пору. Например, потенциалзависимый натриевый канал подвергается инактивации , при которой часть белка попадает в пору, закрывая ее. [18] Эта инактивация отключает ток натрия и играет решающую роль в потенциале действия.
Ионные каналы можно классифицировать по тому, как они реагируют на окружающую среду. [19] Например, ионные каналы, участвующие в формировании потенциала действия, являются чувствительными к напряжению каналами ; они открываются и закрываются в ответ на напряжение на мембране. Лиганд-зависимые каналы образуют еще один важный класс; эти ионные каналы открываются и закрываются в ответ на связывание молекулы- лиганда , например нейромедиатора . Другие ионные каналы открываются и закрываются под действием механических сил. Другие ионные каналы, например каналы сенсорных нейронов , открываются и закрываются в ответ на другие стимулы, такие как свет, температура или давление.
Каналы утечки представляют собой простейший тип ионных каналов, поскольку их проницаемость более или менее постоянна. Наибольшее значение в нейронах имеют каналы утечки, калиевые и хлоридные каналы. Даже они не являются совершенно постоянными по своим свойствам: во-первых, большинство из них зависят от напряжения в том смысле, что они проводят лучше в одном направлении, чем в другом (другими словами, они являются выпрямителями ); во-вторых, некоторые из них способны блокироваться химическими лигандами, даже если для их работы лиганды не требуются.
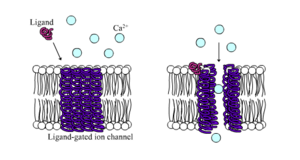
Лиганд-управляемые ионные каналы — это каналы, проницаемость которых значительно увеличивается, когда какой-либо тип химического лиганда связывается со структурой белка. Клетки животных содержат сотни, если не тысячи их типов. Большая их часть выполняет функцию рецепторов нейромедиаторов — они встречаются в постсинаптических участках, и химический лиганд, который их воротает, высвобождается пресинаптическим окончанием аксона . Одним из примеров этого типа является рецептор AMPA , рецептор нейромедиатора глутамата , который при активации обеспечивает прохождение ионов натрия и калия. Другим примером является рецептор ГАМК А , рецептор нейромедиатора ГАМК , который при активации позволяет проходить ионам хлорида.
Рецепторы нейромедиаторов активируются лигандами, которые появляются во внеклеточной области, но существуют и другие типы лиганд-управляемых каналов, которые контролируются взаимодействиями на внутриклеточной стороне.
Потенциал-управляемые ионные каналы , также известные как потенциал-зависимые ионные каналы , представляют собой каналы, на проницаемость которых влияет мембранный потенциал. Они образуют еще одну очень большую группу, каждый член которой имеет определенную ионную селективность и определенную зависимость от напряжения. Многие из них также зависят от времени — другими словами, они реагируют на изменение напряжения не сразу, а только после задержки.
Одним из наиболее важных членов этой группы является тип потенциалзависимых натриевых каналов, лежащих в основе потенциалов действия. Их иногда называют натриевыми каналами Ходжкина-Хаксли, поскольку первоначально они были охарактеризованы Аланом Ллойдом Ходжкином и Эндрю Хаксли в их работе, получившей Нобелевскую премию. исследования физиологии потенциала действия. Канал закрывается при уровне напряжения покоя, но резко открывается, когда напряжение превышает определенный порог, обеспечивая большой приток ионов натрия, что приводит к очень быстрому изменению мембранного потенциала. Восстановление после потенциала действия частично зависит от типа потенциалзависимого калиевого канала, который закрывается на уровне напряжения покоя, но открывается вследствие большого изменения напряжения, возникающего во время потенциала действия.
Обратный потенциал (или равновесный потенциал ) иона — это значение трансмембранного напряжения, при котором диффузионные и электрические силы уравновешиваются, так что нет чистого потока ионов через мембрану. Это означает, что трансмембранное напряжение точно противодействует силе диффузии иона, так что чистый ток иона через мембрану равен нулю и неизменен. Обратный потенциал важен, поскольку он создает напряжение, которое действует на каналы, проницаемые для этого иона, — другими словами, он дает напряжение, которое генерирует градиент концентрации ионов, когда он действует как батарея .
Равновесный потенциал конкретного иона обычно обозначается обозначением E ion . Равновесный потенциал для любого иона можно рассчитать с помощью уравнения Нернста . [20] Например, обратимый потенциал для ионов калия будет следующим:
где
Даже если два разных иона имеют одинаковый заряд (т. е. K + и Na + ), они все равно могут иметь очень разные равновесные потенциалы, при условии, что их внешняя и/или внутренняя концентрации различаются. Возьмем, к примеру, равновесные потенциалы калия и натрия в нейронах. Равновесный потенциал калия E K составляет -84 мВ при 5 мМ калия снаружи и 140 мМ внутри. С другой стороны, равновесный потенциал натрия E Na составляет примерно +66 мВ с примерно 12 мМ натрия внутри и 140 мМ снаружи. [примечание 1]
Мембранный потенциал покоя нейрона фактически меняется в ходе развития организма . Чтобы нейрон в конечном итоге смог полностью реализовать свою взрослую функцию, его потенциал должен жестко регулироваться во время развития. По мере развития организма мембранный потенциал покоя становится более отрицательным. [21] Глиальные клетки также дифференцируются и пролиферируют по мере развития мозга . [22] Добавление этих глиальных клеток увеличивает способность организма регулировать внеклеточный калий . Падение внеклеточного калия может привести к снижению мембранного потенциала на 35 мВ. [23]
Возбудимость клеток — это изменение мембранного потенциала, необходимое для клеточных реакций в различных тканях. Возбудимость клеток — это свойство, которое индуцируется во время раннего эмбриогенеза. [24] Возбудимость клетки также определяется как легкость, с которой может быть вызван ответ. [25] Потенциалы покоя и пороговые потенциалы составляют основу возбудимости клеток, и эти процессы имеют основополагающее значение для генерации градуированных потенциалов и потенциалов действия.
Наиболее важными регуляторами возбудимости клеток являются концентрации внеклеточных электролитов (т.е. Na + , K + , Ca2 + , Cl- , Mg2 + ) и связанных с ними белков. Важными белками, которые регулируют возбудимость клеток, являются потенциалзависимые ионные каналы , транспортеры ионов (например, Na+/K+-АТФаза , транспортеры магния , кислотно-основные транспортеры ), мембранные рецепторы и активируемые гиперполяризацией циклические нуклеотидные каналы . [26] Например, калиевые каналы и кальций-чувствительные рецепторы являются важными регуляторами возбудимости в нейронах , сердечных миоцитах и многих других возбудимых клетках, таких как астроциты . [27] Ион кальция также является наиболее важным вторичным мессенджером в передаче сигналов возбудимых клеток . Активация синаптических рецепторов инициирует длительные изменения возбудимости нейронов. [28] Гормоны щитовидной железы , надпочечников и другие гормоны также регулируют возбудимость клеток, например, прогестерон и эстроген модулируют возбудимость гладкомышечных клеток миометрия .
Считается, что многие типы клеток имеют возбудимую мембрану. Возбудимые клетки — это нейроны, мышцы ( сердечные , скелетные , гладкие ), эндотелиальные клетки сосудов , перициты , юкстагломерулярные клетки , интерстициальные клетки Кахаля , многие типы эпителиальных клеток (например , бета-клетки , альфа-клетки , дельта-клетки , энтероэндокринные клетки , легочные нейроэндокринные клетки) . , пинеалоциты ), глиальные клетки (например, астроциты), механорецепторные клетки (например, волосковые клетки и клетки Меркеля ), хеморецепторные клетки (например, гломусные клетки , вкусовые рецепторы ), некоторые растительные клетки и, возможно, иммунные клетки . [29] Астроциты проявляют форму неэлектрической возбудимости, основанную на внутриклеточных вариациях кальция, связанных с экспрессией нескольких рецепторов, посредством которых они могут обнаруживать синаптический сигнал. В нейронах в некоторых частях клетки имеются разные свойства мембран, например, дендритная возбудимость наделяет нейроны способностью обнаруживать совпадения пространственно разделенных входных сигналов. [30]
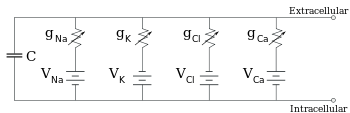
Электрофизиологи моделируют эффекты различий в концентрации ионов, ионных каналов и емкости мембраны с точки зрения эквивалентной схемы , которая предназначена для представления электрических свойств небольшого участка мембраны. Эквивалентная схема состоит из конденсатора, включенного параллельно с четырьмя дорожками, каждый из которых состоит из последовательно включенной батареи с переменной проводимостью. Емкость определяется свойствами липидного бислоя и считается постоянной. Каждый из четырех параллельных путей исходит от одного из основных ионов: натрия, калия, хлорида и кальция. Напряжение каждого ионного пути определяется концентрацией ионов на каждой стороне мембраны; см. раздел «Потенциал разворота» выше. Проводимость каждого ионного пути в любой момент времени определяется состояниями всех ионных каналов, которые потенциально проницаемы для этого иона, включая каналы утечки, лиганд-управляемые каналы и потенциал-управляемые ионные каналы.
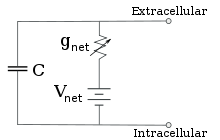
Для фиксированных концентраций ионов и фиксированных значений проводимости ионного канала эквивалентную схему можно свести, используя уравнение Гольдмана, как описано ниже, к схеме, содержащей емкость параллельно с батареей и проводимостью. В электрическом плане это разновидность RC-цепи (резистивно-емкостной цепи), и ее электрические свойства очень просты. Начиная с любого начального состояния, ток, текущий через проводимость или емкость, затухает с экспоненциальным ходом времени, с постоянной времени τ = RC , где C — емкость мембранного участка, а R = 1/ g net чистое сопротивление. В реальных ситуациях постоянная времени обычно находится в диапазоне 1–100 миллисекунд. В большинстве случаев изменения проводимости ионных каналов происходят в более быстром временном масштабе, поэтому RC-цепь не является хорошим приближением; однако дифференциальное уравнение, используемое для моделирования мембранного участка, обычно представляет собой модифицированную версию уравнения RC-цепи.
Когда мембранный потенциал клетки в течение длительного периода времени существенно не меняется, его называют потенциалом покоя или напряжением покоя. Этот термин используется для обозначения мембранного потенциала невозбудимых клеток, а также мембранного потенциала возбудимых клеток в отсутствие возбуждения. В возбудимых клетках другими возможными состояниями являются градуированные мембранные потенциалы (переменной амплитуды) и большие потенциалы действия, повышающие мембранный потенциал по принципу «все или ничего», которые обычно следуют фиксированному временному графику. Возбудимые клетки включают нейроны , мышечные клетки и некоторые секреторные клетки желез . Однако даже в других типах клеток мембранное напряжение может претерпевать изменения в ответ на внешние или внутриклеточные стимулы. Например, деполяризация плазматической мембраны, по-видимому, является важным шагом в запрограммированной гибели клеток . [31]
Взаимодействия, генерирующие потенциал покоя, моделируются уравнением Гольдмана . [32] По форме оно похоже на уравнение Нернста, показанное выше, поскольку оно основано на зарядах рассматриваемых ионов, а также на разнице между их внутренней и внешней концентрацией. Однако он также учитывает относительную проницаемость плазматической мембраны для каждого рассматриваемого иона.
Три иона, которые появляются в этом уравнении, — это калий (K + ), натрий (Na + ) и хлорид (Cl — ). Кальций не используется, но его можно добавить в ситуациях, в которых он играет значительную роль. [33] Поскольку хлоридные термины являются анионами, их трактуют иначе, чем катионные; внутриклеточная концентрация указана в числителе, а внеклеточная концентрация - в знаменателе, обратном катионным членам. Pi означает относительную проницаемость иона типа i .
По сути, формула Гольдмана выражает мембранный потенциал как средневзвешенное значение реверсивных потенциалов для отдельных типов ионов, взвешенных по проницаемости. (Хотя мембранный потенциал изменяется примерно на 100 мВ во время потенциала действия, концентрации ионов внутри и снаружи клетки изменяются незначительно. Они остаются близкими к соответствующим концентрациям, когда мембрана находится в состоянии покоя.) В большинстве животных клеток проницаемость для калия в состоянии покоя значительно выше, чем проницаемость для натрия. Как следствие, потенциал покоя обычно близок к потенциалу обращения калия. [34] [35] Проницаемость для хлоридов может быть достаточно высокой, чтобы быть значительной, но, в отличие от других ионов, хлорид не перекачивается активно и поэтому уравновешивается при обратном потенциале, очень близком к потенциалу покоя, определяемому другими ионами.
Значения мембранного потенциала покоя в большинстве клеток животных обычно варьируются от потенциала обращения калия (обычно около -80 мВ) до около -40 мВ. Потенциал покоя в возбудимых клетках (способных создавать потенциалы действия) обычно составляет около -60 мВ - более деполяризованные напряжения могут привести к спонтанной генерации потенциалов действия. Незрелые или недифференцированные клетки демонстрируют сильно варьирующие значения напряжения покоя, обычно значительно более положительные, чем в дифференцированных клетках. [36] В таких клетках значение потенциала покоя коррелирует со степенью дифференцировки: недифференцированные клетки в некоторых случаях могут вообще не демонстрировать никакой разницы трансмембранного напряжения.
Поддержание потенциала покоя может быть метаболически дорогостоящим для клетки из-за необходимости активной перекачки ионов для противодействия потерям из-за каналов утечки. Цена самая высокая, когда функция клетки требует особенно деполяризованного значения мембранного напряжения. Например, потенциал покоя адаптированных к дневному свету фоторецепторов мясной мухи ( Calliphora vicina ) может достигать -30 мВ. [37] Этот повышенный мембранный потенциал позволяет клеткам очень быстро реагировать на зрительные сигналы; Цена заключается в том, что поддержание потенциала покоя может потреблять более 20% общего клеточного АТФ . [38]
С другой стороны, высокий потенциал покоя в недифференцированных клетках не обязательно влечет за собой высокие метаболические затраты. Этот очевидный парадокс разрешается путем изучения происхождения потенциала покоя. Малодифференцированные клетки характеризуются чрезвычайно высоким входным сопротивлением [36] , что означает, что на этой стадии жизни клетки имеется мало каналов утечки. В результате проницаемость для калия становится аналогичной проницаемости для ионов натрия, что помещает потенциал покоя между обратными потенциалами для натрия и калия, как обсуждалось выше. Снижение токов утечки также означает, что для компенсации не требуется активной накачки, а значит, и низкие метаболические затраты.
Как объяснялось выше, потенциал в любой точке клеточной мембраны определяется разницей в концентрации ионов между внутриклеточными и внеклеточными областями, а также проницаемостью мембраны для каждого типа ионов. Концентрации ионов обычно не меняются очень быстро (за исключением Ca 2+ , где базовая внутриклеточная концентрация настолько низка, что даже небольшой приток может увеличить ее на порядки), но проницаемость ионов может меняться в доли миллисекунды в результате активации лиганд-управляемых ионных каналов. Изменение мембранного потенциала может быть большим или малым, в зависимости от того, сколько ионных каналов активировано и какого они типа, а также может быть длительным или коротким, в зависимости от продолжительности времени, в течение которого каналы остаются открытыми. Изменения этого типа называются градуированными потенциалами , в отличие от потенциалов действия, которые имеют фиксированную амплитуду и временной ход.
Как можно вывести из уравнения Гольдмана, показанного выше, эффект увеличения проницаемости мембраны для иона определенного типа смещает мембранный потенциал в сторону обратимого потенциала для этого иона. Таким образом, открытие Na + -каналов смещает мембранный потенциал в сторону реверсивного потенциала Na + , который обычно составляет около +100 мВ. Аналогично, открытие каналов K + сдвигает мембранный потенциал примерно в сторону –90 мВ, а открытие каналов Cl– сдвигает его примерно в сторону –70 мВ (потенциал покоя большинства мембран). Таким образом, Na + -каналы смещают мембранный потенциал в положительную сторону, K + -каналы смещают его в отрицательную сторону (кроме случаев, когда мембрана гиперполяризована до значения, более отрицательного, чем K + -реверсивный потенциал), а Cl -- каналы имеют тенденцию смещать его в отрицательную сторону. это к потенциалу покоя.

Градуированные мембранные потенциалы особенно важны в нейронах , где они производятся синапсами — временное изменение мембранного потенциала, вызванное активацией синапса одним градуированным потенциалом или потенциалом действия, называется постсинаптическим потенциалом . Нейромедиаторы , которые действуют, открывая каналы Na + , обычно заставляют мембранный потенциал становиться более положительным, тогда как нейротрансмиттеры, которые активируют каналы K + , обычно заставляют его становиться более отрицательным; те, кто блокирует эти каналы, имеют тенденцию иметь противоположный эффект.
Считается ли постсинаптический потенциал возбуждающим или тормозящим, зависит от потенциала разворота ионов этого тока и порога срабатывания клеткой потенциала действия (около –50 мВ). Постсинаптический ток с реверсивным потенциалом выше порога, такой как типичный ток Na + , считается возбуждающим. Ток с реверсивным потенциалом ниже порогового, такой как типичный ток К + , считается тормозящим. Ток с реверсивным потенциалом выше потенциала покоя, но ниже порогового, сам по себе не вызывает потенциалы действия, но вызывает подпороговые колебания мембранного потенциала . Таким образом, нейромедиаторы, которые действуют, открывая каналы Na + , производят возбуждающие постсинаптические потенциалы , или ВПСП, тогда как нейромедиаторы, которые действуют, открывая каналы K + или Cl- , обычно производят тормозные постсинаптические потенциалы , или ТПСП. Когда несколько типов каналов открыты в течение одного и того же периода времени, их постсинаптические потенциалы суммируются (суммируются).
С точки зрения биофизики мембранный потенциал покоя — это просто мембранный потенциал, возникающий в результате проницаемости мембраны, которая преобладает, когда клетка отдыхает. Приведенное выше уравнение средневзвешенных значений применимо всегда, но следующий подход легче визуализировать. В любой момент времени для иона существуют два фактора, которые определяют, какое влияние этот ион окажет на мембранный потенциал клетки:
Если движущая сила велика, ион «проталкивается» через мембрану. Если проницаемость высока, иону будет легче диффундировать через мембрану.
Итак, в покоящейся мембране, хотя движущая сила для калия невелика, ее проницаемость очень высока. Натрий обладает огромной движущей силой, но почти не обладает проницаемостью в состоянии покоя. В этом случае калий проводит примерно в 20 раз больший ток, чем натрий, и, таким образом, оказывает в 20 раз большее влияние на Эм , чем натрий.
Однако рассмотрим другой случай — пик потенциала действия. Здесь проницаемость для Na высокая, а проницаемость для K относительно низкая. Таким образом, мембрана перемещается в сторону E Na и вдаль от EK .
Чем больше ионов проникает, тем сложнее становится предсказать мембранный потенциал. Однако это можно сделать с помощью уравнения Гольдмана-Ходжкина-Каца или уравнения взвешенных средних. Подставив градиенты концентрации и проницаемости ионов в любой момент времени, можно определить мембранный потенциал в этот момент. Уравнения GHK означают, что в любой момент значение мембранного потенциала будет представлять собой средневзвешенное значение равновесных потенциалов всех проникающих ионов. «Вес» представляет собой относительную проницаемость ионов через мембрану.
В то время как клетки тратят энергию на транспортировку ионов и создание трансмембранного потенциала, они, в свою очередь, используют этот потенциал для транспортировки других ионов и метаболитов, таких как сахар. Трансмембранный потенциал митохондрий стимулирует выработку АТФ , которая является общей валютой биологической энергии.
Клетки могут использовать энергию, которую они хранят в потенциале покоя, для запуска потенциалов действия или других форм возбуждения. Эти изменения мембранного потенциала обеспечивают связь с другими клетками (как и потенциалы действия) или инициируют изменения внутри клетки, что происходит в яйцеклетке, когда она оплодотворяется сперматозоидом .
Изменения диэлектрических свойств плазматической мембраны могут служить признаком таких заболеваний, как диабет и дислипидемия. [39]
В нейрональных клетках потенциал действия начинается с притока ионов натрия в клетку через натриевые каналы, что приводит к деполяризации, тогда как восстановление включает выброс калия наружу через калиевые каналы. Оба эти потока возникают путем пассивной диффузии .
Доза соли может заставить все еще работающие нейроны свежего куска мяса активироваться, вызывая мышечные спазмы. [40] [41] [42] [43] [44]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )