Амальгама натрия с общей формулой Na(Hg) представляет собой сплав ртути и натрия . Термин «амальгама» используется для обозначения сплавов, интерметаллических соединений и растворов (как твердых, так и жидких), содержащих ртуть в качестве основного компонента. Амальгамы натрия часто используются в реакциях как сильные восстановители с лучшими эксплуатационными характеристиками по сравнению с твердым натрием. Они менее опасно реагируют с водой и фактически часто используются в виде водной суспензии.
Амальгама натрия использовалась в качестве реагента еще в 1862 году. [1] Метод синтеза был описан Дж. Альфредом Ванклином в 1866 году. [2]
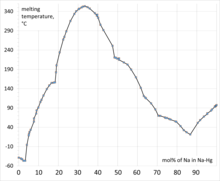
Никакой конкретной формулы «амальгаме натрия» не присвоено. Na 5 Hg 8 и Na 3 Hg являются четко определенными соединениями. В амальгамах натрия расстояния Hg-Hg увеличиваются примерно до 5 Å по сравнению с примерно 3 Å для самой ртути. [3] Обычно амальгамы классифицируют по весовому проценту натрия. Амальгамы с 2% Na при комнатной температуре являются твердыми веществами, тогда как некоторые более разбавленные амальгамы остаются жидкими. [4]
Металлический натрий растворяется в ртути экзотермически , т. е. с выделением тепла, поэтому образование амальгамы натрия опасно искрообразованием. [5] Этот процесс вызывает локальное кипение ртути, и по этой причине образование обычно проводится в вытяжном шкафу и часто выполняется с использованием безвоздушных методов , таких как синтез в безводном жидком парафине. Амальгаму натрия можно получить в лаборатории растворением металлического натрия в ртути или наоборот. [6] [7] [8] Амальгамы натрия можно приобрести в магазинах химической продукции.
Амальгама натрия использовалась в органической химии как мощный восстановитель , обращаться с которым безопаснее, чем с самим натрием. Он используется при деградации Эмде , а также для восстановления ароматических кетонов до гидролов. [9]
В конструкции натриевой лампы высокого давления используется амальгама натрия , обеспечивающая натрий для получения нужного цвета и ртуть для настройки электрических характеристик лампы.
Амальгама натрия — побочный продукт хлора , получаемый электролизом в ртутных элементах . В этой ячейке рассол (концентрированный раствор хлорида натрия ) подвергается электролизу между жидким ртутным катодом и титановым или графитовым анодом . Хлор образуется на аноде, а натрий, образующийся на катоде, растворяется в ртути, образуя амальгаму натрия. Обычно эта амальгама натрия отводится и подвергается реакции с водой в «ячейке разложения» с образованием газообразного водорода, концентрированного раствора гидроксида натрия и ртути, которые подлежат вторичной переработке в процессе. В принципе, вся ртуть должна быть полностью переработана, но небольшая ее часть неизбежно теряется. Из-за опасений по поводу утечки этой ртути в окружающую среду процесс ртутных элементов обычно заменяется установками, в которых используется менее токсичный катод.
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ); Сборник томов , т. 2, с. 607.{{cite book}}: |journal=игнорируется ( помощь ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ); Сборник томов , т. 8, с. 479.