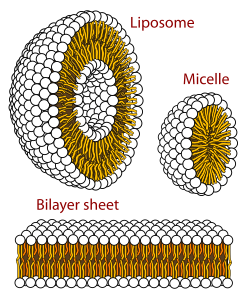
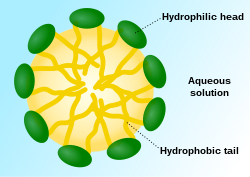
Мицелла ( / m aɪ ˈ s ɛ l / ) или мицелла ( / m aɪ ˈ s ɛ l ə / ) ( мн. мицеллы или мицеллы соответственно) представляет собой совокупность (или супрамолекулярную сборку ) поверхностно-активных амфипатических липидных молекул, диспергированных в жидкость, образующая коллоидную суспензию (также известную как ассоциированная коллоидная система). [4] Типичная мицелла в воде образует агрегат с гидрофильными «головными» областями при контакте с окружающим растворителем , изолируя гидрофобные однохвостые области в центре мицеллы.
Эта фаза вызвана поведением упаковки однохвостых липидов в бислое . Трудность заполнения внутреннего объема бислоя при одновременном учете площади, приходящейся на одну головную группу, навязанную молекуле гидратацией головной группы липида, приводит к образованию мицеллы. Этот тип мицелл известен как мицелла нормальной фазы (или мицелла масло в воде). Обратные мицеллы имеют головные группы в центре с выступающими наружу хвостами (мицелла «вода в масле»).
Мицеллы имеют приблизительно сферическую форму. Возможны также другие формы, такие как эллипсоиды, цилиндры и бислои. Форма и размер мицеллы зависят от молекулярной геометрии ее молекул поверхностно-активного вещества и условий растворения, таких как концентрация поверхностно-активного вещества, температура , pH и ионная сила . Процесс образования мицелл известен как мицеллизация и является частью фазового поведения многих липидов в соответствии с их полиморфизмом . [5]
Способность мыльного раствора действовать как моющее средство была признана на протяжении веков. Однако только в начале двадцатого века состав таких растворов был научно изучен. Пионерскую работу в этой области провел Джеймс Уильям Макбейн в Бристольском университете . Еще в 1913 году он постулировал существование «коллоидных ионов», чтобы объяснить хорошую электролитическую проводимость растворов пальмитата натрия . [6] Эти высокомобильные, спонтанно образующиеся кластеры стали называть мицеллами — термин, заимствованный из биологии и популяризированный Г.С. Хартли в его классической книге « Соли парафиновой цепи: исследование образования мицелл ». [7] Термин мицелла был придуман в научной литературе девятнадцатого века как уменьшительное от латинского слова mica (частица), что означает новое слово, обозначающее «крошечную частицу». [8]
Отдельные молекулы ПАВ , находящиеся в системе, но не входящие в состав мицеллы, называются « мономерами ». Мицеллы представляют собой молекулярную сборку , в которой отдельные компоненты термодинамически находятся в равновесии с мономерами того же вида в окружающей среде. В воде гидрофильные «головки» молекул ПАВ всегда контактируют с растворителем, независимо от того, существуют ли ПАВ в виде мономеров или в составе мицеллы. Однако липофильные «хвосты» молекул ПАВ в составе мицеллы меньше контактируют с водой, что является основой энергетического движения мицеллообразования. В мицелле гидрофобные хвосты нескольких молекул ПАВ собираются в маслоподобное ядро, наиболее устойчивая форма которого не имеет контакта с водой. Напротив, мономеры поверхностно-активных веществ окружены молекулами воды, которые создают «клетку» или сольватную оболочку, соединенную водородными связями . Эта водная клетка похожа на клатрат , имеет ледоподобную кристаллическую структуру и может быть охарактеризована по гидрофобному эффекту. Степень растворимости липидов определяется неблагоприятным вкладом энтропии из-за упорядочения структуры воды в соответствии с гидрофобным эффектом.
Мицеллы, состоящие из ионных поверхностно-активных веществ, обладают электростатическим притяжением к ионам, которые их окружают в растворе, последние известны как противоионы . Хотя ближайшие противоионы частично маскируют заряженную мицеллу (до 92%), влияние заряда мицеллы влияет на структуру окружающего растворителя на значительных расстояниях от мицеллы. Ионные мицеллы влияют на многие свойства смеси, в том числе на ее электропроводность. Добавление солей к коллоидным мицеллам может уменьшить силу электростатических взаимодействий и привести к образованию более крупных ионных мицелл. [9] Точнее это видно с точки зрения эффективного заряда при гидратации системы.
Мицеллы образуются только тогда, когда концентрация поверхностно-активного вещества превышает критическую концентрацию мицелл (ККМ), а температура системы превышает критическую температуру мицелл или температуру Крафта . Образование мицелл можно понять с помощью термодинамики : Мицеллы могут образовываться спонтанно из-за баланса между энтропией и энтальпией . В воде гидрофобный эффект является движущей силой мицеллообразования, несмотря на то, что сборка молекул ПАВ невыгодна как с точки зрения энтальпии, так и с точки зрения энтропии системы. При очень низких концентрациях ПАВ в растворе присутствуют только мономеры. По мере увеличения концентрации поверхностно-активного вещества достигается точка, в которой неблагоприятный вклад энтропии, возникающий из-за кластеризации гидрофобных хвостов молекул, преодолевается увеличением энтропии из-за высвобождения сольватных оболочек вокруг хвостов поверхностно-активного вещества. В этот момент липидные хвосты части поверхностно-активных веществ должны отделиться от воды. Следовательно, они начинают образовывать мицеллы. В широком смысле, выше ККМ потеря энтропии из-за сборки молекул поверхностно-активного вещества меньше, чем прирост энтропии за счет освобождения молекул воды, которые были «захвачены» сольватными оболочками мономеров поверхностно-активного вещества. Также важны энтальпийные соображения, такие как электростатические взаимодействия, которые происходят между заряженными частями поверхностно-активных веществ.
Уравнение параметра упаковки мицелл используется, чтобы помочь «предсказать молекулярную самосборку в растворах поверхностно-активных веществ»: [10]
где – объем хвоста ПАВ, – длина хвоста, – равновесная площадь, приходящаяся на молекулу на поверхности агрегата.
Концепция мицелл была введена для описания агрегатов ядро-корона небольших молекул поверхностно-активных веществ , однако она также распространилась на описание агрегатов амфифильных блок-сополимеров в селективных растворителях. [11] [12] Важно знать разницу между этими двумя системами. Основное различие между этими двумя типами агрегатов заключается в размере их строительных блоков. Молекулы поверхностно-активных веществ имеют молекулярную массу , которая обычно составляет несколько сотен граммов на моль, тогда как блок-сополимеры обычно на один или два порядка больше. Более того, благодаря более крупным гидрофильным и гидрофобным частям блок-сополимеры могут иметь гораздо более выраженную амфифильную природу по сравнению с молекулами ПАВ.
Из-за этих различий в строительных блоках некоторые мицеллы блок-сополимеров ведут себя как мицеллы поверхностно-активных веществ, а другие - нет. Поэтому необходимо различать эти две ситуации. Первые будут принадлежать к динамическим мицеллам , а вторые будут называться кинетически замороженными мицеллами.
Некоторые мицеллы амфифильных блок-сополимеров ведут себя аналогично мицеллам поверхностно-активных веществ. Их обычно называют динамическими мицеллами, и они характеризуются теми же процессами релаксации, что и обмен поверхностно-активных веществ и разрыв/рекомбинация мицелл. Хотя процессы релаксации в мицеллах двух типов одинаковы, кинетика обмена унимеров сильно различается. В то время как в системах поверхностно-активных веществ унимеры покидают мицеллы и присоединяются к ним посредством процесса, контролируемого диффузией , для сополимеров константа скорости проникновения медленнее, чем в процессе, контролируемом диффузией. Установлено, что скорость этого процесса представляет собой убывающую по степенному закону степень полимеризации гидрофобного блока в степени 2/3. Это различие обусловлено скручиванием гидрофобного блока сополимера, выходящего из ядра мицеллы. [13]
Блок-сополимеры, образующие динамические мицеллы , при правильных условиях являются одними из триблочных полоксамеров .
Когда мицеллы блок-сополимера не проявляют характерных процессов релаксации мицелл поверхностно-активных веществ, их называют кинетически замороженными мицеллами . Этого можно достичь двумя способами: когда унимеры, образующие мицеллы, не растворяются в растворителе раствора мицелл, или если блоки, образующие ядро, являются стекловидными при температуре, при которой находятся мицеллы. Кинетически замороженные мицеллы образуются при выполнении любого из этих условий. Особым примером, в котором справедливы оба этих условия, является полистирол-b-поли(этиленоксид). Этот блок-сополимер характеризуется высокой гидрофобностью блока, образующего ядро, PS , что делает унимеры нерастворимыми в воде. Кроме того, ПС имеет высокую температуру стеклования , которая в зависимости от молекулярной массы выше комнатной температуры. Благодаря этим двум характеристикам водный раствор мицелл ПС-ПЭО достаточно высокой молекулярной массы можно считать кинетически замороженным. Это означает, что ни один из процессов релаксации, которые могли бы привести раствор мицеллы к термодинамическому равновесию, невозможен. [14] Новаторскую работу над этими мицеллами провел Ади Айзенберг. [15] Было также показано, что отсутствие процессов релаксации дает большую свободу в возможных формируемых морфологиях. [16] [17] Более того, устойчивость к разбавлению и широкий диапазон морфологии кинетически замороженных мицелл делают их особенно интересными, например, для разработки наночастиц с длинной циркуляцией для доставки лекарств. [18]
В неполярном растворителе воздействие гидрофильных головных групп на окружающий растворитель энергетически невыгодно и приводит к образованию системы вода в масле. В этом случае гидрофильные группы секвестрируются в ядре мицеллы, а гидрофобные группы отходят от центра. Эти обратные мицеллы пропорционально менее склонны образовываться при увеличении заряда головной группы, поскольку гидрофильная секвестрация может создать крайне неблагоприятные электростатические взаимодействия.
Хорошо известно, что для многих систем поверхностно-активное вещество/растворитель небольшая часть обратных мицелл самопроизвольно приобретает суммарный заряд +q e или -q e . Эта зарядка происходит по механизму диспропорционирования/сопропорционирования, а не по механизму диссоциации/ассоциации, и константа равновесия для этой реакции составляет порядка от 10 -4 до 10 -11 , что означает примерно от 1 из 100 до 1 из 100 000 мицелл. будет заряжено. [19]

Супермицелла — это иерархическая мицеллярная структура ( супрамолекулярная сборка ), в которой отдельные компоненты также являются мицеллами. Супермицеллы образуются с помощью химических подходов снизу вверх , таких как самосборка длинных цилиндрических мицелл в радиальные крестообразные, звездчатые или одуванчиковые структуры в специально выбранном растворителе; в раствор можно добавлять твердые наночастицы , которые будут действовать как центры зародышеобразования и образовывать центральное ядро супермицеллы. Стебли первичных цилиндрических мицелл состоят из различных блок- сополимеров , соединенных прочными ковалентными связями ; внутри структуры супермицеллы они слабо удерживаются вместе за счет водородных связей , электростатических или сольвофобных взаимодействий. [20] [21]
Когда поверхностно-активные вещества присутствуют выше критической концентрации мицелл (ККМ), они могут действовать как эмульгаторы , которые позволяют растворить соединение, которое обычно нерастворимо (в используемом растворителе). Это происходит потому, что нерастворимые частицы могут быть включены в ядро мицеллы, которое само растворяется в объеме растворителя благодаря благоприятному взаимодействию головных групп с частицами растворителя. Наиболее распространенным примером этого явления являются моющие средства , которые очищают плохо растворимые липофильные материалы (такие как масла и воски), которые невозможно удалить одной водой. Моющие средства очищают также за счет снижения поверхностного натяжения воды, что облегчает удаление материала с поверхности. Эмульгирующее свойство ПАВ также является основой эмульсионной полимеризации .
Мицеллы также могут играть важную роль в химических реакциях. Мицеллярная химия использует внутреннюю часть мицелл для проведения химических реакций, что в некоторых случаях может сделать более возможным многостадийный химический синтез . [22] [23] Это может увеличить выход реакции, создать условия, более благоприятные для конкретных продуктов реакции (например, гидрофобных молекул), а также уменьшить количество необходимых растворителей, побочных продуктов и требуемых условий (например, экстремальный pH). Из-за этих преимуществ мицеллюлярная химия считается формой зеленой химии . [24] Однако образование мицелл может также ингибировать химические реакции, например, когда реагирующие молекулы образуют мицеллы, которые защищают молекулярный компонент, уязвимый для окисления. [25]
Использование катионных мицелл хлорида цетримония , хлорида бензетония и хлорида цетилпиридиния позволяет ускорить химические реакции между отрицательно заряженными соединениями (такими как ДНК или коэнзим А ) в водной среде до 5 миллионов раз. [26] В отличие от обычного мицеллярного катализа, [27] реакции происходят исключительно на поверхности заряженных мицелл.
Образование мицелл необходимо для всасывания жирорастворимых витаминов и сложных липидов в организме человека. Соли желчных кислот , образующиеся в печени и секретируемые желчным пузырем, позволяют образовываться мицеллам жирных кислот. Это позволяет абсорбировать сложные липиды (например, лецитин) и жирорастворимые витамины (A, D, E и K) в мицеллах тонкой кишки.
В процессе свертывания молока протеазы действуют на растворимую часть казеина , κ-казеин , создавая нестабильное мицеллярное состояние, которое приводит к образованию сгустков.
Мицеллы также можно использовать для адресной доставки лекарств в виде наночастиц золота. [28]