Коэнзим А ( CoA , SHCoA , CoASH ) — кофермент , играющий важную роль в синтезе и окислении жирных кислот , а также окислении пирувата в цикле лимонной кислоты . Все геномы , секвенированные на сегодняшний день, кодируют ферменты, которые используют кофермент А в качестве субстрата , и около 4% клеточных ферментов используют его (или тиоэфир ) в качестве субстрата. У человека биосинтез КоА требует цистеина , пантотената (витамина B 5 ) и аденозинтрифосфата (АТФ). [2]
В своей ацетильной форме коэнзим А представляет собой очень универсальную молекулу, выполняющую метаболические функции как на анаболическом , так и на катаболическом пути. Ацетил-КоА используется в посттрансляционной регуляции и аллостерической регуляции пируватдегидрогеназы и карбоксилазы для поддержания и поддержки разделения синтеза и деградации пирувата . [3]

Коэнзим А был идентифицирован Фрицем Липманом в 1946 году [4] , который позже и дал ему свое название. Его структура была определена в начале 1950-х годов в Институте Листера в Лондоне совместно Липманном и другими сотрудниками Гарвардской медицинской школы и Массачусетской больницы общего профиля . [5] Липманн первоначально намеревался изучить перенос ацетила на животных, и в результате этих экспериментов он заметил уникальный фактор, который не присутствовал в экстрактах ферментов, но был очевиден во всех органах животных. Ему удалось выделить и очистить этот фактор из печени свиньи и обнаружить, что его функция связана с коферментом, который активно участвует в ацетилировании холина. [6] Работа с Беверли Жирар , Натаном Капланом и другими определила, что пантотеновая кислота является центральным компонентом кофермента А. [7] [8] Коэнзим был назван коэнзимом А, что означает «активация ацетата». В 1953 году Фриц Липманн получил Нобелевскую премию по физиологии и медицине «за открытие кофермента А и его значения для промежуточного метаболизма». [6] [9]
Коэнзим А естественным образом синтезируется из пантотената (витамина В 5 ), который содержится в таких продуктах, как мясо, овощи, зерновые, бобовые, яйца и молоко. [10] В организме человека и большинства живых организмов пантотенат является важным витамином, выполняющим множество функций. [11] В некоторых растениях и бактериях, включая Escherichia coli , пантотенат может синтезироваться de novo и поэтому не считается незаменимым. Эти бактерии синтезируют пантотенат из аминокислоты аспартата и метаболита при биосинтезе валина. [12]
Во всех живых организмах коэнзим А синтезируется в пятиэтапном процессе, для которого требуются четыре молекулы АТФ, пантотената и цистеина [13] (см. рисунок):

Сокращения номенклатуры ферментов в скобках обозначают ферменты млекопитающих, других эукариот и прокариот соответственно. У млекопитающих этапы 4 и 5 катализируются бифункциональным ферментом COASY . [14] Этот путь регулируется ингибированием продукта. КоА является конкурентным ингибитором пантотенаткиназы, которая в норме связывает АТФ. [12] Коэнзим А, три АДФ, один монофосфат и один дифосфат образуются в результате биосинтеза. [13]
Коэнзим А может синтезироваться альтернативными путями, когда внутриклеточный уровень кофермента А снижается и путь de novo нарушается. [15] В этих путях коэнзим А должен поступать из внешнего источника, например, из пищи, чтобы производить 4'-фосфопантетеин . Эктонуклеотидпирофосфаты (ENPP) расщепляют кофермент А до 4'-фосфопантетеина, стабильной молекулы в организмах. Ацильные белки-переносчики (ACP) (такие как ACP-синтаза и деградация ACP) также используются для производства 4'-фосфопантетеина. Этот путь позволяет пополнять запасы 4'-фосфопантетеина в клетке и превращать его в кофермент А посредством ферментов PPAT и PPCK. [16]
В статье 2024 года подробно описан вероятный механизм химического синтеза пантеинового компонента (основной функциональной части) коэнзима А в первозданном пребиотическом мире.
Коэнзим А производится в промышленных масштабах путем экстракции из дрожжей, однако это неэффективный процесс (выход примерно 25 мг/кг), в результате чего продукт получается дорогой. Были исследованы различные способы синтетического или полусинтетического производства КоА, хотя ни один из них в настоящее время не работает в промышленном масштабе. [17]
Поскольку коэнзим А с химической точки зрения является тиолом , он может реагировать с карбоновыми кислотами с образованием тиоэфиров , действуя таким образом как переносчик ацильной группы. Он помогает переносить жирные кислоты из цитоплазмы в митохондрии . Молекулу кофермента А, несущую ацильную группу, также называют ацил-КоА . Когда он не связан с ацильной группой, его обычно называют «CoASH» или «HSCoA». Этот процесс облегчает выработку в клетках жирных кислот, которые необходимы для структуры клеточных мембран.
Коэнзим А также является источником фосфопантетеиновой группы, которая добавляется в качестве простетической группы к белкам, таким как ациловый белок-носитель и формилтетрагидрофолатдегидрогеназа . [18] [19]
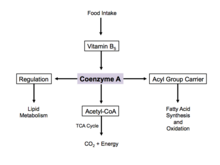
Коэнзим А является одним из пяти важнейших коферментов, которые необходимы в механизме реакции цикла лимонной кислоты . Его форма ацетил-кофермента А является основным вкладом в цикл лимонной кислоты и получается в результате гликолиза , метаболизма аминокислот и бета-окисления жирных кислот. Этот процесс является основным катаболическим путем организма и необходим для разрушения строительных блоков клетки, таких как углеводы , аминокислоты и липиды . [20]
При избытке глюкозы кофермент А используется в цитозоле для синтеза жирных кислот. [21] Этот процесс реализуется путем регуляции ацетил-КоА-карбоксилазы , которая катализирует обязательную стадию синтеза жирных кислот. Инсулин стимулирует ацетил-КоА-карбоксилазу, а адреналин и глюкагон ингибируют ее активность. [22]
Во время клеточного голодания синтезируется коэнзим А, который транспортирует жирные кислоты из цитозоля в митохондрии. Здесь ацетил-КоА генерируется для окисления и производства энергии. [21] В цикле лимонной кислоты коэнзим А действует как аллостерический регулятор, стимулируя фермент пируватдегидрогеназу .
Открытие новой антиоксидантной функции коэнзима А подчеркивает его защитную роль во время клеточного стресса. Клетки млекопитающих и бактерий , подвергнутые окислительному и метаболическому стрессу, демонстрируют значительное увеличение ковалентной модификации белковых остатков цистеина коферментом А. роль белка S -глутатионилирования путем предотвращения необратимого окисления тиоловой группы остатков цистеина.
Используя антитела против коэнзима А [25] и методологии жидкостной хроматографии и тандемной масс-спектрометрии ( ЖХ-МС/МС ), более 2000 коалатированных белков были идентифицированы из стрессированных клеток млекопитающих и бактерий. [26] Большинство этих белков участвуют в клеточном метаболизме и реакции на стресс. [26] Различные исследования были сосредоточены на расшифровке регуляции белков, опосредованной коферментом А. Сообщается , что при коаляции белка ингибируется каталитическая активность различных белков (например, супрессора метастазов NME1 , пероксиредоксина 5 , GAPDH и других). [27] [28] [24] [29] В восстановлении активности белка важную роль играют антиоксидантные ферменты, восстанавливающие дисульфидную связь между коферментом А и остатком цистеина в белке. Этот процесс называется декоаляцией белка. На данный момент показано, что два бактериальных белка, тиоредоксин А и тиоредоксин-подобный белок (YtpP), декоалатируют белки. [30]
Коэнзим А доступен у различных поставщиков химикатов в виде свободной кислоты и солей лития или натрия . Свободная кислота коэнзима А заметно нестабильна: деградация около 5% наблюдается через 6 месяцев при хранении при -20 °C [1] и почти полная деградация через 1 месяц при 37 °C. [31] Литиевые и натриевые соли КоА более стабильны, при этом наблюдается незначительная деградация в течение нескольких месяцев при различных температурах. [32] Водные растворы коэнзима А нестабильны при pH выше 8, при этом 31% активности теряется через 24 часа при 25 ° C и pH 8. Исходные растворы КоА относительно стабильны при замораживании при pH 2–6. Основным путем потери активности КоА, вероятно, является окисление КоА воздухом до дисульфидов КоА. Смешанные дисульфиды КоА, такие как КоА- S - S -глутатион, обычно являются примесями в коммерческих препаратах КоА. [1] Свободный КоА можно регенерировать из дисульфида КоА и смешанных дисульфидов КоА с помощью восстановителей, таких как дитиотреитол или 2-меркаптоэтанол .