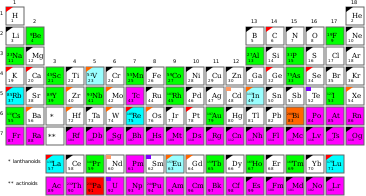
Моноизотопный элемент — это элемент, который имеет только один стабильный изотоп (нуклид). Всего таких элементов, как указано, 26.
Стабильность химических элементов определяется экспериментально, так как существует ряд стабильных нуклидов с атомными номерами более ~ 40, которые теоретически нестабильны, но, по-видимому, имеют настолько длительный период полураспада, что они не наблюдались ни прямо, ни косвенно (по измерению продуктов ) распадаться.
Моноизотопные элементы характеризуются, за исключением одного случая, нечетным числом протонов (нечетное Z ) и четным числом нейтронов. Из-за выигрыша энергии от спаривания ядер нечетное число протонов придает нестабильность изотопам с нечетным Z , что в более тяжелых элементах требует полностью спаренного набора нейтронов, чтобы компенсировать эту тенденцию к стабильности. (Пять стабильных нуклидов с нечетным Z и нечетным числом нейтронов — это водород-2, литий-6, бор-10, азот-14 и тантал-180m1.)
Единственным моноизотопным исключением из правила нечетного Z является бериллий; его единственный стабильный первичный изотоп бериллий-9 имеет 4 протона и 5 нейтронов. Этот элемент не может иметь стабильный изотоп с равным количеством нейтронов и протонов ( бериллий-8 , по 4 каждого) из-за его нестабильности по отношению к альфа-распаду , которому благоприятствует чрезвычайно сильная связь ядер гелия-4 . Наличие стабильного изотопа с 4 протонами и 6 нейтронами не позволяется из-за очень большого несоответствия соотношения протонов/нейтронов для такого легкого элемента. (Тем не менее, период полураспада бериллия-10 составляет 1,36 миллиона лет, что слишком мало, чтобы быть первичным , но все же указывает на необычную стабильность для легкого изотопа с таким дисбалансом.)
Набор моноизотопных элементов перекрывается, но не совпадает с набором из 21 мононуклидного элемента , которые характеризуются наличием по существу только одного изотопа (нуклида), встречающегося в природе. [1] Причиной этого является появление в природе некоторых долгоживущих радиоактивных первичных нуклидов , которые могут образовывать примеси с моноизотопами и, таким образом, мешать им быть естественными мононуклидами. Это происходит в случае семи моноизотопных элементов. Эти изотопы моноизотопны, но из-за присутствия долгоживущего радиоактивного первичного нуклида не являются мононуклидными. Этими элементами являются ванадий , рубидий , индий , лантан , европий , лютеций и рений . Что касается индия и рения, то долгоживущий радионуклид фактически является наиболее распространенным изотопом в природе, а стабильный изотоп менее распространен.
В двух дополнительных случаях ( висмут [2] и протактиний ) изначально встречаются мононуклидные элементы, которые не являются моноизотопными, поскольку встречающийся в природе нуклид радиоактивен, и, следовательно, элемент вообще не имеет стабильных изотопов. Чтобы элемент был моноизотопным, он должен иметь один стабильный нуклид.
Немононуклидные элементы отмечены звездочкой и указан долгоживущий первичный радиоизотоп . В двух случаях (индий и рений) наиболее распространенным в природе изотопом является слаборадиоактивный, а в случае европия - почти половина его.