Неон — химический элемент ; он имеет символ Ne и атомный номер 10. Это второй благородный газ в периодической таблице. [13] Неон — бесцветный, не имеющий запаха, инертный одноатомный газ при стандартных условиях , плотность которого составляет примерно две трети плотности воздуха.
Неон был открыт в 1898 году вместе с криптоном и ксеноном , идентифицирован как один из трех оставшихся редких инертных элементов в сухом воздухе после удаления азота , кислорода , аргона и углекислого газа . Его открытие было отмечено отличительным ярко-красным спектром излучения, который он продемонстрировал, что привело к его немедленному признанию в качестве нового элемента. Название неон происходит от греческого слова νέον , средней формы единственного числа от νέος ( neos ), что означает «новый». Неон — химически инертный газ , не имеющий известных незаряженных соединений неона. Существующие соединения неона в основном представляют собой ионные молекулы или хрупкие молекулы, удерживаемые вместе силами Ван-дер-Ваальса .
Синтез большей части неона в космосе произошел в результате ядерного синтеза внутри звезд кислорода и гелия посредством процесса альфа-захвата . Несмотря на его обильное присутствие во Вселенной и Солнечной системе — занимая пятое место по распространенности в космосе после водорода, гелия, кислорода и углерода — неон сравнительно редок на Земле. Он составляет около 18,2 ppm объема атмосферы Земли и меньшую долю в земной коре. Высокая летучесть неона и его неспособность образовывать соединения, которые бы прикрепляли его к твердым телам, объясняют его ограниченное присутствие на Земле и внутренних планетах земной группы . Высокая летучесть неона способствовала его выходу из планетезималей под воздействием тепла зарождающегося Солнца ранней Солнечной системы.
Известные применения неона включают его использование в низковольтных неоновых лампах свечения , высоковольтных разрядных трубках и неоновых рекламных вывесках , где он излучает отчетливое красновато-оранжевое свечение. [14] [15] Эта же красная линия излучения отвечает за характерный красный свет гелий-неоновых лазеров . Хотя неон имеет некоторые применения в плазменных трубках и в качестве хладагента, его коммерческое использование относительно ограничено. Его в основном получают путем фракционной перегонки жидкого воздуха , что делает его значительно более дорогим, чем гелий, поскольку воздух является его единственным источником.

Неон был открыт в 1898 году британскими химиками сэром Уильямом Рамзаем (1852–1916) и Моррисом Трэверсом (1872–1961) в Лондоне . [16] Неон был открыт, когда Рамзай охладил образец воздуха до тех пор, пока он не стал жидкостью, затем нагрел жидкость и захватил газы по мере их испарения. Газы азот , кислород и аргон были идентифицированы, но остальные газы были выделены примерно в порядке их распространенности в течение шестинедельного периода, начавшегося в конце мая 1898 года. Первым оставшимся газом, который был идентифицирован, был криптон ; следующим, после того как криптон был удален, был газ, который давал яркий красный свет при спектроскопическом разряде. Этот газ, идентифицированный в июне, был назван «неон», греческим аналогом латинского novum («новый») [17], предложенным сыном Рамзая. Характерный яркий красно-оранжевый цвет, испускаемый газообразным неоном при электрическом возбуждении, был отмечен немедленно. Трэверс позже писал: «Вспышка малинового света из трубки рассказывала свою собственную историю и была зрелищем, которое заставляло вспоминать и никогда не забывать». [18]
Второй газ также был обнаружен вместе с неоном, имея примерно такую же плотность, как аргон, но с другим спектром – Рамсей и Трэверс назвали его метаргоном . [19] [20] Однако последующий спектроскопический анализ показал, что это аргон, загрязненный оксидом углерода . Наконец, та же группа открыла ксенон тем же способом в сентябре 1898 года. [19]
Дефицит неона помешал его быстрому применению для освещения по типу трубок Мура , которые использовали азот и были коммерциализированы в начале 1900-х годов. После 1902 года компания Жоржа Клода Air Liquide производила промышленные количества неона как побочного продукта его бизнеса по сжижению воздуха. В декабре 1910 года Клод продемонстрировал современное неоновое освещение на основе запаянной неоновой трубки. Клод некоторое время пытался продавать неоновые трубки для внутреннего домашнего освещения из-за их интенсивности, но рынок потерпел неудачу, потому что домовладельцы возражали против цвета. В 1912 году партнер Клода начал продавать неоновые разрядные трубки в качестве привлекательных рекламных вывесок и сразу же добился большего успеха. Неоновые трубки были представлены в США в 1923 году с двумя большими неоновыми вывесками, купленными автосалоном Packard в Лос-Анджелесе. Свечение и приковывающий внимание красный цвет сделали неоновую рекламу совершенно отличной от конкурентов. [21] Интенсивный цвет и яркость неона соответствовали американскому обществу того времени, предполагая «столетие прогресса» и превращая города в сенсационные новые среды, наполненные сияющей рекламой и «электрографической архитектурой». [22] [23]
Неон сыграл свою роль в базовом понимании природы атомов в 1913 году, когда Дж. Дж. Томсон , в рамках своего исследования состава канальных лучей , направил потоки ионов неона через магнитное и электрическое поле и измерил отклонение потоков с помощью фотографической пластины. Томсон наблюдал два отдельных пятна света на фотографической пластине (см. изображение), что предполагало две различные параболы отклонения. В конечном итоге Томсон пришел к выводу, что некоторые из атомов в неоновом газе имели большую массу, чем остальные. Хотя в то время Томсон этого не понимал, это было первое открытие изотопов стабильных атомов . Устройство Томсона было грубой версией прибора, который мы теперь называем масс-спектрометром .

Неон имеет три стабильных изотопа : 20 Ne (90,48%), 21 Ne (0,27%) и 22 Ne (9,25%). [24]
21 Ne и 22 Ne являются частично первичными и частично нуклеогенными (т.е. образованными ядерными реакциями других нуклидов с нейтронами или другими частицами в окружающей среде), и их вариации в естественном содержании хорошо изучены. Напротив, 20 Ne (главный первичный изотоп, образованный в звездном нуклеосинтезе ) не известен как нуклеогенный или радиогенный , за исключением распада кислорода-20 , который образуется в очень редких случаях распада кластера тория -228 . Таким образом, причины вариации 20 Ne на Земле были предметом горячих споров. [25] [26]
Основные ядерные реакции, генерирующие нуклеогенные изотопы неона, начинаются с 24 Mg и 25 Mg, которые производят 21 Ne и 22 Ne соответственно, после захвата нейтрона и немедленного испускания альфа -частицы . Нейтроны , которые производят реакции, в основном производятся вторичными реакциями расщепления из альфа-частиц, в свою очередь, полученных из цепочек распада урана . Конечный результат дает тенденцию к более низким отношениям 20 Ne/ 22 Ne и более высоким отношениям 21 Ne/ 22 Ne, наблюдаемым в богатых ураном породах, таких как граниты . [26]
Кроме того, изотопный анализ обнаженных земных пород продемонстрировал космогенное (космическое излучение) производство 21 Ne. Этот изотоп генерируется реакциями расщепления магния , натрия , кремния и алюминия . Анализируя все три изотопа, космогенный компонент может быть выделен из магматического неона и нуклеогенного неона. Это говорит о том, что неон будет полезным инструментом для определения возраста поверхностных пород и метеоритов, полученного в результате космического воздействия . [27]
Неон в солнечном ветре содержит более высокую долю 20 Ne, чем нуклеогенные и космогенные источники. [26] Содержание неона, наблюдаемое в образцах вулканических газов и алмазов, также обогащено 20 Ne, что предполагает его изначальное, возможно, солнечное происхождение. [28]
Неон — второй по легкости благородный газ после гелия . Как и другие благородные газы, неон бесцветен и не имеет запаха. Он светится красновато-оранжевым цветом в вакуумной разрядной трубке . Его холодопроизводительность (на единицу объема) в 40 раз больше, чем у жидкого гелия, и в три раза больше, чем у жидкого водорода . [3] В большинстве случаев это менее дорогой хладагент , чем гелий. [29] [30] Несмотря на то, что гелий превосходит неон по энергии ионизации , теоретически считается, что он наименее реакционноспособен из всех элементов, даже меньше, чем первый. [31]

Неоновая плазма имеет самый интенсивный световой разряд при нормальных напряжениях и токах среди всех благородных газов. Средний цвет этого света для человеческого глаза — красно-оранжевый из-за множества линий в этом диапазоне; он также содержит сильную зеленую линию, которая скрыта, если только визуальные компоненты не рассеиваются спектроскопом. [32]
Стабильные изотопы неона производятся в звездах. Самый распространенный изотоп неона 20 Ne (90,48%) создается в результате ядерного синтеза углерода и углерода в процессе сжигания углерода звездного нуклеосинтеза . Для этого требуются температуры выше 500 мегакельвинов , которые возникают в ядрах звезд с массой более 8 солнечных. [33] [34]
Неон распространен в мировом масштабе; это пятый по распространенности химический элемент во Вселенной по массе после водорода, гелия, кислорода и углерода (см. химический элемент ). [35] Его относительная редкость на Земле, как и у гелия, обусловлена его относительной легкостью, высоким давлением паров при очень низких температурах и химической инертностью, все свойства которых, как правило, удерживают его от попадания в конденсирующиеся газовые и пылевые облака, которые образовали меньшие и более теплые твердые планеты, такие как Земля. Неон одноатомен, что делает его легче молекул двухатомного азота и кислорода, которые составляют большую часть атмосферы Земли; воздушный шар, наполненный неоном, поднимется в воздух, хотя и медленнее, чем гелиевый воздушный шар. [36]
Распространенность неона во Вселенной составляет около 1 части к 750 по массе; в Солнце и, предположительно, в его прото-солнечной системной туманности — около 1 части к 600. [ требуется ссылка ] Атмосферный зонд космического аппарата Галилео обнаружил, что в верхних слоях атмосферы Юпитера распространенность неона уменьшается (истощается) примерно в 10 раз, до уровня 1 части к 6000 по массе. Это может указывать на то, что ледяные планетезимали , которые принесли неон на Юпитер из внешней части Солнечной системы, образовались в регионе, который был слишком теплым, чтобы удерживать неоновый атмосферный компонент (распространенность более тяжелых инертных газов на Юпитере в несколько раз выше, чем на Солнце), [37] или что неон выборочно изолируется во внутренних частях планеты. [38]
Неон составляет 1 часть на 55 000 в атмосфере Земли , или 18,2 ppm по объему (это примерно то же самое, что молекулярная или мольная доля), или 1 часть на 79 000 воздуха по массе. Он составляет меньшую часть в земной коре. Он производится в промышленности путем криогенной фракционной перегонки сжиженного воздуха. [3]
17 августа 2015 года ученые НАСА сообщили об обнаружении неона в экзосфере Луны на основе исследований, проведенных с помощью космического аппарата Lunar Atmosphere and Dust Environment Explorer (LADEE) . [39]
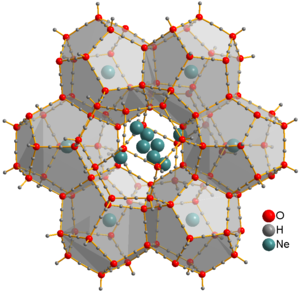
Неон — первый благородный газ p-блока и первый элемент с истинным октетом электронов. Он инертен : как и в случае с его более легким аналогом, гелием , не было идентифицировано прочно связанных нейтральных молекул, содержащих неон . Ионы [Ne Ar ] + , [Ne H ] + и [HeNe] + были обнаружены с помощью оптических и масс-спектрометрических исследований. [3] Твердый клатратный гидрат неона был получен из водяного льда и неонового газа при давлениях 350–480 МПа и температурах около −30 °C. [41] Атомы Ne не связаны с водой и могут свободно перемещаться через этот материал. Их можно извлечь, поместив клатрат в вакуумную камеру на несколько дней, что даст лед XVI , наименее плотную кристаллическую форму воды. [40]
Знакомая шкала электроотрицательности Полинга основана на энергиях химических связей, но такие значения, очевидно, не были измерены для инертного гелия и неона. Шкала электроотрицательности Аллена , которая основана только на (измеримых) атомных энергиях, определяет неон как наиболее электроотрицательный элемент, за которым следуют фтор и гелий. [42]
Температура тройной точки неона (24,5561 К) является определяющей фиксированной точкой в Международной шкале температур 1990 года . [43]
Неон производится из воздуха на криогенных воздухоразделительных установках. Газофазная смесь, в основном состоящая из азота, неона, гелия и водорода [44], отводится из главного конденсатора в верхней части воздухоразделительной колонны высокого давления и подается в нижнюю часть боковой колонны для ректификации неона. [45] Затем ее можно дополнительно очистить от гелия, приведя ее в контакт с активированным углем. Водород очищается от неона путем добавления кислорода, в результате чего образуется вода, которая конденсируется. [44] Один фунт чистого неона может быть получен путем переработки 88 000 фунтов газофазной смеси. [44]
До эскалации войны с Россией в 2022 году около 70% мировых поставок неона производилось на Украине [46] как побочный продукт производства стали в России . [47] По состоянию на 2020 год [обновлять]компания Iceblick с заводами в Одессе и Москве поставляет 65% мирового производства неона, а также 15% криптона и ксенона . [ 48] [49]
Мировые цены на неон подскочили примерно на 600% после российской аннексии Крыма в 2014 году , [50] что побудило некоторых производителей микросхем начать отходить от российских и украинских поставщиков [51] и обращаться к поставщикам в Китае . [49] Российское вторжение в Украину в 2022 году также привело к закрытию двух компаний в Украине, которые производили около половины мировых поставок: Cryoin Engineering ( укр .: Кріоін Інжинірінг ) и Inhaz ( укр .: ІНГАЗ ), расположенных в Одессе и Мариуполе соответственно. [50] Прогнозировалось, что закрытие усугубит дефицит микросхем из-за COVID-19 , [49] [48] что может еще больше переместить производство неона в Китай. [51]
.jpg/440px-FLORIST_(neon_sign).jpg)
Широко используются два совершенно разных вида неонового освещения . Неоновые лампы свечения, как правило, крошечные, большинство из них работают при напряжении от 100 до 250 вольт . [52] Они широко использовались в качестве индикаторов включения питания и в оборудовании для проверки цепей, но в настоящее время в этих приложениях доминируют светодиоды (LED). Эти простые неоновые устройства были предшественниками плазменных дисплеев и плазменных телевизионных экранов . [53] [54] Неоновые вывески обычно работают при гораздо более высоких напряжениях (2–15 киловольт ), а светящиеся трубки обычно имеют длину в несколько метров. [55] Стеклянные трубки часто формируются в формы и буквы для вывесок, а также для архитектурных и художественных целей.
В неоновых вывесках неон производит безошибочно яркий красновато-оранжевый свет, когда через него проходит электрический ток под низким давлением. [56] Хотя трубчатые лампы других цветов часто называют «неоновыми», они используют другие благородные газы или различные цвета флуоресцентного освещения, например, аргон производит лавандовый или синий оттенок. [57] По состоянию на 2012 год доступно более ста цветов. [58]
Неон используется в вакуумных трубках , высоковольтных индикаторах, грозозащитных разрядниках , волномерных трубках, телевизионных трубках и гелий-неоновых лазерах . Газовые смеси, включающие высокочистый неон, используются в лазерах для фотолитографии при изготовлении полупроводниковых приборов . [50]
Сжиженный неон используется в коммерческих целях в качестве криогенного хладагента в приложениях, не требующих более низкого температурного диапазона, достижимого при более экстремальном охлаждении жидким гелием .
Плазменные дисплеи тесно связаны с простой неоновой лампой.