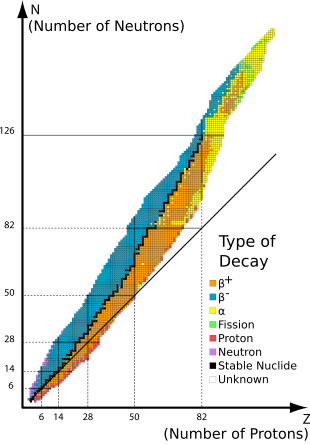
Стабильные нуклиды — это изотопы химического элемента , нуклоны которого находятся в конфигурации, которая не позволяет им получить избыточную энергию, необходимую для создания радиоактивного излучения. Ядра таких изотопов не являются радиоактивными и в отличие от радионуклидов не подвергаются спонтанному радиоактивному распаду . [1] Когда эти нуклиды упоминаются в связи с конкретными элементами, их обычно называют стабильными изотопами этого элемента .
80 элементов с одним или несколькими стабильными изотопами включают в общей сложности 251 нуклид, для которых не было показано распада с использованием современного оборудования. Из этих 80 элементов 26 имеют только один стабильный изотоп и называются моноизотопными . Остальные 56 имеют более одного стабильного изотопа. Олово имеет десять стабильных изотопов, наибольшее количество среди всех элементов.
Большинство встречающихся в природе нуклидов стабильны (около 251; см. список в конце этой статьи), и около 35 (всего 286) известны как радиоактивные с достаточно длинными периодами полураспада (также известны), чтобы возникнуть изначально. Если период полураспада нуклида сопоставим или превышает возраст Земли (4,5 миллиарда лет), значительное количество сохранилось с момента образования Солнечной системы , и тогда говорят, что оно является первичным . Затем оно внесет свой вклад в естественный изотопный состав химического элемента. Первичные радиоизотопы легко обнаруживаются с периодами полураспада всего 700 миллионов лет (например, 235 U ). Это текущий предел обнаружения, [ необходима ссылка ], поскольку более короткоживущие нуклиды пока не были обнаружены в природе бесспорно, за исключением случаев, когда они были произведены недавно, например, в виде продуктов распада или расщепления космическими лучами.
Многие встречающиеся в природе радиоизотопы (еще около 53, всего около 339) имеют период полураспада еще короче 700 миллионов лет, но они производятся недавно, как дочерние продукты процессов распада первичных нуклидов (например, радий из урана) или в ходе продолжающихся энергетических реакций, таких как космогенные нуклиды, образующиеся в результате современной бомбардировки Земли космическими лучами (например, 14C , образующийся из азота).
Некоторые изотопы, которые классифицируются как стабильные (т.е. для них не наблюдалось никакой радиоактивности), как прогнозируется, имеют чрезвычайно долгий период полураспада (иногда 10 18 лет и более). [2] Если прогнозируемый период полураспада попадает в экспериментально доступный диапазон, такие изотопы имеют шанс перейти из списка стабильных нуклидов в категорию радиоактивных, как только будет обнаружена их активность. Например, 209 Bi и 180 W ранее классифицировались как стабильные, но были обнаружены как альфа -активные в 2003 году. Однако такие нуклиды не меняют своего статуса как первичные, когда они обнаруживаются как радиоактивные.
Большинство стабильных изотопов на Земле, как полагают, образовались в процессах нуклеосинтеза , либо во время Большого взрыва , либо в поколениях звезд, предшествовавших образованию Солнечной системы . Однако некоторые стабильные изотопы также показывают вариации распространенности на Земле в результате распада долгоживущих радионуклидов. Эти продукты распада называются радиогенными изотопами, чтобы отличать их от гораздо более многочисленной группы «нерадиогенных» изотопов.
Из известных химических элементов 80 элементов имеют по крайней мере один стабильный нуклид. Они включают в себя первые 82 элемента от водорода до свинца , за исключением технеция (элемент 43) и прометия (элемент 61), которые не имеют стабильных нуклидов. По состоянию на 2023 год было известно в общей сложности 251 «стабильный» нуклид. В этом определении «стабильный» означает нуклид, распад которого на естественном фоне никогда не наблюдался. Таким образом, эти элементы имеют периоды полураспада слишком длинные, чтобы их можно было измерить какими-либо способами, прямыми или косвенными.
Стабильные изотопы:
Таким образом, эти последние 26 элементов называются моноизотопными . [3] Среднее число стабильных изотопов для элементов, имеющих хотя бы один стабильный изотоп, составляет 251/80 = 3,1375.
Стабильность изотопов зависит от соотношения протонов и нейтронов, а также от наличия определенных магических чисел нейтронов или протонов, которые представляют собой закрытые и заполненные квантовые оболочки. Эти квантовые оболочки соответствуют набору энергетических уровней в оболочечной модели ядра; заполненные оболочки, такие как заполненная оболочка из 50 протонов для олова, придают нуклиду необычную стабильность. Как и в случае с оловом, магическое число для Z , атомного номера, имеет тенденцию увеличивать количество стабильных изотопов для элемента.
Так же, как и в случае электронов, которые имеют самое низкое энергетическое состояние, когда они встречаются парами на данной орбитали, нуклоны (как протоны, так и нейтроны) демонстрируют более низкое энергетическое состояние, когда их число четное, а не нечетное. Эта стабильность имеет тенденцию предотвращать бета-распад (в два этапа) многих четно-четных нуклидов в другой четно-четный нуклид с тем же массовым числом, но с более низкой энергией (и, конечно, с двумя протонами больше и двумя нейтронами меньше), потому что распад, происходящий по одному этапу за раз, должен был бы проходить через нечетно-нечетный нуклид с более высокой энергией. Такие ядра, таким образом, вместо этого подвергаются двойному бета-распаду (или теоретически предполагают, что это происходит) с периодами полураспада на несколько порядков больше, чем возраст Вселенной . Это приводит к большему числу стабильных четно-четных нуклидов, которые составляют 150 из 251 общего числа. Стабильные четно-четные нуклиды насчитывают до трех изобар для некоторых массовых чисел и до семи изотопов для некоторых атомных чисел.
Наоборот, из 251 известного стабильного нуклида только пять имеют как нечетное число протонов , так и нечетное число нейтронов: водород-2 ( дейтерий ), литий-6 , бор-10 , азот-14 и тантал-180m . Кроме того, только четыре природных радиоактивных нечетно-нечетных нуклида имеют период полураспада >10 9 лет: калий-40 , ванадий-50 , лантан-138 и лютеций-176 . Нечетно-нечетные первичные нуклиды редки, потому что большинство нечетно-нечетных ядер бета-распадаются , потому что продукты распада четно-четные и, следовательно, более прочно связаны из-за эффектов ядерного спаривания . [4]
Еще одним следствием нестабильности нечетного числа нуклонов любого типа является то, что элементы с нечетным числом имеют тенденцию иметь меньше стабильных изотопов. Из 26 моноизотопных элементов (тех, которые имеют только один стабильный изотоп), все, кроме одного, имеют нечетное атомное число, и все, кроме одного, имеют четное число нейтронов: единственным исключением из обоих правил является бериллий .
Конец стабильных элементов наступает после свинца , в основном потому, что ядра со 128 нейтронами — на два нейтрона выше магического числа 126 — чрезвычайно нестабильны и почти немедленно распадаются на альфа-элементы. [5] Это способствует очень коротким периодам полураспада астата , радона и франция . Похожее явление происходит в гораздо меньшей степени с 84 нейтронами — на два нейтрона выше магического числа 82 — где различные изотопы лантаноидов распадаются на альфа-элементы.
251 известный стабильный нуклид включает тантал-180m, поскольку, хотя его распад автоматически подразумевается его «метастабильностью», этого не наблюдалось. Все «стабильные» изотопы (стабильные по наблюдению, а не по теории) являются основными состояниями ядер, за исключением тантала-180m, который является ядерным изомером или возбужденным состоянием. Основное состояние, тантал-180, радиоактивно с периодом полураспада 8 часов; в отличие от этого, распад ядерного изомера крайне строго запрещен правилами отбора по спиновой четности. Было сообщено путем прямого наблюдения, что период полураспада 180m Ta до гамма-распада должен быть >10 15 лет. Другие возможные режимы распада 180m Ta (бета-распад, электронный захват и альфа-распад) также никогда не наблюдались.
Ожидается, что улучшение экспериментальной чувствительности позволит обнаружить очень слабую радиоактивность некоторых изотопов, которые сейчас считаются стабильными. Например, в 2003 году было сообщено, что висмут-209 (единственный первичный изотоп висмута) очень слабо радиоактивен, с периодом полураспада (1,9 ± 0,2) × 10 19 лет, [6] [7] подтверждая более ранние теоретические предсказания [8] из ядерной физики о том, что висмут-209 будет очень медленно альфа-распадаться .
Изотопы, которые теоретически считаются нестабильными, но не были замечены в распаде, называются наблюдательно стабильными . В настоящее время существует 105 «стабильных» изотопов, которые теоретически нестабильны, 40 из которых были детально изучены без признаков распада, самым легким в любом случае является 36 Ar. Многие «стабильные» нуклиды являются « метастабильными » в том смысле, что они выделяли бы энергию, если бы распадались, [9] и, как ожидается, подвергаются очень редким видам радиоактивного распада , включая двойной бета-распад .
146 нуклидов из 62 элементов с атомными номерами от 1 ( водород ) до 66 ( диспрозий ), за исключением 43 ( технеций ), 61 ( прометий ), 62 ( самарий ) и 63 ( европий ), теоретически стабильны к любому виду ядерного распада — за исключением теоретической возможности протонного распада , который никогда не наблюдался, несмотря на интенсивные его поиски; и спонтанного деления (SF), которое теоретически возможно для нуклидов с атомными массовыми числами ≥ 93. [10]
Помимо SF, другие теоретические пути распада более тяжелых элементов включают: [10]
К ним относятся все нуклиды с массой 165 и более. Аргон-36 — самый легкий известный «стабильный» нуклид, который теоретически нестабилен. [10]
Положительность выделения энергии в этих процессах означает, что они разрешены кинематически (не нарушают закон сохранения энергии) и, таким образом, в принципе могут происходить. [10] Они не наблюдаются из-за сильного, но не абсолютного подавления, правил отбора по спину и четности (для бета-распадов и изомерных переходов) или толщины потенциального барьера (для альфа- и кластерных распадов и спонтанного деления).
Это сводная таблица из Списка нуклидов . Обратите внимание, что цифры не точны и могут немного измениться в будущем, поскольку нуклиды будут обнаружены как радиоактивные или новые периоды полураспада будут определены с некоторой точностью.
Первичные радионуклиды включены для сравнения; они выделены курсивом и смещены относительно списка стабильных нуклидов.
Сокращения для предсказанного ненаблюдаемого распада: [12] [2] [11]
α для альфа-распада, B для бета-распада, 2B для двойного бета-распада, E для электронного захвата, 2E для двойного электронного захвата, IT для изомерного перехода, SF для спонтанного деления, * для нуклидов, периоды полураспада которых имеют нижнюю границу. Двойной бета-распад указан только тогда, когда бета-распад также невозможен.
^ Тантал-180m является «метастабильным изотопом», то есть он является возбуждённым ядерным изомером тантала-180. См. изотопы тантала . Однако период полураспада этого ядерного изомера настолько велик, что его распад никогда не наблюдался, и поэтому он является «наблюдательно стабильным» первичным нуклидом , редким изотопом тантала. Это единственный ядерный изотоп с периодом полураспада настолько велик, что его распад никогда не наблюдался. Поэтому он включён в этот список.
^^ Долгое время считалось, что висмут-209 стабилен из-за его периода полураспада 2,01×10 19 лет, что более чем в миллиард раз превышает возраст Вселенной.
§ Европий-151 и самарий-147 являются первичными нуклидами с очень длительными периодами полураспада: 4,62×10 18 лет и 1,066×10 11 лет соответственно.