Обратная генетика — это метод молекулярной генетики , который используется, чтобы помочь понять функцию(и) гена путем анализа фенотипических эффектов, вызванных генной инженерией определенных последовательностей нуклеиновых кислот внутри гена. Процесс идет в противоположном направлении, в сторону генетического скрининга классической генетики . В то время как прямая генетика стремится найти генетическую основу фенотипа или признака, обратная генетика стремится выяснить, какие фенотипы контролируются конкретными генетическими последовательностями.
Автоматизированное секвенирование ДНК сравнительно быстро генерирует большие объемы данных о геномных последовательностях . Многие генетические последовательности обнаруживаются раньше, чем другая, менее легко получаемая биологическая информация. Обратная генетика пытается связать данную генетическую последовательность с определенным воздействием на организм. [1] Системы обратной генетики также могут позволить извлекать и генерировать инфекционные или дефектные вирусы с желаемыми мутациями. [2] Это дает возможность изучать вирус in vitro и in vivo .
Чтобы изучить влияние последовательности на фенотип или обнаружить ее биологическую функцию, исследователи могут изменить или разрушить ДНК . После того, как это изменение было произведено, исследователь может искать эффект таких изменений во всем организме . Существует несколько различных методов обратной генетики:
Сайт-направленный мутагенез — это сложный метод, который может либо изменить регуляторные области в промоторе гена, либо внести незначительные изменения кодонов в открытой рамке считывания для идентификации важных аминокислотных остатков для функции белка . [ нужна цитата ]

Альтернативно, этот метод можно использовать для создания нулевых аллелей , чтобы ген не работал. Например, удаление гена путем нацеливания на ген ( нокаут гена ) может быть выполнено у некоторых организмов, таких как дрожжи , мыши и мох . Уникальный среди растений, у Physcomitrella patens нокаут гена посредством гомологичной рекомбинации с образованием нокаутного мха (см. рисунок) почти так же эффективен, как и у дрожжей. [4] В случае дрожжевой модельной системы направленные делеции были созданы в каждом несущественном гене дрожжевого генома. [5] В случае с модельной системой растений были созданы огромные библиотеки мутантов на основе конструкций, разрушающих гены. [6] При нокауте гена эндогенный экзон заменяется интересующей измененной последовательностью. [7]
В некоторых случаях можно использовать условные аллели, чтобы ген функционировал нормально до тех пор, пока условный аллель не активируется. Это может повлечь за собой «включение» сайтов рекомбиназы (таких как сайты lox или frt), что приведет к удалению интересующего гена при индуцировании специфической рекомбиназы (например, CRE, FLP). Рекомбиназы Cre или Flp могут быть индуцированы химической обработкой, обработкой тепловым шоком или ограничены определенным подмножеством тканей. [ нужна цитата ]
Другой метод, который можно использовать, — это TILLING . Это метод, который сочетает в себе стандартный и эффективный метод мутагенеза с использованием химического мутагена, такого как этилметансульфонат (EMS), с чувствительным методом скрининга ДНК, который идентифицирует точечные мутации в целевом гене. [ нужна цитата ]
В области вирусологии методы обратной генетики могут использоваться для выделения полноразмерных инфекционных вирусов с желаемыми мутациями или вставками в вирусные геномы или в конкретные вирусные гены. Технологии, позволяющие проводить эти манипуляции, включают реакцию кольцевого полимеразного удлинения (CPER), которая впервые была использована для создания инфекционной кДНК вируса Кунджин, близкого родственника вируса Западного Нила. [8] CPER также успешно использовался для создания ряда РНК-вирусов с положительным смыслом, таких как SARS-CoV-2, [9] возбудитель COVID-19.
Открытие подавления генов с помощью двухцепочечной РНК, также известного как РНК-интерференция (РНКи), и разработка нокдауна генов с использованием морфолиноолигонуклеотидов сделали нарушение экспрессии генов доступным методом для многих других исследователей. Этот метод часто называют нокдауном гена, поскольку эффект этих реагентов обычно временный, в отличие от нокаута гена , который является постоянным. [ нужна цитата ]
RNAi создает специфический эффект нокаута без фактической мутации интересующей ДНК. У C. elegans РНКи использовалась для систематического вмешательства в экспрессию большинства генов в геноме. RNAi действует, направляя клеточные системы на деградацию целевой информационной РНК (мРНК). [ нужна цитата ]
РНКи-интерференция, в частности подавление генов, стала полезным инструментом для подавления экспрессии генов, а также для выявления и анализа их фенотипа потери функции. Когда в аллелях происходят мутации, функция, которую они представляют и кодируют, также мутирует и теряется; обычно это называют мутацией потери функции. [10] Способность анализировать фенотип потери функции позволяет анализировать функцию гена, когда нет доступа к мутантным аллелям. [11]
Хотя эффективность РНК-интерференции зависит от клеточных компонентов (например, белков Dicer, комплекса RISC), простой альтернативой нокдауну гена являются антисмысловые олигонуклеотиды морфолино . Морфолинозы связываются и блокируют доступ к целевой мРНК, не требуя активности клеточных белков и не обязательно ускоряя деградацию мРНК. Морфолино эффективны в системах различной сложности: от бесклеточной трансляции в пробирке до исследований in vivo на моделях крупных животных. [ нужна цитата ]
Молекулярно -генетический подход заключается в создании трансгенных организмов, которые сверхэкспрессируют интересующий нормальный ген. Результирующий фенотип может отражать нормальную функцию гена.
Альтернативно возможна сверхэкспрессия мутантных форм гена, которые мешают нормальному функционированию гена ( дикого типа ). Например, сверхэкспрессия мутантного гена может привести к высоким уровням нефункционального белка, что приведет к доминантному негативному взаимодействию с белком дикого типа. В этом случае мутантная версия будет конкурировать за партнеров по белкам дикого типа, что приведет к мутантному фенотипу.
Другие мутантные формы могут привести к образованию белка, который аномально регулируется и конститутивно активен («все время включен»). Это может быть связано с удалением регуляторного домена или мутацией определенного амино остатка, который обратимо модифицируется (путем фосфорилирования , метилирования или убиквитинирования ). Любое изменение имеет решающее значение для модуляции функции белка и часто приводит к информативным фенотипам.
Обратная генетика играет большую роль в синтезе вакцин . Вакцины могут быть созданы путем разработки новых генотипов инфекционных вирусных штаммов, которые уменьшают их патогенную активность настолько, чтобы усилить иммунитет у хозяина. Подход обратной генетики к синтезу вакцин использует известные вирусные генетические последовательности для создания желаемого фенотипа: вируса как с ослабленной патологической активностью, так и со сходством с нынешним циркулирующим штаммом вируса. Обратная генетика представляет собой удобную альтернативу традиционному методу создания инактивированных вакцин , вирусов которых уничтожают с помощью тепла или других химических методов.
Вакцины, созданные методами обратной генетики, известны как аттенуированные вакцины , потому что они содержат ослабленные (аттенуированные) живые вирусы. Аттенуированные вакцины создаются путем объединения генов нового или существующего штамма вируса с ранее аттенуированными вирусами того же вида. [12] Ослабленные вирусы создаются путем размножения живого вируса в новых условиях, например, в курином яйце. В результате получается вирусный штамм, который все еще жив, но не патогенен для человека [13] , поскольку эти вирусы становятся дефектными, поскольку они не могут достаточно реплицировать свой геном для размножения и достаточного заражения хозяина. Однако вирусные гены по-прежнему экспрессируются в клетке-хозяине посредством одного цикла репликации, что позволяет развить иммунитет. [14]
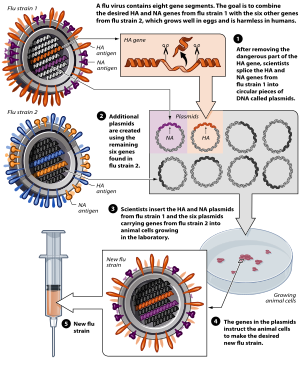
Распространенным способом создания вакцины с использованием методов обратной генетики является использование плазмид для синтеза аттенуированных вирусов. Этот метод чаще всего используется при ежегодном производстве вакцин против гриппа , где восьмиплазмидная система может быстро производить эффективную вакцину. Полный геном вируса гриппа А состоит из восьми сегментов РНК, поэтому комбинация шести аттенуированных вирусных плазмид кДНК с двумя плазмидами дикого типа позволяет создать аттенуированный вакцинный штамм. Для разработки вакцин против гриппа четвертый и шестой сегменты РНК, кодирующие белки гемагглютинин и нейраминидаза соответственно, берутся из циркулирующего вируса, а остальные шесть сегментов получают из ранее аттенуированного мастер-штамма. Белки HA и NA обладают высоким разнообразием антигенов и поэтому взяты из текущего штамма, для которого производится вакцина, для создания хорошо подходящей вакцины. [12]
Плазмида, используемая в этой системе из восьми плазмид, содержит три основных компонента, которые позволяют разработать вакцину. Во-первых, плазмида содержит сайты рестрикции , которые позволяют включить в плазмиду гены гриппа. Во-вторых, плазмида содержит ген устойчивости к антибиотику, что позволяет отбирать только плазмиды, содержащие правильный ген. Наконец, плазмида содержит два промотора: человеческий pol 1 и pol 2, которые транскрибируют гены в противоположных направлениях. [15]
Последовательности кДНК вирусной РНК синтезируют из аттенуированных мастер-штаммов с помощью RT-PCR . [12] Эта кДНК затем может быть вставлена между промотором РНК-полимеразы I (Pol I) и последовательностью терминатора посредством расщепления рестриктазой. Затем кДНК и последовательность pol I, в свою очередь, окружаются промотором РНК-полимеразы II (Pol II) и сайтом полиаденилирования . [16] Вся эта последовательность затем вставляется в плазмиду. Шесть плазмид, полученных из кДНК аттенуированного мастер-штамма, котрансфицируют в клетку-мишень, часто куриное яйцо, вместе с двумя плазмидами циркулирующего в настоящее время штамма гриппа дикого типа. Внутри клетки-мишени два «сложенных друг на друга» фермента Pol I и Pol II транскрибируют вирусную кДНК, синтезируя как вирусную РНК с отрицательным смыслом, так и мРНК с положительным смыслом, эффективно создавая аттенуированный вирус. [12] В результате получается дефектный вакцинный штамм, похожий на нынешний штамм вируса, позволяющий хозяину выработать иммунитет. Этот синтезированный вакцинный штамм затем можно использовать в качестве исходного вируса для создания дальнейших вакцин.
Вакцины, созданные с помощью обратной генетики, имеют ряд преимуществ по сравнению с традиционными разработками вакцин. Самое главное — скорость производства. Из-за высокой антигенной изменчивости гликопротеинов HA и NA подход обратной генетики позволяет быстро сформулировать необходимый генотип (т.е. тот, который содержит белки HA и NA, взятые из циркулирующих в настоящее время вирусных штаммов). [12] Кроме того, поскольку конечным продуктом производства вакцины, аттенуированной обратной генетикой, является живой вирус, он демонстрирует более высокую иммуногенность , чем традиционные инактивированные вакцины, [17] которые необходимо уничтожить с помощью химических процедур перед переносом в качестве вакцины. Однако из-за живой природы аттенуированных вирусов у пациентов с иммунодефицитом могут возникнуть осложнения . [18] Существует также вероятность того, что мутация вируса может привести к тому, что вакцина снова превратится в живой неаттенуированный вирус. [19]