Оксианион , или оксоанион , представляет собой ион с общей формулой A
хОг −
у(где A представляет собой химический элемент , а O представляет собой атом кислорода ). Оксианионы образуются большинством химических элементов . [1] Формулы простых оксианионов определяются правилом октета . Соответствующая оксикислота оксианиона — это соединение H
зА
хО
у. Структуры конденсированных оксианионов можно рационализировать в терминах полиэдрических единиц AO n с общими углами или ребрами между полиэдрами. Оксианионы (в частности, фосфатные и полифосфатные эфиры) аденозинмонофосфат ( АМФ ), аденозиндифосфат ( АДФ ) и аденозинтрифосфат (АТФ) играют важную роль в биологии.
Формула мономерных оксианионов, АОм −
н, определяется степенью окисления элемента A и его положением в периодической таблице . Элементы первого ряда ограничены максимальным координационным числом 4. Однако ни один из элементов первого ряда не имеет мономерного оксианиона с таким координационным числом. Вместо этого карбонат ( CO2−
3) и нитрат ( NO−
3) имеют тригональную плоскую структуру с π-связью между центральным атомом и атомами кислорода. Эта π-связь благоприятствует схожести размеров центрального атома и кислорода.
Оксианионы элементов второго ряда в степени окисления группы являются тетраэдрическими . Тетраэдрические блоки SiO 4 встречаются в минералах оливина , (Mg,Fe) 2 SiO 4 , но анион не существует отдельно, так как атомы кислорода окружены тетраэдрически катионами в твердом состоянии. Фосфат ( PO3−
4), сульфат ( SO2−
4) и перхлорат ( ClO−
4) ионы могут быть обнаружены как таковые в различных солях. Многие оксианионы элементов в более низкой степени окисления подчиняются правилу октета , и это может быть использовано для рационализации принятых формул. Например, хлор(V) имеет два валентных электрона, поэтому он может вмещать три электронные пары из связей с оксидными ионами. Заряд иона равен +5 − 3 × 2 = −1, и поэтому формула имеет вид ClO−
3. Структура иона предсказывается теорией VSEPR как пирамидальная, с тремя связывающими электронными парами и одной неподеленной парой. Аналогичным образом, оксианион хлора(III) имеет формулу ClO−
2, и изогнут с двумя неподеленными парами и двумя связывающими парами.
В третьей и последующих строках периодической таблицы возможна 6-координация, но изолированные октаэдрические оксианионы неизвестны, поскольку они несли бы слишком высокий электрический заряд. Таким образом, молибден(VI) не образует MoO6−
6, но образует тетраэдрический молибдат- анион MoO2−
4. Единицы MoO 6 встречаются в конденсированных молибдатах. Полностью протонированные оксианионы с октаэдрической структурой встречаются в таких видах, как Sn(OH)2−
6и Sb(ОН)−
6. Кроме того, ортопериодат может быть только частично депротонирован, [Примечание 1] с
Наименование мономерных оксианионов подчиняется следующим правилам.
Здесь группа галогенов (группа 7 А, 17) упоминается как группа VII, а группа благородных газов (группа 8 А) упоминается как группа VIII.
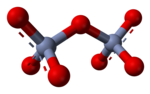
В водном растворе оксианионы с высоким зарядом могут вступать в реакции конденсации, например, при образовании дихромат- иона Cr2O .2−7:
Движущей силой этой реакции является уменьшение плотности электрического заряда на анионе и устранение иона гидроксония ( H + ). Количество порядка в растворе уменьшается, высвобождая определенное количество энтропии , что делает свободную энергию Гиббса более отрицательной и благоприятствует прямой реакции. Это пример кислотно-основной реакции с мономерным оксианионом, действующим как основание, и конденсированным оксианионом, действующим как его сопряженная кислота . Обратная реакция является реакцией гидролиза , поскольку молекула воды , действующая как основание, расщепляется. Может происходить дальнейшая конденсация, особенно с анионами с более высоким зарядом, как это происходит с аденозинфосфатами.
Превращение АТФ в АДФ представляет собой реакцию гидролиза и является важным источником энергии в биологических системах.
Образование большинства силикатных минералов можно рассматривать как результат реакции деконденсации, в которой кремний реагирует с основным оксидом, кислотно-щелочной реакцией в смысле Люкса-Флада .

Полиоксианион — это полимерный оксианион, в котором несколько мономеров оксианиона, обычно рассматриваемых как полиэдры MO n , соединены общими углами или ребрами. [4] Когда два угла полиэдра являются общими, результирующая структура может быть цепью или кольцом. Короткие цепи встречаются, например, в полифосфатах . Иносиликаты, такие как пироксены , имеют длинную цепь тетраэдров SiO 4 , каждый из которых имеет два общих угла. Такая же структура встречается в так называемых метаванадатах, таких как метаванадат аммония , NH 4 VO 3 .
Формула оксианиона SiO2−3получается следующим образом: каждый номинальный ион кремния ( Si 4+ ) присоединен к двум номинальным оксидным ионам ( O 2− ) и имеет половину доли в двух других. Таким образом, стехиометрия и заряд определяются как:
Кольцо можно рассматривать как цепь, в которой два конца соединены. Циклический трифосфат , P 3 O3−9является примером.
Когда три угла являются общими, структура расширяется в двух измерениях. В амфиболах (примером которых является асбест ) две цепи связаны вместе путем совместного использования третьего угла в чередующихся местах вдоль цепи. Это приводит к идеальной формуле Si 4 O6−11и линейная цепочечная структура, которая объясняет волокнистую природу этих минералов. Совместное использование всех трех углов может привести к образованию листовой структуры, как в слюде , Si 2 O2−5, в котором каждый кремний имеет один кислород для себя и половину доли в трех других. Кристаллическая слюда может быть расколота на очень тонкие листы.
Совместное использование всех четырех углов тетраэдров приводит к образованию трехмерной структуры, например, кварца . Алюмосиликаты — это минералы, в которых часть кремния замещена алюминием. Однако степень окисления алюминия на единицу меньше, чем у кремния, поэтому замена должна сопровождаться добавлением еще одного катиона. Число возможных комбинаций такой структуры очень велико, что отчасти является причиной того, почему существует так много алюмосиликатов.
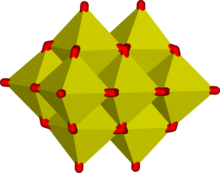
Октаэдрические единицы MO 6 обычны в оксианионах более крупных переходных металлов. Некоторые соединения, такие как соли цепочечно-полимерного иона, Mo 2 O2−7даже содержат как тетраэдрические, так и октаэдрические единицы. [5] [6] Совместное использование ребер распространено в ионах, содержащих октаэдрические строительные блоки, и октаэдры обычно искажены, чтобы уменьшить напряжение в мостиковых атомах кислорода. Это приводит к трехмерным структурам, называемым полиоксометаллатами . Типичные примеры встречаются в структуре Кеггина иона фосфоромолибдата . Совместное использование ребер является эффективным средством снижения плотности электрического заряда, как можно увидеть с помощью гипотетической реакции конденсации с участием двух октаэдров:
Здесь средний заряд на каждом атоме М уменьшается на 2. Эффективность совместного использования ребер демонстрируется следующей реакцией, которая происходит при подкислении щелочного водного раствора молибдата.
Тетраэдрический ион молибдата преобразуется в кластер из 7 октаэдров, связанных ребрами [6] [7], что дает средний заряд на каждом молибдене 6 ⁄ 7. Гептамолибдатный кластер настолько стабилен, что кластеры с 2–6 единицами молибдата не были обнаружены, хотя они должны были образоваться в качестве промежуточных продуктов.
pKa соответствующих кислот можно определить по числу двойных связей с кислородом. Таким образом, хлорная кислота является очень сильной кислотой, а хлорноватистая кислота — очень слабой. Простое правило обычно работает с точностью до 1 единицы pH.
Большинство оксианионов являются слабыми основаниями и могут быть протонированы с образованием кислот или кислых солей. Например, ион фосфата может быть последовательно протонирован с образованием фосфорной кислоты.


Степень протонирования в водном растворе будет зависеть от констант диссоциации кислоты и pH . Например, AMP (аденозинмонофосфат) имеет значение ap K a 6,21, [8], поэтому при pH 7 он будет протонирован примерно на 10%. Нейтрализация заряда является важным фактором в этих реакциях протонирования. Напротив, одновалентные анионы перхлорат- и перманганат- ионы очень трудно протонировать, и поэтому соответствующие кислоты являются сильными кислотами .
Хотя кислоты, такие как фосфорная кислота, записываются как H 3 PO 4 , протоны присоединены к атомам кислорода, образуя гидроксильные группы, поэтому формулу можно также записать как OP(OH) 3 , чтобы лучше отразить структуру. Серную кислоту можно записать как O 2 S(OH) 2 ; это молекула, наблюдаемая в газовой фазе.
Ион фосфита , PO3−3, является сильным основанием , и поэтому всегда несет по крайней мере один протон. В этом случае протон присоединен непосредственно к атому фосфора со структурой HPO2−3. При образовании этого иона ион фосфита ведет себя как основание Льюиса и отдает пару электронов кислоте Льюиса, H + .

Как упоминалось выше, реакция конденсации также является кислотно-основной реакцией. Во многих системах могут происходить как реакции протонирования, так и реакции конденсации. Случай хромат-иона дает относительно простой пример. На диаграмме преобладания для хромата, показанной справа, pCr обозначает отрицательный логарифм концентрации хрома, а pH обозначает отрицательный логарифм концентрации ионов H + . Существует два независимых равновесия. Константы равновесия определяются следующим образом. [9]
Диаграмма преобладания интерпретируется следующим образом.
Виды H 2 CrO 4 и HCr 2 O−7не показаны, поскольку они образуются только при очень низком pH.
Диаграммы преобладания могут стать очень сложными, когда могут образовываться многие полимерные виды, [10] такие как ванадаты , молибдаты и вольфраматы . Другое осложнение заключается в том, что многие из высших полимеров образуются чрезвычайно медленно, так что равновесие может не быть достигнуто даже за месяцы, что приводит к возможным ошибкам в константах равновесия и диаграмме преобладания.
{{cite book}}: CS1 maint: multiple names: authors list (link)