Олефинирование Жюлиа ( также известное как олефинирование Жюлиа–Литго ) — это химическая реакция, используемая в органической химии фенилсульфонов (1) с альдегидами (или кетонами ) для получения алкенов (олефинов) (3) после функционализации спирта и восстановительного элиминирования с использованием амальгамы натрия [1] [2] или SmI 2 . [3] Реакция названа в честь французского химика Марка Жюлиа .
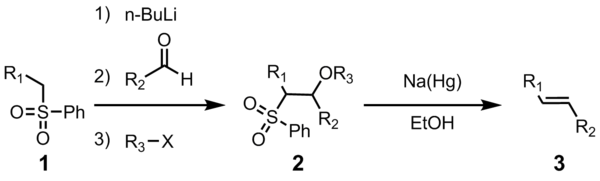
Полезность этой реакции олефинирования соединительных соединений обусловлена ее универсальностью, широкой толерантностью к функциональным группам и мягкими условиями, в которых протекает реакция.
Все четыре стадии можно осуществить в одном реакционном сосуде, и использование R 3 X необязательно. Однако очистка промежуточного сульфона 2 приводит к более высокому выходу и чистоте. Чаще всего R 3 представляет собой ацетил или бензоил , с уксусным ангидридом или бензоилхлоридом, используемыми при получении 2.
В 1973 году Марк Жюлиа и Жан-Марк Парис сообщили о новом синтезе олефинов, в котором β-ацилоксисульфоны были восстановительно элиминированы в соответствующие ди-, три- или тетразамещенные алкены. [4] Бэзил Литго и Филип Дж. Косиенски исследовали область применения и ограничения реакции, и сегодня это олефинирование официально известно как олефинирование Джулиа-Литго. [5] Реакция включает добавление сульфонил-стабилизированного карбаниона к карбонильному соединению с последующим элиминированием с образованием алкена. В первоначальных версиях реакций элиминирование проводилось в восстановительных условиях. Совсем недавно была разработана модифицированная версия, которая избегает этого этапа. Первая версия иногда называется олефинированием Джулиа-Литго, тогда как последняя называется олефинированием Джулиа-Коциенски. В восстановительном варианте аддукт обычно ацилируют, а затем обрабатывают восстановителем, таким как амальгама натрия [6] [7] или SmI 2 . [8] Было опубликовано несколько обзоров этих реакций. [9] [10]
Начальные шаги просты. Анион фенилсульфона (2) реагирует с альдегидом, образуя алкоксид (3). Алкоксид функционализируется с помощью R 3 -X, давая стабильное промежуточное соединение (4). Точный механизм восстановления амальгамы натрия неизвестен, но было показано, что он протекает через винильный радикал (5) [11] . Протонирование винильного радикала дает желаемый продукт (6).

Стереохимия алкена (6) не зависит от стереохимии промежуточного сульфона 4. Считается, что радикальные промежуточные соединения способны уравновешиваться, так что чаще всего получается более термодинамически стабильный транс-олефин. Это превращение в значительной степени благоприятствует образованию E -алкена. [12]

Модифицированное олефинирование Джулиа, также известное как однореакторное олефинирование Джулиа, является модификацией классического олефинирования Джулиа. Замена фенилсульфонов гетероарилсульфонами значительно изменяет путь реакции. [13] Наиболее популярным примером является бензотиазолсульфон . [14] Реакция бензотиазолсульфона (1) с диизопропиламидом лития (LDA) дает металлированный бензотиазолилсульфон, который быстро реагирует с альдегидами (или кетонами) с образованием промежуточного алкоксида (2). В отличие от фенилсульфонов, этот промежуточный алкоксид (2) более реакционноспособен и будет подвергаться перегруппировке Смайлса [15] с образованием сульфинатной соли (4). Сульфинатная соль (4) будет спонтанно отщеплять диоксид серы и литийбензотиазолон (5), образуя желаемый алкен (6).

Поскольку бензотиазольная вариация олефинирования Джулиа не включает в себя уравновешивающие промежуточные продукты, стереохимический результат является результатом стереохимии начального карбонильного присоединения. В результате эта реакция часто генерирует смесь стереоизомеров алкенов.

Олефинирование Джулиа-Коциенски, дальнейшее усовершенствование модифицированного олефинирования Джулиа, обеспечивает очень хорошую E -селективность. В олефинировании Джулиа-Коциенски [16] алкилирующим агентом является тетразол . Он протекает по тому же механизму, что и бензотиазолсульфон выше. Высокая E -селективность олефинирования Джулиа-Коциенски является результатом кинетически контролируемого диастереоселективного присоединения металлированных 1-фенил-1H-тетразол-5-ил (PT) сульфонов к несопряженным альдегидам. Это дает анти-β-алкоксисульфоны, которые стереоспецифически разлагаются до E -алкенов . [17] В одной из адаптаций [18] с t-бутилтетразоилметилсульфоном условия реакции — либо бис(триметилсилил)амид натрия при −70 °C в тетрагидрофуране , либо карбонат цезия при +70 °C. Эта реакция названа в честь Филиппа Дж. Коченски за его модификацию олефинирования Жюлиа.

Реакция олефинирования Жюлиа или модифицированная реакция Жюлиа представляет собой мощное и универсальное синтетическое превращение, широко используемое при создании сложных природных продуктов с превосходным контролем геометрической изомерии.
Птеростильбен — это стильбеноид, химически родственный ресвератролу. Он относится к группе фитоалексинов, агентов, вырабатываемых растениями для борьбы с инфекциями. [19] Птеростильбен — это встречающийся в природе аналог ресвератрола — диметиловый эфир. Считается, что это соединение также обладает антидиабетическими свойствами, но до сих пор этот вопрос изучен очень мало.
По сравнению с реакциями Виттига , Виттига-Хорнера, Перкина или катализируемыми переходными металлами реакциями синтеза птеростилебена, олефинирование по Жюлиа предлагает простой и экономичный альтернативный метод получения птеростилебена. [20] [21]
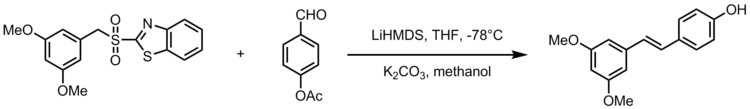
Одна из адаптаций олефинирования Джулии-Коциенски дает синтез стильбеноида ресвератрола , природного соединения, встречающегося в обычных продуктах питания, таких как виноград, вина и орехи. Ресвератрол является биологически важным стильбеноидом, который, как предполагается, имеет много преимуществ для здоровья. Олефинирование Джулии-Коциенски служит мощной реакцией в синтезе аналогов ресвератрола с 3,5-бис(трифторметил)фенилсульфонами. Следующая схема отображает общую схему синтеза аналогов ресвератрола, где R 2 представляет собой арильную группу. [22]

В асимметричном общем синтезе (−)-каллистатина А, проведенном Амосом Смитом , два отдельных олефинирования Джулиа были использованы для присоединения двух E -алкеновых фрагментов. [23] (−)-каллистатин А является членом семейства антибиотиков лептомицина. Следующая схема отображает олефинирование Джулиа-Коциенски, используемое для получения предшественника натурального продукта, как показано с помощью использования PT-сульфона.
