Актиний — химический элемент ; он имеет символ Ac и атомный номер 89. Впервые он был выделен Фридрихом Оскаром Гизелем в 1902 году, который дал ему название эманиум ; элемент получил свое название из-за того, что его ошибочно отождествили с веществом, которое Андре-Луи Дебьерн обнаружил в 1899 году и назвал актинием. Актиний дал название ряду актинидов — набору из 15 элементов между актинием и лоуренсием в периодической таблице . Вместе с полонием , радием и радоном актиний был одним из первых непервичных радиоактивных элементов, которые были выделены.
Мягкий серебристо-белый радиоактивный металл актиний быстро реагирует с кислородом и влагой воздуха, образуя белый налет оксида актиния, который предотвращает дальнейшее окисление. Как и большинство лантаноидов и многих актинидов , актиний принимает степень окисления +3 почти во всех своих химических соединениях. Актиний встречается только в следовых количествах в урановых и ториевых рудах в виде изотопа 227 Ac, который распадается с периодом полураспада 21,772 года, преимущественно испуская бета- , а иногда и альфа-частицы , и 228 Ac, который является бета-активным с периодом полураспада 6.15 часов. Одна тонна природного урана в руде содержит около 0,2 миллиграмма актиния-227, а одна тонна тория — около 5 нанограммов актиния-228. Близкое сходство физических и химических свойств актиния и лантана делает выделение актиния из руды нецелесообразным. Вместо этого элемент в миллиграммовых количествах получают нейтронным облучением 226 Ra в ядерном реакторе . Из-за своей редкости, высокой цены и радиоактивности актиний не имеет значительного промышленного применения. Его текущие применения включают источник нейтронов и агент для лучевой терапии .
Андре-Луи Дебьерн , французский химик, объявил об открытии нового элемента в 1899 году. Он выделил его из остатков настурана, оставленного Марией и Пьером Кюри после того, как они извлекли радий . В 1899 году Дебьерн описал вещество как похожее на титан [5] и (в 1900 году) как похожее на торий . [6] Фридрих Оскар Гизель обнаружил в 1902 году [7] вещество, похожее на лантан, и назвал его «эманиумом» в 1904 году. [8] После сравнения периодов полураспада веществ, определенных Дебьерном, [9] Гарриет Брукс в 1904 году. и Отто Хана и Отто Сакура в 1905 году, выбранное Дебьерном название нового элемента было сохранено, поскольку оно имело старшинство, несмотря на противоречивые химические свойства, которые он утверждал для этого элемента в разное время. [10] [11]
Статьи, опубликованные в 1970-х годах [12] и позже [13], предполагают, что результаты Дебьерна, опубликованные в 1904 году, противоречат результатам, опубликованным в 1899 и 1900 годах. Более того, известный теперь химический состав актиния исключает его присутствие в качестве чего-либо иного, чем второстепенный компонент Дебьерна Результаты 1899 и 1900 годов; на самом деле, химические свойства, о которых он сообщил, позволяют предположить, что вместо этого он случайно идентифицировал протактиний , который не будет открыт еще четырнадцать лет, только для того, чтобы он исчез из-за его гидролиза и адсорбции на его лабораторном оборудовании . Это побудило некоторых авторов выступить за то, чтобы приписать открытие только Гизелю. [2] Менее конфронтационный взгляд на научные открытия предложен Адлоффом. [13] Он предполагает, что ретроспективная критика ранних публикаций должна быть смягчена тогдашним зарождающимся состоянием радиохимии: подчеркивая разумность утверждений Дебьерна в оригинальных статьях, он отмечает, что никто не может утверждать, что вещество Дебьерна не содержало актиния. [13] Дебьерн, которого сейчас подавляющее большинство историков считает первооткрывателем, потерял интерес к элементу и оставил эту тему. С другой стороны, Гизелю по праву можно приписать первое получение радиохимически чистого актиния и определение его атомного номера 89. [12]
Название актиний происходит от древнегреческого слова aktis, aktinos (ακτίς, ακτίνος), что означает луч или луч. [14] Его символ Ac также используется в аббревиатурах других соединений, не имеющих ничего общего с актинием, таких как ацетил , ацетат [15] и иногда ацетальдегид . [16]
Актиний — мягкий серебристо-белый [17] [18] радиоактивный металлический элемент. Его расчетный модуль сдвига аналогичен модулю сдвига свинца . [19] Благодаря своей сильной радиоактивности актиний светится в темноте бледно-голубым светом, который исходит от окружающего воздуха, ионизированного испускаемыми энергичными частицами. [20] Актиний имеет сходные химические свойства с лантаном и другими лантанидами, поэтому эти элементы трудно отделить при извлечении из урановых руд. Для разделения обычно используют экстракцию растворителем и ионную хроматографию . [21]
Первый элемент актинидов , актиний, дал этому множеству свое название, так же, как лантан дал лантанидам . Актиниды гораздо более разнообразны, чем лантаноиды [22] , и поэтому только в 1945 году наиболее значительное изменение в периодической таблице Дмитрия Менделеева с момента признания лантаноидов, введение актинидов , было общепринятым после Гленна Т. Исследования Сиборга по трансурановым элементам [23] (хотя они были предложены ещё в 1892 году британским химиком Генри Бассеттом). [24]
Актиний быстро реагирует с кислородом и влагой воздуха, образуя белый налет оксида актиния , препятствующий дальнейшему окислению. [17] Как и большинство лантаноидов и актинидов, актиний существует в степени окисления +3, а ионы Ac 3+ в растворах бесцветны. [25] Степень окисления +3 возникает из электронной конфигурации [Rn] 6d 1 7s 2 актиния с тремя валентными электронами, которые легко отдаются, чтобы создать стабильную структуру закрытой оболочки благородного газа радона . [18] Хотя 5f-орбитали в атоме актиния незаняты, ее можно использовать в качестве валентной орбитали в актиниевых комплексах, и поэтому авторы, работающие над ней, обычно считают ее первым 5f-элементом. [26] [27] [28] Ac 3+ является самым крупным из всех известных триположительных ионов, и его первая координационная сфера содержит примерно 10,9 ± 0,5 молекул воды. [29]
Из-за высокой радиоактивности актиния известно лишь ограниченное количество соединений актиния. К ним относятся: AcF 3 , AcCl 3 , AcBr 3 , AcOF, AcOCl, AcOBr, Ac 2 S 3 , Ac 2 O 3 , AcPO 4 и Ac(NO 3 ) 3 . Все они содержат актиний в степени окисления +3. [25] [30] В частности, постоянные решетки аналогичных соединений лантана и актиния различаются всего на несколько процентов. [30]
Здесь a , b и c — постоянные решетки, No — номер пространственной группы, а Z — количество формульных единиц на элементарную ячейку . Плотность не измерялась напрямую, а рассчитывалась по параметрам решетки.
Оксид актиния (Ac 2 O 3 ) можно получить нагреванием гидроксида при 500 °C или оксалата при 1100 °C в вакууме. Его кристаллическая решетка изотипна оксидам большинства трехвалентных редкоземельных металлов. [30]
Трифторид актиния можно получить как в растворе, так и в твердой реакции. Первую реакцию проводят при комнатной температуре, добавляя плавиковую кислоту к раствору, содержащему ионы актиния. В последнем методе металлический актиний обрабатывается парами фторида водорода при температуре 700 ° C в полностью платиновой установке. Обработка трифторида актиния гидроксидом аммония при 900–1000 ° C дает оксифторид AcOF. Если оксифторид лантана легко получить сжиганием трифторида лантана на воздухе при температуре 800 °С в течение часа, то аналогичная обработка трифторида актиния не дает AcOF и приводит лишь к плавлению исходного продукта. [30] [36]
Трихлорид актиния получают путем взаимодействия гидроксида или оксалата актиния с парами четыреххлористого углерода при температуре выше 960 °С. Подобно оксифториду, оксихлорид актиния можно получить гидролизом трихлорида актиния гидроксидом аммония при 1000 ° C. Однако, в отличие от оксифторида, оксихлорид вполне можно было синтезировать путем прокаливания раствора трихлорида актиния в соляной кислоте с аммиаком . [30]
Реакция бромида алюминия и оксида актиния дает трибромид актиния:
и обработка его гидроксидом аммония при 500 ° C приводит к образованию оксибромида AcOBr. [30]
Гидрид актиния был получен восстановлением трихлорида актиния калием при 300 °С, а его строение установлено по аналогии с соответствующим гидридом LaH 2 . Источник водорода в реакции был неопределенным. [37]
Смешивание мононатрийфосфата (NaH 2 PO 4 ) с раствором актиния в соляной кислоте дает полугидрат фосфата актиния белого цвета (AcPO 4 ·0,5H 2 O), а нагревание оксалата актиния с парами сероводорода при 1400 °С в течение нескольких минут. приводит к образованию черного сульфида актиния Ac 2 S 3 . Возможно, его можно получить, воздействуя смесью сероводорода и сероуглерода на оксид актиния при температуре 1000 °С. [30]
Встречающийся в природе актиний в основном состоит из двух радиоактивных изотопов ;227
Ас (из радиоактивного семейства235
У ) и228
Ак (внучка232
эт ).227
Ac распадается в основном как бета-излучатель с очень малой энергией, но в 1,38% случаев он испускает альфа-частицу , поэтому его легко идентифицировать с помощью альфа-спектрометрии. [2] Идентифицировано тридцать три радиоизотопа , наиболее стабильным из которых является227
Ас с периодом полураспада 21,772 года,225
Ас с периодом полураспада 10,0 дней и226
Ac с периодом полураспада 29,37 часов. Все остальные радиоактивные изотопы имеют период полураспада менее 10 часов, а у большинства из них период полураспада короче одной минуты. Самый короткоживущий известный изотоп актиния —217
Ac (период полураспада 69 наносекунд), который распадается посредством альфа-распада . Актиний также имеет два известных метасостояния . [38] Наиболее значимыми для химии изотопами являются 225 Ac, 227 Ac и 228 Ac. [2]
очищенный227
Ас приходит в равновесие с продуктами распада примерно через пол года. Он распадается в соответствии со своим периодом полураспада 21,772 года, выделяя в основном бета-частицы (98,62%) и некоторые альфа-частицы (1,38%); [38] последовательные продукты распада входят в ряд актиния . Из-за небольших доступных количеств, низкой энергии его бета-частиц (максимум 44,8 кэВ) и низкой интенсивности альфа-излучения,227
Ac трудно обнаружить непосредственно по его излучению, поэтому его отслеживают по продуктам распада. [25] Изотопы актиния имеют атомный вес от 203 u (203
Ac ) до 236 u (236
Ас ). [38]

Актиний встречается лишь в следовых количествах в урановых рудах (одна тонна урана в руде содержит около 0,2 миллиграмма 227 Ac [39] [40] ) и в ториевых рудах, которые содержат около 5 нанограммов 228 Ac на одну тонну тория. Изотоп актиния 227 Ac — переходный член цепочки распада уран-актиниевого ряда , которая начинается с родительского изотопа 235 U (или 239 Pu ) и заканчивается стабильным изотопом свинца 207 Pb . Изотоп 228 Ac является переходным членом цепочки распада ряда тория , которая начинается с родительского изотопа 232 Th и заканчивается стабильным изотопом свинца 208 Pb . Другой изотоп актиния ( 225 Ac) временно присутствует в цепочке распада ряда нептуния , начиная с 237 Np (или 233 U ) и заканчивая таллием ( 205 Tl ) и почти стабильным висмутом ( 209 Bi ); хотя весь первичный 237 Np распался, он постоянно образуется в результате реакций выбивания нейтронов на природном 238 U.
Низкая природная концентрация и близкое сходство физических и химических свойств со свойствами лантана и других лантаноидов, которых всегда много в актинийсодержащих рудах, делают отделение актиния от руды непрактичным. Наиболее концентрированный образец актиния, приготовленный из сырья, содержал 7 микрограмм 227 Ac и менее 0,1 миллиграмма La 2 O 3 , и полного разделения так и не удалось достичь. [41] Вместо этого актиний в миллиграммовых количествах получают нейтронным облучением 226 Ra в ядерном реакторе . [40] [42]
Выход реакции составляет около 2% от массы радия. 227 Ac может дополнительно захватывать нейтроны, в результате чего образуются небольшие количества 228 Ac. После синтеза актиний отделяется от радия и продуктов распада и ядерного синтеза, таких как торий, полоний, свинец и висмут. Экстракцию можно проводить теноилтрифторацетон - бензольным раствором из водного раствора продуктов радиации, а селективность по определенному элементу достигается регулированием рН (около 6,0 для актиния). [39] Альтернативной процедурой является анионный обмен с соответствующей смолой в азотной кислоте , что может привести к коэффициенту разделения 1 000 000 для радия и актиния по сравнению с торием в двухстадийном процессе. Затем актиний можно отделить от радия в соотношении около 100, используя катионообменную смолу с низкой степенью поперечных связей и азотную кислоту в качестве элюента . [43]
225 Ac был впервые получен искусственно в Институте трансурановых элементов (ITU) в Германии с использованием циклотрона и в больнице Святого Георгия в Сиднее с использованием линейного ускорителя в 2000 году. [44] Этот редкий изотоп имеет потенциальное применение в лучевой терапии и наиболее эффективно производится. бомбардировкой мишени из радия-226 ионами дейтерия с энергией 20–30 МэВ . Эта реакция также дает 226 Ac, который, однако, распадается с периодом полураспада 29 часов и, таким образом, не загрязняет 225 Ac. [45]
Металлический актиний был получен восстановлением фторида актиния парами лития в вакууме при температуре от 1100 до 1300 °C. Более высокие температуры приводят к испарению продукта, а более низкие – к неполному превращению. Литий был выбран среди других щелочных металлов, поскольку его фторид наиболее летуч. [14] [17]
Из-за своей редкости, высокой цены и радиоактивности 227 Ac в настоящее время не имеет значительного промышленного применения, но в настоящее время 225 Ac изучается на предмет использования в лечении рака, например, в таргетной альфа-терапии. [14] [28] 227 Ac обладает высокой радиоактивностью и поэтому изучался для использования в качестве активного элемента радиоизотопных термоэлектрических генераторов , например, в космических кораблях. Оксид 227 Ас, спрессованный с бериллием, также является эффективным источником нейтронов , активность которого превышает активность стандартных пар америций-бериллий и радий-бериллий. [46] Во всех этих приложениях 227 Ac (бета-источник) является просто предшественником, который при своем распаде генерирует альфа-излучающие изотопы. Бериллий захватывает альфа-частицы и испускает нейтроны благодаря своему большому сечению ядерной реакции (α,n):
Источники нейтронов 227 AcBe можно применять в нейтронном зонде – стандартном устройстве для измерения количества воды, присутствующей в почве, а также влажности/плотности для контроля качества при строительстве дорог. [47] [48] Такие зонды также используются при каротаже скважин, в нейтронной радиографии , томографии и других радиохимических исследованиях. [49]
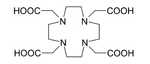
225 Ac применяется в медицине для получения 213 Bi в многоразовом генераторе [43] или может использоваться отдельно в качестве агента для лучевой терапии , в частности таргетной альфа-терапии (ТАТ). Период полураспада этого изотопа составляет 10 дней, что делает его более подходящим для лучевой терапии, чем Bi -213 (период полураспада 46 минут). [28] Кроме того, 225 Ac распадается на нетоксичный 209 Bi, а не на токсичный свинец , который является конечным продуктом в цепочках распада нескольких других изотопов-кандидатов, а именно 227 Th, 228 Th и 230 U. [28] Не только 225 Ac сама по себе, но и ее дочерние частицы испускают альфа-частицы, которые убивают раковые клетки в организме. Основная трудность применения 225 Ас заключалась в том, что внутривенное введение простых комплексов актиния приводило к их накоплению в костях и печени на протяжении десятков лет. В результате после того, как раковые клетки были быстро уничтожены альфа-частицами 225 Ac, излучение актиния и его дочерних клеток могло вызвать новые мутации. Чтобы решить эту проблему, 225 Ac связали с хелатирующим агентом, таким как цитрат , этилендиаминтетрауксусная кислота (ЭДТА) или диэтилентриаминпентауксусная кислота (ДТПА). Это уменьшало накопление актиния в костях, но выведение из организма оставалось медленным. Гораздо лучшие результаты были получены с такими хелатирующими агентами, как НЕНА ( 1,4,7,10,13,16-гексаазациклогексадекан-N,N',N″,N‴,N‴',N‴″-гексауксусная кислота ) [50 ] или DOTA ( 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусная кислота ) в сочетании с трастузумабом , моноклональным антителом , которое вмешивается в рецептор HER2/neu . Последняя комбинация была протестирована на мышах и доказала свою эффективность против лейкемии , лимфомы , рака молочной железы , яичников , нейробластомы и рака простаты . [51] [52] [53]
Средний период полураспада 227 Ac (21,77 года) делает его очень удобным радиоактивным изотопом для моделирования медленного вертикального перемешивания океанических вод. Сопутствующие процессы не могут быть изучены с необходимой точностью путем прямых измерений скоростей течений (порядка 50 метров в год). Однако оценка профилей концентрации по глубине для различных изотопов позволяет оценить скорости смешивания. Физика этого метода такова: океанические воды содержат однородно дисперсный 235 U. Продукт его распада 231 Па постепенно оседает на дно, так что его концентрация сначала увеличивается с глубиной, а затем остается почти постоянной. 231 Па распадается до 227 Ac; однако концентрация последнего изотопа не соответствует профилю глубины 231 Па, а увеличивается по направлению к морскому дну. Это происходит из-за процессов перемешивания, в результате которых со дна моря поднимается некоторое количество дополнительного 227 Ac. Таким образом, анализ глубинных профилей как 231 Па, так и 227 Ac позволяет исследователям моделировать поведение смешивания. [54] [55]
Существуют теоретические предсказания, что гидриды AcH x (в данном случае с очень высоким давлением) являются кандидатами на роль сверхпроводника при температуре, близкой к комнатной, поскольку их T c значительно выше, чем H 3 S, возможно, около 250 К. [56]
227 Ac высокорадиоактивен, и эксперименты с ним проводятся в специально оборудованной лаборатории, оборудованной герметичным перчаточным боксом . При внутривенном введении трихлорида актиния крысам около 33% актиния откладывается в костях и 50% - в печени. Его токсичность сравнима с токсичностью америция и плутония, но несколько ниже. [57] Для следовых количеств достаточно вытяжных шкафов с хорошей аэрацией; для граммовых количеств необходимы горячие камеры с защитой от интенсивного гамма-излучения, испускаемого 227 Ac. [58]
{{cite book}}: |journal=игнорируется ( помощь )