Уран — химический элемент с символом U и атомным номером 92. Это серебристо-серый металл из ряда актиноидов периодической таблицы . Атом урана имеет 92 протона и 92 электрона , из которых 6 являются валентными электронами . Уран радиоактивно распадается , обычно испуская альфа-частицу . Период полураспада этого распада варьируется от 159 200 до 4,5 миллиардов лет для разных изотопов , что делает их полезными для датирования возраста Земли . Наиболее распространенными изотопами в природном уране являются уран-238 (который имеет 146 нейтронов и составляет более 99% урана на Земле) и уран-235 (который имеет 143 нейтрона). Уран имеет самый высокий атомный вес среди изначально встречающихся элементов. Его плотность примерно на 70% выше, чем у свинца , и немного ниже, чем у золота или вольфрама . Он встречается в природе в низких концентрациях, несколько частей на миллион, в почве, горных породах и воде, и добывается в промышленных масштабах из урансодержащих минералов , таких как уранинит . [9]
Многие современные применения урана используют его уникальные ядерные свойства. Уран-235 является единственным естественным делящимся изотопом , что делает его широко используемым на атомных электростанциях и в ядерном оружии . Однако из-за низкой распространенности урана-235 в природном уране (который, в подавляющем большинстве, представляет собой уран-238), уран необходимо обогащать , чтобы присутствовало достаточно урана-235. Уран-238 делится быстрыми нейтронами и является фертильным , то есть его можно преобразовать в делящийся плутоний-239 в ядерном реакторе . Другой делящийся изотоп, уран-233 , может быть получен из природного тория и изучается для будущего промышленного использования в ядерной технологии. Уран-238 имеет небольшую вероятность спонтанного деления или даже вынужденного деления быстрыми нейтронами; уран-235 и в меньшей степени уран-233 имеют гораздо более высокое сечение деления для медленных нейтронов. При достаточной концентрации эти изотопы поддерживают устойчивую ядерную цепную реакцию . Это генерирует тепло в ядерных энергетических реакторах и производит расщепляющийся материал для ядерного оружия. Основное гражданское использование урана заключается в использовании тепловой энергии для производства электроэнергии. Обедненный уран ( 238 U) используется в кинетических проникающих элементах и броневых покрытиях . [10]
Открытие урана в 1789 году в минерале урана приписывают Мартину Генриху Клапроту , который назвал новый элемент в честь недавно открытой планеты Уран . Эжен-Мельхиор Пелиго был первым человеком, который изолировал металл, а его радиоактивные свойства были обнаружены в 1896 году Анри Беккерелем . Исследования Отто Гана , Лизы Мейтнер , Энрико Ферми и других, таких как Дж. Роберт Оппенгеймер, начатые в 1934 году, привели к его использованию в качестве топлива в ядерной энергетике и в «Малыше» , первом ядерном оружии, использованном на войне . Последовавшая гонка вооружений во время холодной войны между Соединенными Штатами и Советским Союзом произвела десятки тысяч единиц ядерного оружия, в котором использовался металлический уран и полученный из урана плутоний-239 . Демонтаж этого оружия и связанных с ним ядерных объектов осуществляется в рамках различных программ ядерного разоружения и обходится в миллиарды долларов. Оружейный уран, полученный из ядерного оружия, разбавляется ураном-238 и повторно используется в качестве топлива для ядерных реакторов. Отработанное ядерное топливо образует радиоактивные отходы , которые в основном состоят из урана-238 и представляют значительную угрозу для здоровья и окружающей среды .

Уран — серебристо-белый, слаборадиоактивный металл . Его твёрдость по шкале Мооса равна 6, что достаточно для того, чтобы поцарапать стекло, и примерно равна твёрдости титана , родия , марганца и ниобия . Он ковкий , пластичный , слегка парамагнитный , сильно электроположительный и плохой проводник электричества . [11] [12] Металлический уран имеет очень высокую плотность — 19,1 г/см3 , [ 13] плотнее свинца (11,3 г/см3 ) , [14] но немного менее плотный, чем вольфрам и золото (19,3 г/см3 ) . [15] [16]
Металлический уран реагирует почти со всеми неметаллическими элементами (кроме благородных газов ) и их соединениями , при этом реакционная способность увеличивается с температурой. [17] Соляная и азотная кислоты растворяют уран, но неокисляющие кислоты, отличные от соляной кислоты, воздействуют на элемент очень медленно. [11] При тонком измельчении он может реагировать с холодной водой; на воздухе металлический уран покрывается темным слоем оксида урана . [12] Уран в рудах извлекается химическим путем и преобразуется в диоксид урана или другие химические формы, пригодные для использования в промышленности.
Уран-235 был первым изотопом, который, как было обнаружено, является делящимся . Другие встречающиеся в природе изотопы делятся, но не делятся. При бомбардировке медленными нейтронами уран-235 большую часть времени распадается на два меньших ядра , высвобождая ядерную энергию связи и больше нейтронов. Если слишком много этих нейтронов поглощается другими ядрами урана-235, происходит цепная ядерная реакция , которая приводит к выбросу тепла или (в некоторых обстоятельствах) взрыву. В ядерном реакторе такая цепная реакция замедляется и контролируется нейтронным ядом , поглощающим часть свободных нейтронов. Такие поглощающие нейтроны материалы часто являются частью стержней управления реактором (см. физику ядерного реактора для описания этого процесса управления реактором).
Для создания атомной бомбы можно использовать всего 15 фунтов (6,8 кг) урана-235. [18] Ядерное оружие, взорванное над Хиросимой , названное «Малыш» , основывалось на делении урана. Однако первая ядерная бомба ( Gadget, использованная в Тринити ) и бомба, взорванная над Нагасаки ( Fat Man ), были плутониевыми бомбами.
Металлический уран имеет три аллотропные формы: [19]

Основное применение урана в военном секторе — в высокоплотных пенетраторах. Эти боеприпасы состоят из обедненного урана (DU), легированного 1–2% других элементов, таких как титан или молибден . [21] При высокой скорости удара плотность, твердость и пирофорность снаряда позволяют уничтожать тяжелобронированные цели. Броня танков и другая съемная броня транспортных средств также может быть укреплена пластинами из обедненного урана. Использование обедненного урана стало политически и экологически спорным после того, как использование таких боеприпасов США, Великобританией и другими странами во время войн в Персидском заливе и на Балканах подняло вопросы относительно соединений урана, остающихся в почве (см. Синдром войны в Персидском заливе ). [18]
Обедненный уран также используется в качестве защитного материала в некоторых контейнерах, используемых для хранения и транспортировки радиоактивных материалов. Хотя сам металл радиоактивен, его высокая плотность делает его более эффективным, чем свинец, в остановке радиации от мощных источников, таких как радий . [11] Другие применения обедненного урана включают противовесы для поверхностей управления самолетами, в качестве балласта для боеголовок ракет и в качестве защитного материала. [12] Благодаря своей высокой плотности этот материал используется в инерциальных системах наведения и в гироскопических компасах . [12] Обедненный уран предпочтительнее металлов с такой же плотностью из-за его способности легко обрабатываться и отливаться, а также из-за его относительно низкой стоимости. [22] Основной риск воздействия обедненного урана — это химическое отравление оксидом урана, а не радиоактивность (уран является лишь слабым альфа-излучателем ).
На поздних этапах Второй мировой войны , всей Холодной войны и в меньшей степени после нее уран-235 использовался в качестве расщепляющегося взрывчатого вещества для производства ядерного оружия. Первоначально были построены два основных типа бомб деления: относительно простое устройство, использующее уран-235, и более сложный механизм, использующий плутоний-239 , полученный из урана-238. Позже был построен гораздо более сложный и гораздо более мощный тип бомбы деления/синтеза ( термоядерное оружие ), использующий устройство на основе плутония, чтобы заставить смесь трития и дейтерия подвергнуться ядерному синтезу . Такие бомбы заключены в нерасщепляющийся (необогащенный) урановый корпус, и они получают более половины своей мощности от деления этого материала быстрыми нейтронами из процесса ядерного синтеза. [23]
Основное применение урана в гражданском секторе — это топливо для атомных электростанций . Один килограмм урана-235 теоретически может произвести около 20 тераджоулей энергии (2 × 1013 джоулей ), предполагая полное деление; столько же энергии , сколько 1,5 миллиона килограммов (1500 тонн ) угля . [10]
Коммерческие атомные электростанции используют топливо, которое обычно обогащено примерно до 3% урана-235. [10] Конструкции CANDU и Magnox являются единственными коммерческими реакторами, способными использовать необогащенное урановое топливо. Топливо, используемое для реакторов ВМС США , обычно высокообогащено ураном-235 (точные значения засекречены ). В реакторе-размножителе уран-238 также может быть преобразован в плутоний-239 посредством следующей реакции: [12]

До (а иногда и после) открытия радиоактивности уран в основном использовался в небольших количествах для производства желтого стекла и керамической глазури, например, уранового стекла , а также в посуде для праздников . [24]
Открытие и выделение радия из урановой руды (урановой смолки) Марией Кюри послужило толчком к развитию добычи урана для извлечения радия, который использовался для изготовления светящихся в темноте красок для циферблатов часов и самолетов. [25] [26] Это оставило колоссальное количество урана в качестве отходов, поскольку для извлечения одного грамма радия требуется три тонны урана. Эти отходы были направлены в стекольную промышленность, что сделало урановые глазури очень недорогими и распространенными. Помимо гончарных глазурей, большую часть использования составляли урановые глазури для плитки , включая обычную плитку для ванных комнат и кухонь, которая может быть произведена в зеленом, желтом, лиловом , черном, синем, красном и других цветах.


Уран также использовался в фотографических химикатах (особенно нитрат урана в качестве тонера ), [12] в нитях накаливания лампочек для сценического освещения , [27] для улучшения внешнего вида зубных протезов , [28] и в кожевенной и деревообрабатывающей промышленности для получения пятен и красителей. Соли урана являются протравителями шелка или шерсти. Уранилацетат и уранилформиат используются в качестве электронно-плотных «пятен» в просвечивающей электронной микроскопии , для повышения контрастности биологических образцов в ультратонких срезах и при негативном окрашивании вирусов , изолированных клеточных органелл и макромолекул .
Открытие радиоактивности урана открыло новые возможности научного и практического использования этого элемента. Длительный период полураспада урана-238 (4,47 × 109 лет) делает его хорошо подходящим для использования при оценке возраста самых ранних магматических пород и для других типов радиометрического датирования , включая уран-ториевое датирование , уран-свинцовое датирование и уран-урановое датирование . Металлический уран используется для рентгеновских мишеней при создании высокоэнергетических рентгеновских лучей. [12]
Использование уранита , урана в форме его естественного оксида , восходит как минимум к 79 году н. э., когда он использовался в Римской империи для придания желтого цвета керамическим глазурям. [12] Желтое стекло с 1% оксида урана было найдено на римской вилле на мысе Позиллипо в Неаполитанском заливе , Италия, Р. Т. Гюнтером из Оксфордского университета в 1912 году. [29] Начиная с позднего Средневековья , уранит добывался на серебряных рудниках Габсбургов в Иоахимстале , Богемия (ныне Яхимов в Чешской Республике) в Рудных горах и использовался в качестве красителя в местной стекольной промышленности. [30] В начале 19 века единственными известными в мире источниками урановой руды были эти рудники.

Открытие элемента приписывают немецкому химику Мартину Генриху Клапроту . Работая в своей экспериментальной лаборатории в Берлине в 1789 году, Клапрот смог выделить желтое соединение (вероятно, диуранат натрия ), растворив урановую смолку в азотной кислоте и нейтрализовав раствор гидроксидом натрия . [30] Клапрот предположил, что желтое вещество было оксидом еще не открытого элемента, и нагрел его с древесным углем, чтобы получить черный порошок, который, по его мнению, был самим недавно открытым металлом (на самом деле этот порошок был оксидом урана ). [30] [31] Он назвал недавно открытый элемент в честь планеты Уран (названной в честь древнегреческого бога неба ), которая была открыта восемью годами ранее Уильямом Гершелем . [32]
В 1841 году Эжен-Мельхиор Пелиго , профессор аналитической химии в Национальной консерватории искусств и ремесел (Центральная школа искусств и мануфактур) в Париже , выделил первый образец металлического урана путем нагревания тетрахлорида урана с калием . [30] [33]

Анри Беккерель открыл радиоактивность, используя уран в 1896 году. [17] Беккерель сделал открытие в Париже, оставив образец соли урана, K2UO2 ( SO4 ) 2 ( сульфат калия-уранил), на неэкспонированной фотографической пластинке в ящике и заметив, что пластинка «запотела». [34] Он определил, что форма невидимого света или лучей, испускаемых ураном, экспонировала пластинку .
Во время Первой мировой войны, когда Центральные державы испытывали нехватку молибдена для производства артиллерийских стволов и быстрорежущих инструментальных сталей, они обычно использовали сплав ферроурана в качестве замены, так как он обладает многими из тех же физических характеристик, что и молибден. Когда эта практика стала известна в 1916 году, правительство США попросило несколько известных университетов исследовать использование урана в производстве и металлообработке. Инструменты, изготовленные по этим формулам, использовались в течение нескольких десятилетий, [35] [36] пока Манхэттенский проект и Холодная война не предъявили большой спрос на уран для исследований деления и разработки оружия.

Группа под руководством Энрико Ферми в 1934 году обнаружила, что бомбардировка урана нейтронами производит бета-лучи ( электроны или позитроны из полученных элементов; см. бета-частица ). [37] Продукты деления сначала были ошибочно приняты за новые элементы с атомными номерами 93 и 94, которые декан Римского университета Ла Сапиенца Орсо Марио Корбино назвал аузением и гесперием соответственно. [38] [39] [40] [41] Эксперименты, приведшие к открытию способности урана делиться (распадаться) на более легкие элементы и высвобождать энергию связи, были проведены Отто Ганом и Фрицем Штрассманом [37] в лаборатории Гана в Берлине. Лиза Мейтнер и ее племянник, физик Отто Роберт Фриш , опубликовали физическое объяснение в феврале 1939 года и назвали процесс « делением ядра ». [42] Вскоре после этого Ферми выдвинул гипотезу, что деление урана может высвобождать достаточно нейтронов для поддержания реакции деления. Подтверждение этой гипотезы пришло в 1939 году, и более поздние работы показали, что в среднем около 2,5 нейтронов высвобождаются при каждом делении урана-235. [37] Ферми призвал Альфреда О.К. Нира разделить изотопы урана для определения делящегося компонента, и 29 февраля 1940 года Нир использовал прибор, который он построил в Университете Миннесоты , чтобы разделить первый в мире образец урана-235 в лаборатории Тейта. Используя циклотрон Колумбийского университета , Джон Даннинг 1 марта подтвердил, что образец является изолированным делящимся материалом. [43] Дальнейшие работы показали, что гораздо более распространенный изотоп урана-238 может быть преобразован в плутоний, который, как и уран-235, также делится тепловыми нейтронами. Эти открытия привели к тому, что многие страны начали работать над разработкой ядерного оружия и ядерной энергетики . Несмотря на то, что деление было открыто в Германии, проект Uranverein («урановый клуб») Германии военного времени по исследованию ядерной энергетики и/или оружия был затруднен из-за ограниченных ресурсов, внутренних распрей, изгнания или неучастия нескольких выдающихся ученых в этой области и нескольких важных ошибок, таких как неспособность учесть примеси в имеющихся образцах графита, из-за чего он казался менее подходящим в качестве замедлителя нейтронов.чем есть на самом деле. Попытки Германии построить реактор на природном уране / тяжелой воде не приблизились к достижению критичности к тому времени, когда американцы достигли Хайгерлоха , места последнего немецкого эксперимента с реактором во время войны. [44]
2 декабря 1942 года в рамках Манхэттенского проекта другая группа под руководством Энрико Ферми смогла инициировать первую искусственную самоподдерживающуюся цепную ядерную реакцию , Чикагскую поленницу-1 . Первоначальный план с использованием обогащенного урана-235 был заброшен, поскольку он еще не был доступен в достаточных количествах. [45] Работая в лаборатории под трибунами Стагг-Филд в Чикагском университете , группа создала необходимые для такой реакции условия, сложив вместе 360 тонн графита , 53 тонны оксида урана и 5,5 тонн металлического урана, большая часть которого была поставлена Westinghouse Lamp Plant в импровизированном производственном процессе. [37] [46]

Во время Второй мировой войны Соединенными Штатами были разработаны два типа атомной бомбы : устройство на основе урана (кодовое название « Малыш »), расщепляющимся материалом которого был высокообогащенный уран , и устройство на основе плутония (см. испытание «Тринити» и « Толстяк »), плутоний которого был получен из урана-238. «Малыш» стал первым ядерным оружием, использованным в войне, когда был взорван над Хиросимой , Япония , 6 августа 1945 года. Взорвавшись с мощностью, эквивалентной 12 500 тонн тротила , взрывная и тепловая волна бомбы разрушили около 50 000 зданий и убили около 75 000 человек (см. Атомные бомбардировки Хиросимы и Нагасаки ). [34] Первоначально считалось, что уран относительно редок, и что ядерного распространения можно избежать, просто скупив все известные запасы урана, но в течение десятилетия во многих местах по всему миру были обнаружены его крупные месторождения. [47]

Графитовый реактор X -10 в Окриджской национальной лаборатории (ORNL) в Окридже, штат Теннесси, ранее известный как Clinton Pile и X-10 Pile, был вторым в мире искусственным ядерным реактором (после Chicago Pile Энрико Ферми) и первым реактором, спроектированным и построенным для непрерывной работы. Экспериментальный реактор-размножитель I Аргоннской национальной лаборатории , расположенный на Национальной испытательной станции реакторов Комиссии по атомной энергии около Арко, штат Айдахо , стал первым ядерным реактором, выработавшим электричество 20 декабря 1951 года. [48] Первоначально реактор зажигал четыре 150-ваттные лампочки, но усовершенствования в конечном итоге позволили ему обеспечить питанием весь объект (позже город Арко стал первым в мире, где вся электроэнергия поступала от ядерной энергии, вырабатываемой BORAX-III , другим реактором, спроектированным и эксплуатируемым Аргоннской национальной лабораторией ). [49] [50] Первая в мире атомная электростанция коммерческого масштаба, Обнинская в Советском Союзе , начала выработку электроэнергии с помощью реактора АМ-1 27 июня 1954 года. Другими ранними атомными электростанциями были Колдер-Холл в Англии, которая начала выработку электроэнергии 17 октября 1956 года, [ 51] и АЭС Шиппингпорт в Пенсильвании , которая начала работу 26 мая 1958 года. Впервые ядерная энергия была использована для движения подводной лодкой USS Nautilus в 1954 году. [37] [52]
В 1972 году французский физик Франсис Перрен обнаружил пятнадцать древних и более не активных природных ядерных реакторов деления в трех отдельных рудных месторождениях на руднике Окло в Габоне , Африка, известных под общим названием Ископаемые реакторы Окло . Возраст рудного месторождения составляет 1,7 миллиарда лет; тогда уран-235 составлял около 3% урана на Земле. [53] Это достаточно много, чтобы обеспечить устойчивую цепную реакцию, если существуют другие поддерживающие условия. Способность окружающих отложений удерживать опасные для здоровья продукты ядерных отходов была процитирована федеральным правительством США в качестве подтверждающего доказательства целесообразности хранения отработанного ядерного топлива в хранилище ядерных отходов Юкка-Маунтин . [53]
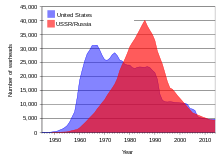
Наземные ядерные испытания, проведенные Советским Союзом и Соединенными Штатами в 1950-х и начале 1960-х годов, а также Францией в 1970-х и 1980-х годах [22], привели к значительному выпадению радиоактивных осадков из дочерних изотопов урана по всему миру. [54] Дополнительные радиоактивные осадки и загрязнение произошли в результате нескольких ядерных аварий . [55]
Урановые шахтеры имеют более высокую заболеваемость раком . Например, повышенный риск рака легких среди шахтеров -навахо , работающих на урановых рудниках, был задокументирован и связан с их профессией. [56] Закон о компенсации за радиационное воздействие , принятый в США в 1990 году, требовал выплаты 100 000 долларов в качестве «выплат из сострадания» шахтерам-урановодам, у которых диагностирован рак или другие респираторные заболевания. [57]
Во время Холодной войны между Советским Союзом и Соединенными Штатами были накоплены огромные запасы урана и десятки тысяч единиц ядерного оружия были созданы с использованием обогащенного урана и плутония, изготовленных из урана. После распада Советского Союза в 1991 году, по оценкам, 600 коротких тонн (540 метрических тонн) высокообогащенного оружейного урана (достаточно для изготовления 40 000 ядерных боеголовок) хранились на часто недостаточно охраняемых объектах в Российской Федерации и нескольких других бывших советских государствах. [18] Полиция в Азии , Европе и Южной Америке по крайней мере 16 раз с 1993 по 2005 год перехватывала партии контрабандного оружейного урана или плутония, большинство из которых было из бывших советских источников. [18] С 1993 по 2005 год Программа защиты, контроля и учета материалов , реализуемая федеральным правительством Соединенных Штатов , потратила около 550 миллионов долларов США на обеспечение сохранности запасов урана и плутония в России. Эти деньги были использованы на усовершенствования и повышение безопасности на исследовательских и складских объектах. [18]
Безопасность ядерных объектов в России значительно улучшилась после стабилизации политической и экономической нестабильности начала 1990-х годов. Например, в 1993 году произошло 29 инцидентов, классифицированных выше уровня 1 по Международной шкале ядерных событий , а в 1995–2003 годах это число сократилось до менее четырех в год. Количество сотрудников, получающих годовые дозы облучения свыше 20 мЗв , что эквивалентно одному КТ всего тела , [58] резко сократилось около 2000 года. В ноябре 2015 года правительство России утвердило федеральную программу по ядерной и радиационной безопасности на 2016–2030 годы с бюджетом в 562 млрд рублей (около 8 млрд долларов США ). Ее ключевым вопросом является «отложенные обязательства, накопленные за 70 лет атомной промышленности, особенно во времена Советского Союза». Около 73% бюджета будет потрачено на вывод из эксплуатации устаревших и отслуживших свой срок ядерных реакторов и ядерных установок, особенно задействованных в государственных оборонных программах; 20% — на переработку и утилизацию ядерного топлива и радиоактивных отходов, 5% — на контроль и обеспечение ядерной и радиационной безопасности. [59]
Уран — это встречающийся в природе элемент, который в небольших количествах содержится во всех горных породах, почве и воде. Это самый высокопоставленный элемент, который естественным образом встречается в значительных количествах на Земле и почти всегда встречается в сочетании с другими элементами. [12] Уран — 48-й по распространенности элемент в земной коре. [60] Распад урана, тория и калия-40 в мантии Земли считается основным источником тепла [61] [62] , которое поддерживает внешнее ядро Земли в жидком состоянии и управляет конвекцией мантии , которая, в свою очередь, управляет тектоникой плит .
Концентрация урана в земной коре составляет (в зависимости от источника) от 2 до 4 частей на миллион [11] [22], или примерно в 40 раз больше, чем серебра . [17] Подсчитано, что земная кора от поверхности до глубины 25 км (15 миль) содержит 10 17 кг (2 × 1017 фунтов) урана, в то время как океаны могут содержать 10 13 кг (2 × 1013 фунтов). [11] Концентрация урана в почве колеблется от 0,7 до 11 частей на миллион (до 15 частей на миллион в почве сельскохозяйственных угодий из-за использования фосфатных удобрений ), [63] а его концентрация в морской воде составляет 3 части на миллиард. [22]
Уран более распространен, чем сурьма , олово , кадмий , ртуть или серебро, и примерно так же распространен, как мышьяк или молибден . [12] [22] Уран содержится в сотнях минералов, включая уранинит (наиболее распространенная урановая руда ), карнотит , аутунит , уранофан , торбернит и коффинит . [12] Значительные концентрации урана встречаются в некоторых веществах, таких как месторождения фосфатных пород, и минералах, таких как лигнит и монацитовые пески в богатых ураном рудах [12] (его извлекают в промышленных масштабах из источников с содержанием урана всего лишь 0,1% [17] ).
Как и все элементы с атомным весом выше, чем у железа , уран естественным образом образуется только в результате r-процесса (быстрый захват нейтронов) при слияниях сверхновых и нейтронных звезд . [64] Первичный торий и уран производятся только в результате r-процесса, поскольку s-процесс (медленный захват нейтронов) слишком медленный и не может пройти через промежуток нестабильности после висмута. [65] [66] Помимо двух существующих первичных изотопов урана, 235 U и 238 U, r-процесс также производит значительные количества 236 U , который имеет более короткий период полураспада и поэтому является вымершим радионуклидом , давно уже полностью распавшимся до 232 Th. Кроме того, уран-236 был произведен в результате распада 244 Pu , что объясняет наблюдаемое более высокое, чем ожидалось, содержание тория и более низкое, чем ожидалось, содержание урана. [67] Хотя естественное изобилие урана было дополнено распадом вымерших 242 Pu (период полураспада 375 000 лет) и 247 Cm (период полураспада 16 миллионов лет), в результате чего образовались 238 U и 235 U соответственно, это произошло в почти ничтожной степени из-за более коротких периодов полураспада этих родительских элементов и их более низкого производства, чем у 236 U и 244 Pu, родительских элементов тория: соотношение 247 Cm/ 235 U при формировании Солнечной системы было(7,0 ± 1,6) × 10 −5 . [68]


Некоторые бактерии, такие как Shewanella putrefaciens , Geobacter metallireducens и некоторые штаммы Burkholderia fungorum , используют уран для своего роста и преобразуют U(VI) в U(IV). [69] [70] Недавние исследования показывают, что этот путь включает восстановление растворимого U(VI) через промежуточное пятивалентное состояние U(V). [71] [72] Другие организмы, такие как лишайник Trapelia involuta или микроорганизмы, такие как бактерия Citrobacter , могут поглощать концентрации урана, которые в 300 раз превышают уровень их окружающей среды. [73] Виды Citrobacter поглощают ионы уранила при введении им фосфата глицерина (или других подобных органических фосфатов). Через день один грамм бактерий может покрыться коркой из девяти граммов кристаллов уранилфосфата; это создает возможность того, что эти организмы могут быть использованы в биоремедиации для дезактивации воды, загрязненной ураном. [30] [74] Также было показано, что протеобактерия Geobacter биоремедиирует уран в грунтовых водах. [75] Микоризный гриб Glomus intraradices увеличивает содержание урана в корнях своего симбиотического растения. [76]
В природе уран(VI) образует высокорастворимые карбонатные комплексы при щелочном pH. Это приводит к увеличению подвижности и доступности урана для грунтовых вод и почвы из ядерных отходов, что приводит к опасности для здоровья. Однако трудно осаждать уран в виде фосфата в присутствии избытка карбоната при щелочном pH. Было обнаружено, что штамм Sphingomonas sp. BSAR-1 экспрессирует высокоактивную щелочную фосфатазу (PhoK), которая применялась для биопреципитации урана в виде уранилфосфатных видов из щелочных растворов. Способность к осаждению была усилена за счет сверхэкспрессии белка PhoK в E. coli . [77]
Растения поглощают некоторое количество урана из почвы. Концентрация урана в растениях в сухом весе составляет от 5 до 60 частей на миллиард, а зола от сожженной древесины может иметь концентрацию до 4 частей на миллион. [30] Концентрация урана в сухом весе в пищевых растениях обычно ниже, с пищей, которую потребляют люди, в количестве от одного до двух микрограммов в день. [30]
Мировое производство урана в 2021 году составило 48 332 тонны , из которых 21 819 тонн (45%) было добыто в Казахстане . Другими важными странами-добытчиками урана являются Намибия (5 753 тонны), Канада (4 693 тонны), Австралия (4 192 тонны), Узбекистан (3 500 тонн) и Россия (2 635 тонн). [78]
Урановая руда добывается несколькими способами: открытым способом , под землей , выщелачиванием на месте и скважинной добычей . [10] Низкосортная урановая руда обычно содержит от 0,01 до 0,25% оксидов урана. Для извлечения металла из руды необходимо применять обширные меры. [79] Высокосортные руды, обнаруженные в месторождениях бассейна Атабаска в Саскачеване , Канада, могут содержать в среднем до 23% оксидов урана. [80] Урановую руду измельчают и превращают в мелкий порошок, а затем выщелачивают либо кислотой , либо щелочью . Выщелачивающий продукт подвергают одной из нескольких последовательностей осаждения, экстракции растворителем и ионного обмена. Полученная смесь, называемая желтым кеком , содержит не менее 75% оксидов урана U3O8 . Затем желтый кек прокаливают для удаления примесей из процесса измельчения перед очисткой и конверсией. [81]
Коммерческий уран может быть получен путем восстановления галогенидов урана щелочными или щелочноземельными металлами . [12] Металлический уран также может быть получен путем электролиза KUF .
5или УФ4, растворенный в расплавленном хлориде кальция ( CaCl
2) и раствор хлорида натрия ( NaCl ). [12] Очень чистый уран получается путем термического разложения галогенидов урана на горячей нити. [12]

По оценкам, 6,1 млн тонн урана содержится в рудах, добыча которых экономически выгодна при цене 130 долларов США за кг урана [83] , в то время как 35 млн тонн классифицируются как минеральные ресурсы (разумные перспективы для возможной экономической добычи) [84] .
В Австралии находится 28% известных мировых запасов урановой руды [83] , а крупнейшее в мире месторождение урана находится на руднике Олимпик-Дэм в Южной Австралии . [85] Значительные запасы урана имеются в Бакуме , субпрефектуре в префектуре Мбому в Центральноафриканской Республике . [86]
Часть урана также поступает из демонтированного ядерного оружия. [87] Например, в 1993–2013 годах Россия поставила в США 15 000 тонн низкообогащенного урана в рамках программы «Мегатонны в мегаватты» . [88]
По оценкам, еще 4,6 млрд тонн урана растворены в морской воде ( японские ученые в 1980-х годах показали, что извлечение урана из морской воды с использованием ионообменников технически осуществимо). [89] [90] Были проведены эксперименты по извлечению урана из морской воды, [91] но выход был низким из-за карбоната, присутствующего в воде. В 2012 году исследователи ORNL объявили об успешной разработке нового абсорбирующего материала, названного HiCap, который выполняет поверхностное удержание твердых или газообразных молекул, атомов или ионов, а также эффективно удаляет токсичные металлы из воды, согласно результатам, подтвержденным исследователями из Тихоокеанской северо-западной национальной лаборатории . [92] [93]
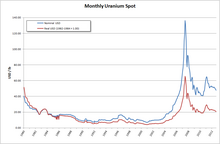
В 2005 году на долю десяти стран приходилось большинство мировых запасов концентрированных оксидов урана: Канада (27,9%), Австралия (22,8%), Казахстан (10,5%), Россия (8,0%), Намибия (7,5%), Нигер (7,4%), Узбекистан (5,5%), США (2,5%), Аргентина (2,1%) и Украина (1,9%). [95] В 2008 году прогнозировалось, что Казахстан увеличит добычу и станет крупнейшим в мире поставщиком урана к 2009 году; [96] [97] Казахстан доминирует на мировом рынке урана с 2010 года. В 2021 году его доля составила 45,1%, за ним следуют Намибия (11,9%), Канада (9,7%), Австралия (8,7%), Узбекистан (7,2%), Нигер (4,7%), Россия (5,5%), Китай (3,9%), Индия (1,3%), Украина (0,9%) и Южная Африка (0,8%), с общим мировым производством 48 332 тонн. [78] Большая часть урана была добыта не путем традиционной подземной добычи руды (29% добычи), а методом подземного выщелачивания (66%). [78] [98]
В конце 1960-х годов геологи ООН обнаружили крупные месторождения урана и другие редкие минеральные запасы в Сомали . Находка была крупнейшей в своем роде, и отраслевые эксперты оценили месторождения в более чем 25% от известных тогда мировых запасов урана в 800 000 тонн. [99]
Предполагается, что конечный доступный запас будет достаточным по крайней мере на следующие 85 лет, [84] хотя некоторые исследования указывают на то, что недостаточное инвестирование в конце двадцатого века может привести к проблемам с поставками в XXI веке. [100] Месторождения урана, по-видимому, распределены логарифмически нормально. Количество извлекаемого урана увеличивается в 300 раз на каждое десятикратное уменьшение содержания руды. [101] Другими словами, доступно мало высокосортной руды и пропорционально гораздо больше низкосортной руды.
Прокаленный желтый урановый кек, который производится на многих крупных заводах, содержит распределение видов окисления урана в различных формах, от наиболее окисленных до наименее окисленных. Частицы с коротким временем пребывания в кальцинаторе, как правило, будут менее окисленными, чем те, которые имеют длительное время удержания или частицы, извлеченные в скруббере дымовой трубы. Содержание урана обычно ссылается на U
3О
8, которая восходит к временам Манхэттенского проекта, когда U
3О
8использовался как стандарт отчетности по аналитической химии. [102]
Фазовые соотношения в системе уран-кислород сложны. Наиболее важными степенями окисления урана являются уран(IV) и уран(VI), а их два соответствующих оксида — это, соответственно, диоксид урана ( UO
2) и триоксид урана ( UO
3). [103] Другие оксиды урана, такие как оксид урана (UO), пентоксид диурана ( U
2О
5) и перекись урана ( UO
4·2H
2О ) также существуют.
Наиболее распространенными формами оксида урана являются октаоксид триурана ( U
3О
8) и УО
2. [104] Обе формы оксида являются твердыми веществами, которые имеют низкую растворимость в воде и относительно стабильны в широком диапазоне условий окружающей среды. Оксид триурана является (в зависимости от условий) наиболее стабильным соединением урана и является формой, наиболее часто встречающейся в природе. Диоксид урана является формой, в которой уран чаще всего используется в качестве топлива для ядерных реакторов. [104] При температуре окружающей среды UO
2постепенно перейдет в U
3О
8. Благодаря своей стабильности оксиды урана обычно считаются предпочтительной химической формой для хранения или утилизации. [104]

Соли многих степеней окисления урана растворимы в воде и могут быть изучены в водных растворах . Наиболее распространенными ионными формами являются U3+
(коричнево-красный), У4+
(зеленый), УО+
2(нестабильный) и UO2+
2(желтый) для U(III), U(IV), U(V) и U(VI) соответственно. [105] Для формальной степени окисления урана(II) существует несколько твердых и полуметаллических соединений, таких как UO и US , но не известно, чтобы простые ионы существовали в растворе для этого состояния. Ионы U3+
выделяют водород из воды и поэтому считаются крайне нестабильными. UO2+
2Ион представляет состояние урана (VI) и, как известно, образует такие соединения, как уранилкарбонат , уранилхлорид и уранилсульфат . UO2+
2также образует комплексы с различными органическими хелатирующими агентами, наиболее часто встречающимся из которых является ацетат уранила . [105]
В отличие от солей уранила урана и катионных форм многоатомного иона оксида урана, уранаты , соли, содержащие многоатомный анион оксида урана, как правило, не растворяются в воде.
Взаимодействие карбонатных анионов с ураном(VI) приводит к тому, что диаграмма Пурбе сильно меняется при изменении среды с воды на раствор, содержащий карбонат. В то время как подавляющее большинство карбонатов нерастворимы в воде (студентов часто учат, что все карбонаты, кроме карбонатов щелочных металлов, нерастворимы в воде), карбонаты урана часто растворимы в воде. Это происходит потому, что катион U(VI) способен связывать два конечных оксида и три или более карбонатов, образуя анионные комплексы.
Диаграммы распределения урана в присутствии карбоната иллюстрируют это еще раз: при повышении pH раствора урана (VI) уран превращается в гидратированный гидроксид оксида урана, а при высоких значениях pH он становится анионным гидроксидным комплексом.
При добавлении карбоната уран преобразуется в ряд карбонатных комплексов, если pH увеличивается. Одним из эффектов этих реакций является повышенная растворимость урана в диапазоне pH от 6 до 8, что имеет прямое отношение к долгосрочной стабильности отработанного ядерного топлива из диоксида урана.
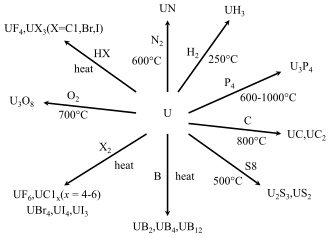
Металлический уран, нагретый до 250–300 °C (482–572 °F), реагирует с водородом, образуя гидрид урана . Даже более высокие температуры обратимо удаляют водород. Это свойство делает гидриды урана удобными исходными материалами для создания реактивного уранового порошка вместе с различными карбидом урана , нитридами и галогенидными соединениями. [107] Существуют две кристаллические модификации гидрида урана: α-форма, которая получается при низких температурах, и β-форма, которая создается, когда температура образования превышает 250 °C. [107]
Карбиды и нитриды урана являются относительно инертными полуметаллическими соединениями, которые минимально растворимы в кислотах , реагируют с водой и могут воспламеняться на воздухе с образованием U
3О
8. [107] Карбиды урана включают монокарбид урана (UC ) , дикарбид урана ( UC
2) и трикарбид диурана ( U
2С
3). Оба UC и UC
2образуются при добавлении углерода к расплавленному урану или при воздействии на металл оксида углерода при высоких температурах. Устойчивы ниже 1800 °C, U
2С
3готовят путем воздействия нагретой смеси UC и UC
2к механическому напряжению. [108] Нитриды урана, полученные путем прямого воздействия азота на металл, включают мононитрид урана (UN), динитрид урана ( UN
2) и тринитрид диурана ( U
2Н
3). [108]

Все фториды урана создаются с использованием тетрафторида урана ( UF
4); УФ
4Сам по себе получен путем гидрофторирования диоксида урана. [107] Восстановление UF
4с водородом при 1000 °C образует трифторид урана ( UF
3). При правильных условиях температуры и давления реакция твердого UF
4с газообразным гексафторидом урана ( UF
6) могут образовывать промежуточные фториды U
2Ф
9, У
4Ф
17, и УФ5. [107]
При комнатной температуре УФ
6имеет высокое давление паров , что делает его полезным в процессе газовой диффузии для отделения редкого урана-235 от обычного изотопа урана-238. Это соединение может быть получено из диоксида урана и гидрида урана следующим способом: [107]
Полученный UF
6, белое твердое вещество, очень реакционноспособно (при фторировании), легко возгоняется (выделяя пар, который ведет себя как почти идеальный газ ) и является самым летучим соединением урана, известным из существующих. [107]
Один из методов получения тетрахлорида урана ( UCl
4) заключается в непосредственном соединении хлора либо с металлическим ураном, либо с гидридом урана. Восстановление UCl
4водородом производит трихлорид урана ( UCl
3), тогда как высшие хлориды урана получаются путем реакции с дополнительным хлором. [107] Все хлориды урана реагируют с водой и воздухом.
Бромиды и иодиды урана образуются при прямой реакции соответственно брома и иода с ураном или при добавлении UH
3к кислотам этих элементов. [107] Известные примеры включают: UBr3, UBr4, Пользовательский интерфейс
3и пользовательский интерфейс
4. Пользовательский интерфейс
5никогда не был подготовлен. Оксигалогениды урана растворимы в воде и включают UO
2Ф
2, UOCl
2, УО
2Кл
2, и UO2Br2. Стабильность оксигалогенидов уменьшается с увеличением атомного веса галогенида компонента. [107]
Уран, как и все элементы с атомным числом больше 82, не имеет стабильных изотопов . Все изотопы урана радиоактивны , поскольку сильная ядерная сила не преобладает над электромагнитным отталкиванием в нуклидах, содержащих более 82 протонов. [109] Тем не менее, два самых стабильных изотопа, 238 U и 235 U, имеют периоды полураспада, достаточно длинные, чтобы встречаться в природе в качестве первичных радионуклидов , с измеримыми количествами, сохранившимися с момента образования Земли. [110] Эти два нуклида , наряду с торием-232 , являются единственными подтвержденными первичными нуклидами, тяжелее почти стабильного висмута-209 . [7] [111]
Природный уран состоит из трех основных изотопов: уран-238 (99,28% естественной распространенности), уран-235 (0,71%) и уран-234 (0,0054%). Также существует пять других следовых изотопов: уран-240, продукт распада плутония -244 ; [111] уран-239, который образуется при спонтанном делении 238U, высвобождая нейтроны, которые захватываются другим атомом 238U ; уран-237, который образуется при захвате 238U нейтрона, но испускает еще два, который затем распадается на нептуний-237 ; уран-236 , который встречается в следовых количествах из-за захвата нейтронов 235U и как продукт распада плутония-244; [111] и, наконец, уран-233 , который образуется в цепочке распада нептуния-237. Кроме того, уран-232 может быть получен в результате двойного бета-распада природного тория-232 , хотя этот энергетически возможный процесс никогда не наблюдался. [114]
Уран-238 — наиболее стабильный изотоп урана с периодом полураспада около4,463 × 10 9 лет, [7] примерно возраст Земли . Уран-238 является преимущественно альфа-излучателем, распадаясь до тория-234. В конечном итоге он распадается через ряд урана , который состоит из 18 элементов, до свинца-206 . [17] Уран-238 не является делящимся, но является фертильным изотопом, потому что после активации нейтронами он может быть преобразован в плутоний-239, другой делящийся изотоп. Действительно, ядро 238 U может поглотить один нейтрон для получения радиоактивного изотопа урана-239 . 239 U распадается путем бета-излучения до нептуния -239, также бета-излучателя, который, в свою очередь, распадается в течение нескольких дней до плутония-239. 239 Pu использовался в качестве расщепляющегося материала в первой атомной бомбе , взорванной в ходе « испытания Тринити » 16 июля 1945 года в Нью-Мексико . [37]
Уран-235 имеет период полураспада около7,04 × 10 8 лет; это следующий по стабильности изотоп урана после 238 U, а также преимущественно альфа-излучатель, распадающийся до тория-231. [7] Уран-235 важен как для ядерных реакторов, так и для ядерного оружия , поскольку это единственный изотоп урана, существующий в природе на Земле в значительных количествах, который является делящимся. Это означает, что он может быть разделен на два или три фрагмента ( продукта деления ) тепловыми нейтронами. [17] Цепочка распада 235 U, которая называется рядом актиния , имеет 15 членов и в конечном итоге распадается до свинца-207. [17] Постоянные скорости распада в этих рядах распада делают сравнение соотношений родительских и дочерних элементов полезным при радиометрическом датировании.
Уран-236 имеет период полураспада2,342 × 10 7 лет [7] и не встречается в значительных количествах в природе. Период полураспада урана-236 слишком короток, чтобы он был первичным, хотя он был идентифицирован как вымерший предшественник своего дочернего альфа-распада, тория-232. [67] Уран-236 встречается в отработанном ядерном топливе , когда захват нейтронов на 235 U не вызывает деления, или как продукт распада плутония-240 . Уран-236 не является фертильным, так как для получения делящегося 239 Pu требуются еще три захвата нейтронов , и сам по себе не является делящимся; как таковой, он считается долгоживущими радиоактивными отходами. [115]
Уран-234 является членом ряда урана и находится в равновесии со своим предшественником 238U ; он претерпевает альфа-распад с периодом полураспада 245 500 лет [7] и распадается до свинца-206 через ряд относительно короткоживущих изотопов.
Уран-233 претерпевает альфа-распад с периодом полураспада 160 000 лет и, как и 235 U, является делящимся. [12] Его можно получить из тория-232 с помощью нейтронной бомбардировки, обычно в ядерном реакторе; этот процесс известен как ториевый топливный цикл . Благодаря делимости 233 U и большей естественной распространенности тория (в три раза больше, чем у урана), [116] 233 U исследовался для использования в качестве ядерного топлива в качестве возможной альтернативы 235 U и 239 Pu, [117] хотя по состоянию на 2022 год он не получил широкого распространения [обновлять]. [116] Цепочка распада урана-233 является частью ряда нептуния и заканчивается на почти стабильном висмуте-209 (период полураспада2,01 × 10 19 лет ) [7] и стабильный таллий -205.
Уран-232 является альфа-излучателем с периодом полураспада 68,9 лет. [7] Этот изотоп производится как побочный продукт при производстве 233 U и считается помехой, так как он не делится и распадается через короткоживущие альфа- и гамма-излучатели, такие как 208 Tl . [117] Также ожидается, что торий-232 должен быть способен подвергаться двойному бета-распаду , в результате чего образуется уран-232, но это пока не наблюдалось экспериментально. [7]
Все изотопы от 232 U до 236 U включительно имеют незначительные кластерные ветви распада (менее10−10 %), и все они, за исключением 233 U, в дополнение к 238 U, имеют второстепенные ветви спонтанного деления ; [7] наибольшее отношение ветвей для спонтанного деления составляет около5 × 10−5 % для 238 U, или примерно один на два миллиона распадов. [118] Более короткоживущие следовые изотопы 237 U и 239 U подвергаются исключительно бета-распаду , с соответствующими периодами полураспада 6,752 дня и 23,45 минуты. [7]
Всего было идентифицировано 28 изотопов урана, массовые числа которых варьируются от 214 [119] до 242, за исключением 220. [7] [120] Среди изотопов урана, не обнаруженных в природных образцах или ядерном топливе, самым долгоживущим является 230U , альфа-излучатель с периодом полураспада 20,23 дня. [7] Этот изотоп рассматривался для использования в таргетной альфа-частичной терапии (ТАТ). [121] Все остальные изотопы имеют период полураспада менее одного часа, за исключением 231U (период полураспада 4,2 дня) и 240U (период полураспада 14,1 часа). [7] Самым короткоживущим известным изотопом является 221U с периодом полураспада 660 наносекунд, и ожидается, что до сих пор неизвестный 220U имеет еще более короткий период полураспада. [122] Изотопы, богатые протонами, легче 232 U, в первую очередь подвергаются альфа-распаду, за исключением 229 U и 231 U, которые распадаются на изотопы протактиния посредством испускания позитронов и захвата электронов соответственно; изотопы, богатые нейтронами 240 U, 241 U и 242 U, подвергаются бета-распаду с образованием изотопов нептуния . [7] [120]

В природе уран встречается в виде урана-238 (99,2742%) и урана-235 (0,7204%). Разделение изотопов концентрирует (обогащает) делящийся уран-235 для ядерного оружия и большинства атомных электростанций, за исключением газоохлаждаемых реакторов и реакторов с тяжелой водой под давлением . Большинство нейтронов, испускаемых делящимся атомом урана-235, должны воздействовать на другие атомы урана-235, чтобы поддерживать ядерную цепную реакцию . Концентрация и количество урана-235, необходимые для достижения этого, называются « критической массой ».
Чтобы считаться «обогащенным», фракция урана-235 должна быть между 3% и 5%. [123] Этот процесс производит огромные количества урана, обедненного ураном-235 и с соответственно увеличенной фракцией урана-238, называемого обедненным ураном или «DU». Чтобы считаться «обедненным», концентрация урана- 235 должна быть не более 0,3%. [124] Цена на уран выросла с 2001 года, поэтому хвосты обогащения, содержащие более 0,35% урана-235, рассматриваются для повторного обогащения, в результате чего цена обедненного гексафторида урана превысила 130 долларов за килограмм в июле 2007 года с 5 долларов в 2001 году . [124]
Газоцентрифужная технология , в которой газообразный гексафторид урана ( UF
6) разделяется по разнице в молекулярном весе между 235 UF 6 и 238 UF 6 с использованием высокоскоростных центрифуг , является самым дешевым и ведущим процессом обогащения. [34] Процесс газовой диффузии был ведущим методом обогащения и использовался в Манхэттенском проекте . В этом процессе гексафторид урана многократно диффундирует через серебряно - цинковую мембрану, а различные изотопы урана разделяются по скорости диффузии (поскольку уран-238 тяжелее, он диффундирует немного медленнее, чем уран-235). [34] Молекулярный лазерный метод разделения изотопов использует лазерный луч точной энергии для разрыва связи между ураном-235 и фтором. Это оставляет уран-238 связанным с фтором и позволяет металлическому урану-235 осаждаться из раствора. [10] Альтернативный лазерный метод обогащения известен как разделение изотопов с помощью лазера на атомных парах (AVLIS) и использует видимые перестраиваемые лазеры, такие как лазеры на красителях . [125] Другим используемым методом является термодиффузия жидкости. [11]
Единственное значительное отклонение от соотношения 235 U к 238 U в любых известных природных образцах происходит в Окло , Габон , где естественные ядерные реакторы деления потребляли часть 235 U около двух миллиардов лет назад, когда соотношение 235 U к 238 U было больше похоже на соотношение низкообогащенного урана, позволяя обычной («легкой») воде действовать как замедлитель нейтронов, подобно процессу в рукотворных легководных реакторах . Существование таких естественных реакторов деления, которые были теоретически предсказаны заранее, было доказано, поскольку небольшое отклонение концентрации 235 U от ожидаемых значений было обнаружено во время обогащения урана во Франции. Последующие исследования, чтобы исключить любые злонамеренные действия человека (например, кражу 235 U), подтвердили теорию, обнаружив изотопные соотношения обычных продуктов деления (или, скорее, их стабильных дочерних нуклидов) в соответствии со значениями, ожидаемыми для деления, но отклоняющимися от значений, ожидаемых для образцов этих элементов, полученных не путем деления.
Человек может подвергнуться воздействию урана (или его радиоактивных дочерних продуктов , таких как радон ) при вдыхании пыли в воздухе или при употреблении загрязненной воды и пищи. Количество урана в воздухе обычно очень мало; однако люди, которые работают на заводах, перерабатывающих фосфатные удобрения , живут рядом с государственными объектами, которые производили или испытывали ядерное оружие, живут или работают рядом с современным полем боя, где использовалось оружие с обедненным ураном, или живут или работают рядом с угольной электростанцией, объектами, которые добывают или перерабатывают урановую руду или обогащают уран для реакторного топлива, могут подвергаться повышенному воздействию урана. [126] [127] Дома или сооружения, которые находятся над залежами урана (естественными или искусственными шлаковыми отложениями), могут иметь повышенную частоту воздействия радонового газа. Управление по охране труда и технике безопасности (OSHA) установило допустимый предел воздействия урана на рабочем месте в размере 0,25 мг/м 3 в течение 8-часового рабочего дня. Национальный институт охраны труда и здоровья (NIOSH) установил рекомендуемый предел воздействия (REL) в 0,2 мг/м 3 в течение 8-часового рабочего дня и краткосрочный предел в 0,6 мг/м 3 . При 10 мг/м 3 уран становится непосредственно опасным для жизни и здоровья . [128]
Большая часть потребленного урана выводится во время пищеварения . Только 0,5% усваивается при употреблении нерастворимых форм урана, таких как его оксид, тогда как усвоение более растворимого иона уранила может достигать 5%. [30] Однако растворимые соединения урана имеют тенденцию быстро проходить через организм, тогда как нерастворимые соединения урана, особенно при вдыхании в виде пыли в легкие , представляют более серьезную опасность воздействия. После попадания в кровоток поглощенный уран имеет тенденцию биоаккумулироваться и оставаться в костной ткани в течение многих лет из-за сродства урана к фосфатам. [30] Включенный уран становится ионами уранила , которые накапливаются в костях, печени, почках и репродуктивных тканях. [129]
Радиологическая и химическая токсичность урана сочетаются в том, что элементы с высоким атомным номером Z, такие как уран, проявляют фантомную или вторичную радиотоксичность за счет поглощения естественного фонового гамма- и рентгеновского излучения и повторного излучения фотоэлектронов, что в сочетании с высоким сродством урана к фосфатной части ДНК вызывает увеличение одно- и двухцепочечных разрывов ДНК. [130]
Уран не всасывается через кожу, а альфа-частицы , выделяемые ураном, не могут проникнуть через кожу. [27]
Уран можно дезактивировать со стальных поверхностей [131] и водоносных горизонтов . [132] [133]
Нормальное функционирование почек , мозга , печени , сердца и других систем может быть нарушено воздействием урана, поскольку уран не только слабо радиоактивен, но и является токсичным металлом . [30] [134] [135] Уран также является репродуктивным токсичным веществом . [136] [137] Радиологические эффекты, как правило, локальны, поскольку альфа-излучение, первичная форма распада 238 U, имеет очень короткий радиус действия и не проникает через кожу. Было показано, что альфа-излучение от вдыхаемого урана вызывает рак легких у подвергшихся воздействию работников ядерной промышленности. [138] Хотя CDC опубликовал одно исследование, в котором говорится, что в результате воздействия природного или обедненного урана не было зафиксировано ни одного случая рака у человека , [139] воздействие урана и продуктов его распада, особенно радона , представляет значительную угрозу для здоровья. [140] Воздействие стронция-90 , йода-131 и других продуктов деления не связано с воздействием урана, но может быть результатом медицинских процедур или воздействия отработанного реакторного топлива или радиоактивных осадков от ядерного оружия. [141]
Хотя случайное вдыхание высокой концентрации гексафторида урана приводило к человеческим жертвам, эти смерти были связаны с образованием высокотоксичной плавиковой кислоты и фторида уранила , а не с самим ураном. [142] Мелко измельченный металлический уран представляет опасность возгорания, поскольку уран является пирофорным веществом ; мелкие зерна будут самопроизвольно воспламеняться на воздухе при комнатной температуре. [12]
С металлическим ураном обычно работают в перчатках в качестве достаточной меры предосторожности. [143] Концентрат урана обрабатывается и хранится таким образом, чтобы гарантировать, что люди не вдыхают или не глотают его. [143]