
В химии и производстве электролиз — это метод, который использует постоянный электрический ток (DC) для управления иначе несамопроизвольной химической реакцией . Электролиз имеет коммерчески важное значение как этап разделения элементов из природных источников, таких как руды, с использованием электролитической ячейки . Напряжение , необходимое для осуществления электролиза, называется потенциалом разложения. Слово «лизис» означает разделять или разрывать, поэтому в терминах электролиз будет означать «разрушение посредством электричества».
Слово «электролиз» было введено Майклом Фарадеем в 1834 году [1], используя греческие слова ἤλεκτρον [ɛ̌ːlektron] «янтарь», который с XVII века ассоциировался с электрическими явлениями , и λύσις [lýsis] — «растворение». Тем не менее, электролиз как инструмент для изучения химических реакций и получения чистых элементов предшествует созданию термина и формальному описанию Фарадеем.
В начале девятнадцатого века Уильям Николсон и Энтони Карлайл пытались продолжить эксперименты Вольта . Они прикрепили два провода к каждой стороне вольтова столба и поместили другие концы в трубку, наполненную водой. Они заметили, что когда провода были соединены вместе, каждый провод производил пузырьки. Один тип был водородом, другой — кислородом. [2]
В 1785 году голландский ученый Мартин ван Марум создал электростатический генератор, который он использовал для восстановления олова, цинка и сурьмы из их солей, используя процесс, позже известный как электролиз. Хотя он неосознанно произвел электролиз, только в 1800 году Уильям Николсон и Энтони Карлайл открыли, как работает электролиз. [3]
В 1791 году Луиджи Гальвани экспериментировал с лягушачьими лапками. Он утверждал, что помещение мышц животных между двумя разнородными металлическими листами приводит к появлению электричества. В ответ на эти заявления Алессандро Вольта провел собственные испытания. [4] [5] Это дало бы представление об идеях Гемфри Дэви об электролизе. Во время предварительных экспериментов Гемфри Дэви выдвинул гипотезу, что когда два элемента объединяются, образуя соединение, выделяется электрическая энергия. Гемфри Дэви продолжил создавать Таблицы разложения на основе своих предварительных экспериментов по электролизу. Таблицы разложения дали бы представление об энергиях, необходимых для расщепления определенных соединений. [6]
В 1817 году Йохан Август Арфведсон определил, что в некоторых образцах есть еще один элемент — литий; однако он не смог выделить этот компонент. Только в 1821 году Уильям Томас Бранде использовал электролиз, чтобы выделить его. Два года спустя он оптимизировал процесс, используя хлорид лития и хлорид калия с электролизом для получения лития и гидроксида лития. [7] [8]
В последние годы исследований Гемфри Дэви, Майкл Фарадей стал его помощником. Изучая процесс электролиза под руководством Гемфри Дэви, Майкл Фарадей открыл два закона электролиза . [5]
Во времена Максвелла и Фарадея появились [ смутные ] опасения относительно электроположительной и электроотрицательной активности. [9]
В ноябре 1875 года Поль Эмиль Лекок де Буабодран открыл галлий, используя электролиз гидроксида галлия, получив 3,4 мг галлия. В декабре следующего года он представил свое открытие галлия в Парижской академии наук . [10]
26 июня 1886 года Фердинанд Фредерик Анри Муассан наконец почувствовал себя комфортно, выполняя электролиз безводного фтористого водорода, чтобы создать газообразный чистый элемент фтора. До того, как он использовал фтористый водород, Анри Муассан использовал фтористые соли с электролизом. Таким образом, 28 июня 1886 года он провел свой эксперимент перед Академией наук, чтобы продемонстрировать свое открытие нового элемента фтора. [11] При попытке найти элементарный фтор посредством электролиза фтористых солей погибло много химиков, включая Полина Луйе и Жерома Никле. [12]
В 1886 году Чарльз Мартин Холл из Америки и Поль Эру из Франции подали заявки на американские патенты на электролиз алюминия, причем Эру подал свою заявку в мае, а Холл — в июле. [13] Холл смог получить свой патент, доказав с помощью писем своему брату и семье, что его метод был открыт до подачи французского патента. [14] Это стало известно как процесс Холла–Эру , который принес пользу многим отраслям промышленности, поскольку цена алюминия тогда упала с четырех долларов до тридцати центов за фунт. [15]
В 1902 году польский инженер и изобретатель Станислав Лащинский подал заявку и получил польский патент на электролиз меди и цинка . [16] [17] [18]
Электролиз — это пропускание постоянного электрического тока через электролит , в результате чего на электродах происходят химические реакции и разложение материалов.
Основными компонентами, необходимыми для достижения электролиза, являются электролит , электроды и внешний источник питания. Перегородка (например, ионообменная мембрана или солевой мостик ) является необязательной для предотвращения диффузии продуктов в окрестности противоположного электрода.
Электролит — это химическое вещество , которое содержит свободные ионы и переносит электрический ток (например, полимер с ионным проводником , раствор или ионное жидкое соединение). Если ионы неподвижны, как в большинстве твердых солей , то электролиз невозможен. Жидкий электролит получается путем:
Электроды погружены на расстоянии друг от друга, так что ток течет между ними через электролит , и подключены к источнику питания, который замыкает электрическую цепь . Постоянный ток, подаваемый источником питания, запускает реакцию, заставляя ионы в электролите притягиваться к соответствующему противоположно заряженному электроду.
Широко используются электроды из металла , графита и полупроводникового материала. Выбор подходящего электрода зависит от химической реактивности между электродом и электролитом и стоимости производства. Исторически, когда для электролиза требовались нереактивные аноды, выбирались графит (называемый плюмбаго во времена Фарадея) или платина. [21] Было обнаружено, что они являются одними из наименее реактивных материалов для анодов. Платина разрушается очень медленно по сравнению с другими материалами, а графит крошится и может выделять углекислый газ в водных растворах, но в остальном не участвует в реакции. Катоды могут быть изготовлены из того же материала, или они могут быть изготовлены из более реактивного, поскольку износ анода больше из-за окисления на аноде.
Ключевым процессом электролиза является взаимообмен атомами и ионами путем удаления или добавления электронов из-за приложенного потенциала. Желаемые продукты электролиза часто находятся в другом физическом состоянии, чем электролит, и могут быть удалены механическими процессами (например, путем сбора газа над электродом или осаждения продукта из электролита).
Количество продуктов пропорционально току, и когда две или более электролитических ячеек соединены последовательно с одним и тем же источником питания, продукты, произведенные в ячейках, пропорциональны их эквивалентному весу . Они известны как законы электролиза Фарадея .
Каждый электрод притягивает ионы с противоположным зарядом . Положительно заряженные ионы ( катионы ) движутся к катоду, дающему электроны (отрицательному). Отрицательно заряженные ионы ( анионы ) движутся к аноду, извлекающему электроны (положительному). В этом процессе электроны эффективно вводятся на катоде в качестве реагента и удаляются на аноде в качестве продукта . В химии потеря электронов называется окислением , тогда как присоединение электронов называется восстановлением .
Когда нейтральные атомы или молекулы, например, находящиеся на поверхности электрода, приобретают или теряют электроны, они становятся ионами и могут растворяться в электролите и реагировать с другими ионами.
Когда ионы получают или теряют электроны и становятся нейтральными, они образуют соединения, которые отделяются от электролита. Положительные ионы металлов, такие как Cu2 +, осаждаются на катоде в виде слоя. Термины для этого — гальванопокрытие , электровыделение и электрорафинирование .
Когда ион приобретает или теряет электроны, не становясь нейтральным, его электронный заряд при этом изменяется.
Например, электролиз рассола производит водород и хлорные газы, которые пузырятся из электролита и собираются. Начальная общая реакция выглядит следующим образом: [22]
Реакция на аноде приводит к образованию газообразного хлора из ионов хлора:
В результате реакции на катоде образуются газообразный водород и гидроксид-ионы:
Без перегородки между электродами ионы OH − , образующиеся на катоде, могут свободно диффундировать через электролит к аноду. По мере того, как электролит становится более основным из-за образования OH − , из раствора выделяется меньше Cl 2 , поскольку он начинает реагировать с гидроксидом, образуя гипохлорит (ClO − ) на аноде:
Чем больше возможностей у Cl 2 для взаимодействия с NaOH в растворе, тем меньше Cl 2 выходит на поверхность раствора и тем быстрее происходит образование гипохлорита. Это зависит от таких факторов, как температура раствора, время контакта молекулы Cl 2 с раствором и концентрация NaOH.
Аналогично, по мере увеличения концентрации гипохлорита из него образуются хлораты:
Происходят и другие реакции, такие как самоионизация воды и разложение гипохлорита на катоде, скорость последнего зависит от таких факторов, как диффузия и площадь поверхности катода, контактирующая с электролитом. [23]
Потенциал разложения или напряжение разложения относится к минимальному напряжению (разнице электродного потенциала ) между анодом и катодом электролитической ячейки, которое необходимо для осуществления электролиза. [24]
Напряжение, при котором электролиз термодинамически предпочтителен, представляет собой разницу электродных потенциалов, рассчитанную с помощью уравнения Нернста . Приложение дополнительного напряжения, называемого перенапряжением , может увеличить скорость реакции и часто требуется выше термодинамического значения. Это особенно необходимо для реакций электролиза с участием газов, таких как кислород , водород или хлор .
На аноде происходит окисление ионов или нейтральных молекул . Например, на аноде возможно окисление ионов железа в ионы железа:
На катоде происходит восстановление ионов или нейтральных молекул. На катоде возможно восстановление ионов феррицианида до ионов ферроцианида :
Нейтральные молекулы также могут реагировать на любом из электродов. Например: п -бензохинон может быть восстановлен до гидрохинона на катоде:
В последнем примере в реакции также принимают участие ионы H + (ионы водорода), источником которых является кислота в растворе или сам растворитель (вода, метанол и т. д.). Реакции электролиза с участием ионов H + довольно распространены в кислых растворах. В водно-щелочных растворах распространены реакции с участием OH− (ионов гидроксида) .
Иногда сами растворители (обычно вода) окисляются или восстанавливаются на электродах. Возможен даже электролиз с участием газов, например, с использованием газодиффузионного электрода .
Количество электроэнергии, которое должно быть добавлено, равно изменению свободной энергии Гиббса реакции плюс потери в системе. Потери могут (теоретически) быть сколь угодно близкими к нулю, поэтому максимальная термодинамическая эффективность равна изменению энтальпии, деленному на изменение свободной энергии реакции. В большинстве случаев электрическая мощность больше, чем изменение энтальпии реакции, поэтому часть энергии выделяется в виде тепла. В некоторых случаях, например, при электролизе пара в водород и кислород при высокой температуре, верно обратное, и тепловая энергия поглощается. Это тепло поглощается из окружающей среды, и теплотворная способность полученного водорода выше электрической мощности.
Пульсирующий ток приводит к продуктам, отличным от постоянного тока. Например, пульсация увеличивает соотношение озона к кислороду, производимому на аноде при электролизе водного кислотного раствора, такого как разбавленная серная кислота. [25] Электролиз этанола с помощью импульсного тока выделяет альдегид вместо первичной кислоты. [26]
Гальванические элементы и батареи используют спонтанные, высвобождающие энергию окислительно-восстановительные реакции для генерации электрического потенциала, который обеспечивает полезную мощность. Когда вторичная батарея заряжается, ее окислительно-восстановительная реакция протекает в обратном направлении, и систему можно рассматривать как электролитическую ячейку .
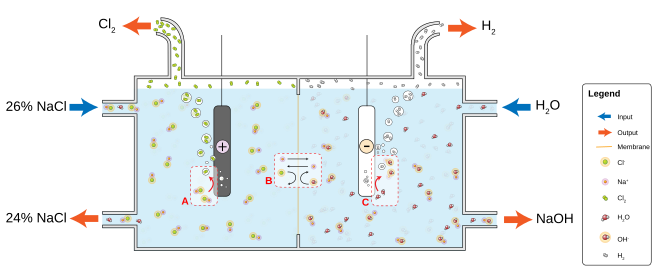
Процесс хлорщелочного производства представляет собой крупномасштабное применение электролиза. Эта технология обеспечивает большую часть хлора и гидроксида натрия, необходимых многим отраслям промышленности. Катод представляет собой титановый анод, покрытый смешанным оксидом металла (также называемый размерно-стабильным анодом). [27] [28]
Многие фторорганические соединения производятся электрофторированием . [29] Одним из проявлений этой технологии является процесс Саймонса , который можно описать следующим образом:
В ходе типичного синтеза эта реакция происходит один раз для каждой связи C–H в прекурсоре. Потенциал ячейки поддерживается около 5–6 В. Анод , электрокатализатор , никелирован .
Акрилонитрил преобразуется в адипонитрил в промышленных масштабах посредством электрокатализа. [30]

Гальванопокрытие , где тонкая пленка металла наносится на материал подложки. Гальванопокрытие используется во многих отраслях промышленности как в функциональных, так и в декоративных целях, например, для кузовов автомобилей и никелевых монет.
В электрохимической обработке электролитический катод используется как фасонный инструмент для удаления материала с заготовки путем анодного окисления. ECM часто используется как метод удаления заусенцев или травления металлических поверхностей, таких как инструменты или ножи, с постоянной маркировкой или логотипом.
При использовании ячейки, содержащей инертные платиновые электроды, электролиз водных растворов некоторых солей приводит к восстановлению катионов (например, осаждению металлов с помощью солей цинка) и окислению анионов (например, выделению брома с помощью бромидов). Однако с солями некоторых металлов (например, натрия) на катоде выделяется водород, а для солей, содержащих некоторые анионы (например, сульфата SO2−
4) кислород выделяется на аноде. В обоих случаях это происходит из-за того, что вода восстанавливается до водорода или окисляется до кислорода. В принципе, напряжение, необходимое для электролиза солевого раствора, можно вывести из стандартного электродного потенциала для реакций на аноде и катоде. Стандартный электродный потенциал напрямую связан со свободной энергией Гиббса , Δ G , для реакций на каждом электроде и относится к электроду, по которому не течет ток. Ниже приведена выдержка из таблицы стандартных электродных потенциалов .
С точки зрения электролиза эту таблицу следует интерпретировать следующим образом:
Используя уравнение Нернста, можно рассчитать электродный потенциал для определенной концентрации ионов, температуры и числа вовлеченных электронов. Для чистой воды ( pH 7):
Сопоставимые цифры, рассчитанные аналогичным образом для 1 M бромида цинка , ZnBr2 , составляют −0,76 В для восстановления до металлического Zn и +1,10 В для окисления с образованием брома. Вывод из этих цифр заключается в том, что на катоде должен образовываться водород, а на аноде — кислород при электролизе воды, что противоречит экспериментальному наблюдению, что металлический цинк осаждается, а бром образуется. [33] Объяснение заключается в том, что эти рассчитанные потенциалы указывают только на термодинамически предпочтительную реакцию. На практике необходимо учитывать множество других факторов, таких как кинетика некоторых задействованных стадий реакции. Эти факторы вместе означают, что для восстановления и окисления воды требуется более высокий потенциал, чем прогнозировалось, и они называются перенапряжениями . Экспериментально известно, что перенапряжения зависят от конструкции ячейки и природы электродов.
При электролизе нейтрального (pH 7) раствора хлорида натрия восстановление ионов натрия термодинамически очень затруднено, и вода восстанавливается, выделяя водород, оставляя гидроксид-ионы в растворе. На аноде наблюдается окисление хлора, а не окисление воды, поскольку перенапряжение для окисления хлорида до хлора ниже , чем перенапряжение для окисления воды до кислорода . Гидроксид-ионы и растворенный газообразный хлор далее реагируют, образуя хлорноватистую кислоту . Водные растворы, полученные в результате этого процесса, называются электролизованной водой и используются в качестве дезинфицирующего и чистящего средства.
Электрохимическое восстановление или электрокаталитическое преобразование CO 2 может производить химические вещества с добавленной стоимостью, такие как метан , этилен , этанол и т. д. [34] [35] [36] Электролиз диоксида углерода дает формиат или оксид углерода, но иногда и более сложные органические соединения, такие как этилен . [37] Эта технология исследуется как углеродно-нейтральный путь к органическим соединениям. [38] [39]
Электролиз воды производит водород и кислород в соотношении 2 к 1 соответственно.
Энергоэффективность электролиза воды сильно различается. Эффективность электролизера является мерой энтальпии, содержащейся в водороде (для сжигания с кислородом или какой-либо другой последующей реакции), по сравнению с входной электрической энергией. Значения теплоты/энтальпии для водорода хорошо опубликованы в научных и инженерных текстах, как 144 МДж/кг (40 кВт·ч/кг). Обратите внимание, что топливные элементы (не электролизеры) не могут использовать это полное количество тепла/энтальпии, что привело к некоторой путанице при расчете значений эффективности для обоих типов технологий. В реакции часть энергии теряется в виде тепла. В некоторых отчетах указывается эффективность от 50% до 70% для щелочных электролизеров (50 кВт·ч/кг); [40] однако, более высокая практическая эффективность доступна при использовании электролиза с полимерным электролитом и каталитической технологии, например, эффективность 95%. [41] [42]
В 2006 году Национальная лаборатория возобновляемой энергии подсчитала, что 1 кг водорода (что примерно эквивалентно 3 кг или 4 литрам нефти в энергетическом выражении) может быть произведен с помощью ветроэлектролиза по цене от 5,55 долл. США в краткосрочной перспективе до 2,27 долл. США в долгосрочной перспективе. [43]
Около 4% производимого в мире водорода генерируется электролизом и обычно используется на месте. Водород используется для создания аммиака для удобрений с помощью процесса Хабера и преобразования тяжелых нефтяных источников в более легкие фракции с помощью гидрокрекинга . Электролиз на месте использовался для улавливания водорода для водородных топливных элементов в водородных транспортных средствах .
В последнее время для снижения энергозатрат в качестве жизнеспособного варианта было предложено использование углерода ( угля ), спиртов (углеводородного раствора) и органического раствора ( глицерина , муравьиной кислоты, этиленгликоля и т. д.) с совместным электролизом воды. [44] [45] Процесс электролиза воды с участием углерода/углеводорода (так называемый CAWE) для получения водорода будет выполнять эту операцию в одном электрохимическом реакторе. Этот энергетический баланс системы может потребовать только около 40% электрического входа, а 60% поступает из химической энергии углерода или углеводорода. [46] Этот процесс использует твердые частицы угля/углерода или порошок в качестве топлива, диспергированного в кислотном/щелочном электролите в форме суспензии, а содержащийся в нем источник совместно участвует в процессе электролиза в соответствии со следующими теоретическими общими реакциями: [47]
или
Таким образом, данный подход CAWE заключается в том, что фактическое перенапряжение ячейки может быть значительно снижено до уровня ниже 1,0 В по сравнению с 1,5 В при обычном электролизе воды.
Специализированное применение электролиза включает в себя рост проводящих кристаллов на одном из электродов из окисленных или восстановленных видов, которые генерируются in situ. Методика использовалась для получения монокристаллов низкоразмерных электрических проводников, таких как соли переноса заряда и линейные цепочечные соединения . [48] [49]
Текущий метод производства стали из железной руды является очень углеродоемким, отчасти из-за прямого выброса CO2 в доменной печи. Исследование сталелитейного производства в Германии показало, что при производстве 1 тонны стали выбрасывается 2,1 тонны CO2e, причем 22 % из них составляют прямые выбросы из доменной печи. [50] По состоянию на 2022 год производство стали обеспечивает 7–9% мировых выбросов. [51] Электролиз железа может устранить прямые выбросы и еще больше сократить выбросы, если электроэнергия будет производиться из зеленой энергии.
Маломасштабный электролиз железа был успешно описан путем растворения его в расплавленных оксидных солях и использования платинового анода. [52] Анионы кислорода образуют газообразный кислород и электроны на аноде. Катионы железа потребляют электроны и образуют металлическое железо на катоде. Этот метод был выполнен при температуре 1550 °C, что представляет собой значительную проблему для поддержания реакции. В частности, коррозия анода является проблемой при этих температурах.
Кроме того, сообщалось о низкотемпературном восстановлении оксида железа путем растворения его в щелочной воде. [53] Температура намного ниже, чем при традиционном производстве железа при 114 °C. Низкие температуры также, как правило, коррелируют с более высокой эффективностью тока, при этом сообщается об эффективности в 95%. Хотя эти методы являются многообещающими, они с трудом могут быть конкурентоспособными по стоимости из-за большой экономии масштаба, удерживающей цену доменного железа на низком уровне.
Исследование 2020 года изучало прямой электролиз морской воды, щелочной электролиз, электролиз с протонообменной мембраной и электролиз твердых оксидов . [54] Прямой электролиз морской воды следует известным процессам, образуя электролизную ячейку, в которой морская вода действует как электролит, обеспечивая реакцию на аноде , 2 Cl − (aq) → Cl 2 (g) + 2e − и реакцию на катоде , 2 H 2 O(l) + 2 e − → H 2 (g) + 2OH − (aq) . Включение ионов магния и кальция в морскую воду делает возможным образование щелочных гидроксидов , которые могут образовывать накипь в ячейке электролизера, сокращая срок службы и увеличивая потребность в техническом обслуживании. Щелочные электролизеры работают со следующими реакциями на аноде, 2 OH − (водн.) → 1/ 2 O 2 (г) + H 2 O(ж) + 2 e − и катоде, 2 H 2 O(ж) + 2 e − → H 2 (г) + 2 OH − (водн.) , и используют высокоосновные растворы в качестве электролитов, работая при 60–90 °C (140–194 °F) и нуждаясь в дополнительных сепараторах, чтобы гарантировать, что газообразная фаза водорода и кислорода остается раздельной. Электролит может легко загрязняться, но щелочной электролизер может работать под давлением, что улучшает потребление энергии. Электроды могут быть изготовлены из недорогих материалов, и в конструкции нет необходимости в дорогостоящем катализаторе. Электролизеры с протонообменной мембраной работают с реакциями на аноде, H 2 O(ж) → 1/ 2 O 2 (г) + 2 H + (водн.) + 2 e − и катоде, 2 H + (водн.) + 2 e − → H 2 (г) , при температурах 60–80 °C (140–176 °F), с использованием твердого полимерного электролита и требуя более высоких затрат на обработку, чтобы твердый электролит равномерно соприкасался с электродами. Подобно щелочному электролизёру, электролизер с протонообменной мембраной может работать при более высоких давлениях, что снижает затраты энергии, необходимые для последующего сжатия газообразного водорода, но электролизер с протонообменной мембраной также выигрывает от быстрого времени отклика на изменения требований или потребностей в мощности и не нуждается в обслуживании, за счет более высокой скорости естественной деградации и наибольшей уязвимости к примесям в воде. Твердооксидные электролизёры запускают реакции O−2(г) → 1/ 2 O 2 (г) + 2 e − на аноде и H 2 O(г) + 2 e − → H 2 (г) + O−2(g) на катоде. Твердооксидные электролизеры требуют высоких температур (700–1000 °C (1292–1832 °F)) для работы, генерируя перегретый пар. Они страдают от деградации при выключении, что делает их более негибкой технологией производства водорода. В выбранной серии сравнений многокритериального анализа решений , в которых наивысший приоритет был отдан экономическим эксплуатационным расходам, за которыми в равной степени следовали экологические и социальные критерии, было обнаружено, что электролизер с протонообменной мембраной предлагает наиболее подходящее сочетание значений (например, инвестиционные затраты, расходы на техническое обслуживание и эксплуатацию, устойчивость к примесям, удельная энергия для производства водорода в море, риск воздействия на окружающую среду и т. д.), за которым следует щелочной электролизер, причем щелочной электролизер является наиболее экономически целесообразным, но более опасным с точки зрения безопасности и экологических проблем из-за необходимости использования основных электролитных растворов в отличие от твердых полимеров, используемых в протонообменных мембранах. В связи с методами, применяемыми при многокритериальном анализе решений, к различным факторам применяются необъективные веса, поэтому одновременно применялись несколько методов анализа решений для проверки электролизеров таким образом, чтобы свести к минимуму влияние предвзятости на выводы о производительности.