
В органической химии пептидная связь представляет собой амидный тип ковалентной химической связи, соединяющей две последовательные альфа-аминокислоты от C1 ( углерод номер один) одной альфа-аминокислоты и N2 ( азот номер два) другой, вдоль пептидной или белковой цепи. [1]
Ее также можно назвать эупептидной связью [1], чтобы отличить ее от изопептидной связи , которая представляет собой другой тип амидной связи между двумя аминокислотами.

Когда две аминокислоты образуют дипептид через пептидную связь , [1] это тип реакции конденсации . [2] При таком типе конденсации две аминокислоты сближаются, при этом не- боковая цепь (C1) карбоновой кислоты одной приближается к не-боковой цепи (N2) аминогруппы другой. Одна теряет водород и кислород из своей карбоксильной группы (COOH), а другая теряет водород из своей аминогруппы (NH 2 ) . Эта реакция производит молекулу воды (H 2 O) и две аминокислоты, соединенные пептидной связью (−CO−NH−). Две соединенные аминокислоты называются дипептидом.
Амидная связь синтезируется, когда карбоксильная группа одной молекулы аминокислоты реагирует с аминогруппой другой молекулы аминокислоты, вызывая высвобождение молекулы воды (H2O ) , поэтому процесс представляет собой реакцию дегидратационного синтеза .
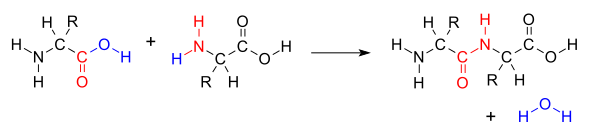
Образование пептидной связи потребляет энергию, которая в организмах вырабатывается из АТФ . [3] Пептиды и белки представляют собой цепи аминокислот, удерживаемые вместе пептидными связями (а иногда и несколькими изопептидными связями ). Организмы используют ферменты для производства нерибосомальных пептидов , [4] и рибосомы для производства белков посредством реакций, которые в деталях отличаются от синтеза дегидратации. [5]
Некоторые пептиды, такие как альфа-аманитин , называются рибосомальными пептидами, поскольку они производятся рибосомами, [6] но многие являются нерибосомальными пептидами , поскольку они синтезируются специализированными ферментами, а не рибосомами. Например, трипептид глутатион синтезируется в два этапа из свободных аминокислот двумя ферментами : глутамат-цистеинлигазой (образует изопептидную связь , которая не является пептидной связью) и глутатионсинтетазой (образует пептидную связь). [7] [8]
Пептидная связь может быть разорвана гидролизом (добавлением воды). Гидролиз пептидных связей в воде высвобождает 8–16 кДж / моль (2–4 ккал / моль ) энергии Гиббса . [9] Этот процесс чрезвычайно медленный, с периодом полураспада при 25 °C от 350 до 600 лет на связь. [10]
В живых организмах этот процесс обычно катализируется ферментами , известными как пептидазы или протеазы , хотя имеются сообщения о гидролизе пептидной связи, вызванном конформационным напряжением, когда пептид/белок сворачивается в нативную структуру. [11] Таким образом, этот неферментативный процесс ускоряется не стабилизацией переходного состояния, а скорее дестабилизацией основного состояния.
Длина волны поглощения пептидной связи составляет 190–230 нм [12] , что делает ее особенно восприимчивой к УФ- излучению.
Значительная делокализация неподеленной пары электронов на атоме азота придает группе характер частичной двойной связи . Частичная двойная связь делает амидную группу плоской , встречающейся либо в цис- , либо в транс-изомерах . В развернутом состоянии белков пептидные группы могут свободно изомеризоваться и принимать оба изомера; однако в свернутом состоянии в каждой позиции принимается только один изомер (за редкими исключениями). Транс-форма в подавляющем большинстве пептидных связей предпочтительнее (примерно 1000:1 соотношение в транс:цис-популяциях). Однако пептидные группы X-Pro имеют тенденцию иметь соотношение примерно 30:1, предположительно потому, что симметрия между атомами C α и C δ пролина делает цис- и транс-изомеры почти равными по энергии, как показано на рисунке ниже.
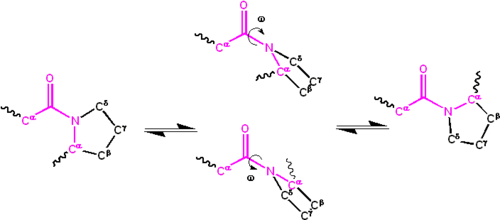
Двугранный угол, связанный с пептидной группой (определяется четырьмя атомами C α –C'–N–C α ), обозначается ; для цис-изомера ( синперипланарная конформация) и для транс-изомера ( антиперипланарная конформация). Амидные группы могут изомеризоваться вокруг связи C'–N между цис- и транс-формами, хотя и медленно ( секунды при комнатной температуре). Переходные состояния требуют, чтобы частичная двойная связь была разорвана, так что энергия активации составляет примерно 80 кДж/моль (20 ккал/моль). Однако энергию активации можно снизить (и катализировать изомеризацию ) путем изменений, которые благоприятствуют форме с одинарной связью, например, путем помещения пептидной группы в гидрофобную среду или передачи водородной связи атому азота пептидной группы X-Pro. Оба эти механизма снижения энергии активации наблюдались в пептидилпролилизомеразах (ППИазах), которые представляют собой природные ферменты, катализирующие цис-транс-изомеризацию пептидных связей X-Pro.
Конформационное сворачивание белка обычно происходит намного быстрее (обычно 10–100 мс), чем цис-транс-изомеризация (10–100 с). Ненативный изомер некоторых пептидных групп может значительно нарушить конформационное сворачивание, либо замедлив его, либо даже предотвратив его возникновение до тех пор, пока не будет достигнут нативный изомер. Однако не все пептидные группы оказывают одинаковое влияние на сворачивание; ненативные изомеры других пептидных групп могут вообще не влиять на сворачивание.
Благодаря своей резонансной стабилизации пептидная связь относительно нереактивна в физиологических условиях, даже меньше, чем аналогичные соединения, такие как эфиры . Тем не менее, пептидные связи могут подвергаться химическим реакциям, обычно посредством атаки электроотрицательного атома на карбонильный углерод , разрывая карбонильную двойную связь и образуя тетраэдрический промежуточный продукт. Это путь, по которому следуют в протеолизе и, в более общем смысле, в реакциях обмена ацила N–O, таких как реакции интеинов . Когда функциональная группа, атакующая пептидную связь, является тиолом , гидроксилом или амином , полученная молекула может быть названа циклолом или, более конкретно, тиациклолом, оксациклолом или азациклолом соответственно.
{{cite book}}: |journal=проигнорировано ( помощь )