Радиационное воздействие является мерой ионизации воздуха из-за ионизирующего излучения от фотонов . [1] Оно определяется как электрический заряд, высвобождаемый таким излучением в определенном объеме воздуха, деленный на массу этого воздуха. [1] По состоянию на 2007 год «медицинское облучение» было определено Международной комиссией по радиологической защите как облучение, которому подвергаются люди в рамках их собственной медицинской или стоматологической диагностики или лечения; лица, не являющиеся профессионально подверженными облучению, сознательно, добровольно помогая в поддержке и комфорте пациентов; и добровольцы в программе биомедицинских исследований, включающих их облучение. [2] Обычные медицинские тесты и методы лечения, включающие в себя облучение, включают рентген , КТ , маммографию , вентиляцию легких и перфузионное сканирование , сканирование костей , перфузионное сканирование сердца , ангиографию , лучевую терапию и многое другое. [3] Каждый тип теста несет свою собственную дозу облучения. [2] Существует две общие категории неблагоприятных последствий для здоровья, вызванных воздействием радиации: детерминированные эффекты и стохастические эффекты. [2] Детерминированные эффекты (вредные реакции тканей) обусловлены гибелью/нарушением функционирования клеток после высоких доз; а стохастические эффекты включают либо развитие рака у облученных людей, вызванное мутацией соматических клеток , либо наследственные заболевания у их потомков из-за мутации репродуктивных (зародышевых) клеток . [2]
Поглощенная доза — это термин, используемый для описания того, сколько энергии излучение откладывает в материале. [4] Обычные единицы измерения поглощенной дозы включают рад, или поглощенную дозу излучения , и Грей, или Гр. Эквивалент дозы рассчитывает воздействие радиации на ткани человека. [4] Это делается с использованием весового коэффициента ткани, который учитывает, насколько каждая ткань в организме имеет различную чувствительность к радиации. [4] Эффективная доза — это риск радиации, усредненный по всему телу. [4] Известно, что ионизирующее излучение вызывает рак у людей. [4] Мы знаем это из исследования продолжительности жизни, в котором наблюдались выжившие после атомной бомбардировки Японии во время Второй мировой войны. [5] [4] Более 100 000 человек наблюдались в течение 50 лет. [5] 1 из 10 случаев рака, образовавшихся за это время, был вызван радиацией. [6] Исследование показывает линейную зависимость дозы от реакции для всех солидных опухолей. [6] Это означает, что связь между дозой и реакцией человеческого организма представляет собой прямую линию. [6]
Риск низкой дозы радиации при медицинской визуализации не доказан. [7] Трудно установить риск из-за низкой дозы радиации. [7] Это отчасти связано с тем, что в окружающей среде присутствуют другие канцерогены, включая курение, химикаты и загрязняющие вещества. [7] Обычная КТ головы имеет эффективную дозу 2 мЗв. [7] Это сопоставимо с количеством фоновой радиации, которому человек подвергается за 1 год. [5] Фоновая радиация исходит от естественных радиоактивных материалов и космической радиации из космоса. [5] Эмбрион и плод считаются высокочувствительными к воздействию радиации. [8] Осложнения от воздействия радиации включают пороки развития внутренних органов, снижение IQ и образование рака. [8] Единица измерения воздействия в системе СИ — кулон на килограмм (Кл/кг), который в значительной степени заменил рентген (Р). [9] Один рентген равен0,000 258 Кл/кг ; воздействие одного кулона на килограмм эквивалентно 3876 рентгенам. [9]
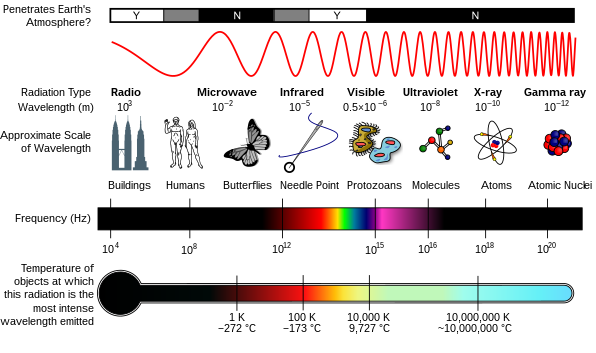
Радиация — это движущаяся форма энергии, классифицируемая на ионизирующий и неионизирующий тип. [4] Ионизирующее излучение далее подразделяется на электромагнитное излучение (без вещества) и корпускулярное излучение (с веществом). [4] Электромагнитное излучение состоит из фотонов, которые можно рассматривать как энергетические пакеты, перемещающиеся в форме волны. [4] Примерами электромагнитного излучения являются рентгеновские лучи и гамма-лучи (см. фото «Типы электромагнитного излучения»). [4] Эти типы излучения могут легко проникать в тело человека из-за высокой энергии. [4]
По состоянию на 2007 год «медицинское облучение» было определено Международной комиссией по радиологической защите как облучение, которому подвергаются люди в ходе собственной медицинской или стоматологической диагностики или лечения; лица, не подвергающиеся профессиональному облучению, сознательно, добровольно помогая в поддержке и комфорте пациентов; и добровольцы в программе биомедицинских исследований, включающей их облучение. [2] По состоянию на 2012 год риск низкой дозы радиации в медицинской визуализации не был доказан. [7] Трудно установить риски, связанные с низкой дозой радиации. [7] Одна из причин этого заключается в том, что между воздействием радиации и появлением рака проходит длительный период времени. [7] Кроме того, существует естественная заболеваемость раком. [7] Трудно определить, вызвано ли увеличение заболеваемости раком среди населения низкой дозой радиации. [7] Наконец, мы живем в среде, где другие мощные канцерогены могут повлиять на результаты этих исследований. [7] Сюда входят химические вещества, загрязняющие вещества, сигаретный дым и многое другое. [7]
См. таблицу эффективных доз от обычных медицинских диагностических визуализационных исследований. [7]
Поглощенная доза — это количество энергии, которое ионизирующее излучение отдает материалу. [4] Поглощенная доза будет зависеть от типа вещества, которое поглощает излучение. [4] При облучении 1 рентген гамма-лучами с энергией 1 МэВ доза в воздухе составит 0,877 рад , доза в воде составит 0,975 рад, доза в кремнии составит 0,877 рад, а доза в усредненной человеческой ткани составит 1 рад. [10] «рад» означает поглощенную дозу излучения . [4] Это специальная дозиметрическая величина, используемая для оценки дозы от радиационного воздействия. [4] Еще одним распространенным измерением для человеческой ткани является Грей (Гр, международная или СИ единица). [4] В ссылке на это предложение есть таблица, в которой дается преобразование экспозиции в дозу для этих четырех материалов. [10] Количество энергии, отложенной в человеческой ткани и органах, является основой для измерений для людей. [4] Затем эти дозы рассчитываются как радиационный риск с учетом типа радиации, а также различной чувствительности органов и тканей. [4]
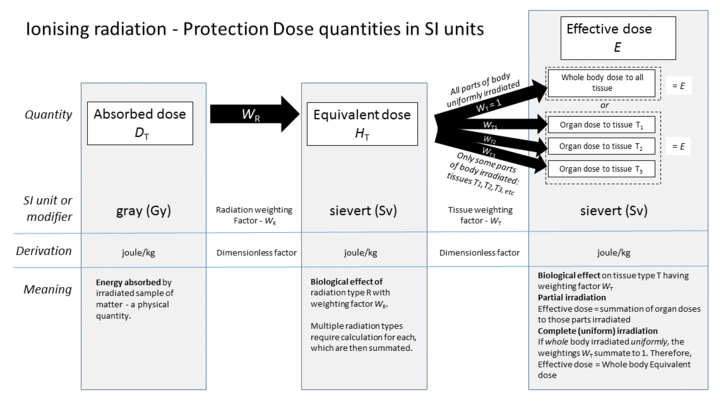
Для измерения биологического воздействия радиации на ткани человека используется эффективная доза или эквивалент дозы. [4] Эквивалент дозы измеряет эффективную дозу радиации в определенном органе или ткани. [4] Эквивалент дозы рассчитывается по следующей формуле: [4]
Эквивалент дозы = Поглощенная доза x Весовой коэффициент ткани
Коэффициент взвешивания ткани отражает относительную чувствительность каждого органа к радиации. [4]
Эффективная доза относится к радиационному риску, усредненному по всему телу. [4] Это сумма эквивалентной дозы всех облученных органов или тканей. [4] Эквивалентная доза и эффективная доза измеряются в зивертах (Зв). [4]
Например, предположим, что тонкий кишечник и желудок человека подвергаются облучению по отдельности. [2] Поглощенная доза тонкого кишечника составляет 100 мЗв, а поглощенная доза желудка составляет 70 мЗв. Весовые коэффициенты тканей различных органов приведены в следующей таблице: [2]
Дозовый эквивалент тонкого кишечника составляет:
Эквивалент дозы = 100 мЗв x 0,12 = 12 мЗв
Эквивалент дозы для желудка составляет:
Эквивалент дозы = 70 мЗв x 0,04 = 2,8 мЗв
Эффективная доза тогда будет равна эквивалентной дозе (тонкий кишечник) + эквивалентной дозе (желудок) = 12 мЗв + 2,8 мЗв = 14,8 мЗв. Этот риск вредного воздействия этого излучения равен 14,8 мЗв, полученным равномерно по всему телу.
Известно, что ионизирующее излучение вызывает развитие рака у людей. [4] Наше понимание этого основано на наблюдении за заболеваемостью раком у выживших после атомной бомбардировки . [4] [5] Исследование продолжительности жизни (LSS) — это долгосрочное исследование последствий для здоровья у японских выживших после атомной бомбардировки. [5] Кроме того, повышенная заболеваемость раком наблюдалась у шахтеров урановых рудников. [5] Это также наблюдается в других медицинских, профессиональных и экологических исследованиях. [4] [5] Сюда входят медицинские пациенты, подвергшиеся диагностическим или терапевтическим дозам радиации. [5] Сюда также входят лица, подвергшиеся воздействию источников радиации в окружающей среде, включая естественную радиацию . [5]

В LSS 105 427 человек (из примерно 325 000 выживших гражданских лиц) наблюдались с 1958 по 1998 год. [6] За это время было диагностировано 17 448 случаев рака. [6] Базовая прогнозируемая заболеваемость раком или количество новых случаев рака составляет около 7 000. [6] 850 из этих случаев рака были диагностированы у людей с предполагаемыми дозами более 0,005 Гр. [6] Другими словами, они были вызваны воздействием радиации атомной бомбы, что составляет 11% или 1 из 10 диагностированных случаев рака. [7] Население было определено как те, кто был выбран, чтобы включить три основные группы зарегистрированных жителей Хиросимы и Нагасаки:
(1) выжившие после атомной бомбардировки, находившиеся в радиусе 2,5 км от эпицентра во время бомбардировки (ATB),
(2) выжившие, которые находились на расстоянии от 2,5 до 10 км от эпицентра ATB (группа с низкой или нулевой дозой) и
(3) жители, которые временно не находились ни в Хиросиме, ни в Нагасаки или находились на расстоянии более 10 км от эпицентра в любом из городов (NIC) во время бомбардировок (группа, не подвергшаяся воздействию). [6]
В целом, люди подвергались воздействию широкого диапазона доз (от менее 0,005 Гр до 4 Гр). [7] Также существует широкий диапазон возраста. [7] Около 45 000 человек подверглись воздействию 0,005 Гр или 5 мЗв. [6] Исследование показывает линейную зависимость дозы от реакции для всех солидных опухолей. [6] Это означает, что связь между дозой и реакцией человеческого организма представляет собой прямую линию. [6] Чтобы увидеть пример, посмотрите на график под названием «Линейный график». Линейная зависимость дозы от реакции также означает, что скорость изменения реакции человеческого организма одинакова при любой дозе. [7]

Международная комиссия по радиологической защите (МКРЗ) описывает, как возникают детерминированные эффекты или вредные реакции тканей. [5] Существует пороговая доза , которая вызывает клиническое радиационное повреждение клеток в организме. [5] По мере увеличения дозы увеличивается тяжесть поражения. [5] Это также ухудшает восстановление тканей. [5] IRCP также описывает, как развивается рак после воздействия радиации. [5] Это происходит через процессы ответа на повреждение ДНК. [5] В последние десятилетия увеличилось количество клеточных и животных данных, которые подтверждают эту точку зрения. [5] Однако существует неопределенность при дозах около 100 мЗв или меньше. [5] Можно предположить, что заболеваемость раком будет расти с эквивалентной дозой в соответствующих органах и тканях. [5] Таким образом, Комиссия основывает рекомендации на этом предположении. [5] Дозы ниже этого порога в 100 мЗв приведут к прямому увеличению вероятности возникновения рака. [5] Эта модель доза-реакция известна как « линейная-беспороговая » или LNT. Чтобы увидеть модель, см. пунктирную линию на графике «Кривая доза-ответ линейно-беспороговой модели». Из-за этой неопределенности при низких дозах Комиссия не рассчитывает гипотетическое число случаев рака. [5]
В сфере здравоохранения специалисты могут подвергаться различным формам ионизации, если не принимают соответствующих профилактических мер. Воздействие может происходить через рентгеновские лучи , КТ и радиотерапию . [11] Эти методы визуализации используют ионное излучение для создания подробных изображений внутренней структуры частей тела, которые играют жизненно важную роль в здравоохранении для диагностических и терапевтических целей. Реализация профилактических мер имеет важное значение для снижения риска воздействия и обеспечения безопасности и защиты работников здравоохранения . [12]
Одной из важнейших мер по снижению риска воздействия радиации в сфере здравоохранения является проведение обучения по технике безопасности для всего персонала, работающего в различных областях радиации. [13] Эти обучения гарантируют, что работники обладают необходимыми знаниями для правильного обращения с этим оборудованием. Это обучение также охватывает использование средств индивидуальной защиты , обеспечивая ношение персоналом надлежащих фартуков/халатов, щитков/масок, очков, перчаток и т. д. Также важно, чтобы средства индивидуальной защиты надевались и снимались правильно. [13] Для дальнейшего обеспечения безопасности персонала в медицинских учреждениях есть контролируемые зоны и участки. Эти участки будут ограничены указателями и барьерами, чтобы обеспечить доступ только уполномоченному персоналу. [14]
Когда пациентам проводилась антиоксидантная терапия перед облучением, повреждение ДНК , измеряемое как двухцепочечные разрывы в лимфоцитах периферической крови, уменьшалось. [15] Таким образом, антиоксидантная терапия была предложена в качестве профилактической меры перед облучением. [15] Также у крыс антиоксидантная терапия улучшала апоптоз зародышевых клеток, вызванный высокой дозой ионизирующего облучения. [16]
Фоновое излучение исходит от естественно радиоактивных материалов и космического излучения из космоса. [5] Люди постоянно подвергаются воздействию этого излучения из окружающей среды, с годовой дозой около 3 мЗв. [5] Газ радон — это радиоактивный химический элемент, который является крупнейшим источником фонового излучения, около 2 мЗв в год. [17] Это похоже на КТ головы (см. таблицу). Другие источники включают космическое излучение, растворенный уран и торий в воде и внутреннее излучение (у людей с рождения внутри тела есть радиоактивный калий-40 и углерод-14). [18] Помимо медицинской визуализации, другие искусственные источники излучения включают строительные и дорожно-строительные материалы, горючее топливо, включая газ и уголь, телевизоры, детекторы дыма, светящиеся часы, табак, некоторые керамические изделия и многое другое в справке. [19] Ниже приведен пример из Комиссии по ядерному регулированию США о том, как различные виды продуктов питания содержат небольшое количество радиации. [20] Источниками радиации являются радиоактивный калий-40 (40K), радий-226 (226Ra) и другие атомы: [20]
На протяжении десятилетий в качестве эталона использовался стандартный мужчина , при этом женские особи и развивающиеся организмы не принимались во внимание.
Эмбрион и плод считаются высокочувствительными к воздействию радиации. [8] Самый высокий риск летальности приходится на период до имплантации . [8] Это до 10-го дня после зачатия . [8] Пороки развития обычно возникают после органогенеза . [8] Это фаза развития, когда три зародышевых слоя ( эктодерма , энтодерма и мезодерма ) формируют внутренние органы плода. [21] Расчетный порог дозы составляет 0,1 Гил линейно-переносящей энергии (ЛПЭ) радиации, и этот период обычно длится с 14-го по 50-й день. [8] Данные, полученные на животных, подтверждают идею о том, что пороки развития возникают при дозе около 100 мГр. [2] Другим риском является снижение коэффициента интеллекта (IQ). [8] Самый чувствительный период — 8–15-я неделя после зачатия. [8] IQ снижается на 30 баллов IQ/Зв, что может привести к тяжелой интеллектуальной инвалидности. [8] Пороки развития начинают возникать при пороговой дозе не менее 300 мГр. [2] Рак также может быть вызван облучением , которое обычно происходит с 51-го по 280-й день беременности. [8] Большинство рентгеновских лучей происходит в третьем триместре беременности. [8] Существует скудная информация о воздействии радиации в первом триместре беременности. [8] Однако данные свидетельствуют о том, что относительный риск составляет 2,7. [8] Относительный риск является мерой вероятности исхода в одной группе по сравнению с другой. В этом случае риск образования рака в первом триместре в 2,7 раза выше, чем риск образования рака в третьем триместре. Кроме того, Научный комитет Организации Объединенных Наций по действию атомной радиации рассчитал избыточный относительный риск в первом триместре. [22] Он составляет 0,28 на мГр. [22] Избыточный относительный риск представляет собой уровень заболеваемости среди облученной популяции, деленный на уровень заболеваемости среди необлученной популяции, минус 1,0. [2] Это означает, что риск развития рака в результате облучения в первом триместре на 28% выше, чем в третьем триместре.
Использование радиации в медицинской визуализации имеет множество преимуществ. [23] Скрининговые обследования с помощью визуализации используются для раннего выявления рака, что снижает риск смерти. [23] Это также снижает риск возникновения серьезных заболеваний, ограничивающих продолжительность жизни, и позволяет избежать хирургического вмешательства . [23] Эти тесты включают скрининг рака легких , скрининг рака груди и многое другое. [23] [24] Радиация также используется в качестве терапии для многих различных типов рака. [25] Около 50% всех онкологических больных получают лучевую терапию . [25] Лучевая терапия уничтожает раковые клетки, останавливая их рост. [25] Помимо рака, многие типы медицинской визуализации используются для диагностики опасных для жизни заболеваний, таких как сердечные приступы , тромбоэмболия легочной артерии и пневмония . [26] [27] [28]
Поле гамма-излучения можно охарактеризовать мощностью экспозиции (в единицах, например, рентген в час). Для точечного источника мощность экспозиции будет линейно пропорциональна радиоактивности источника и обратно пропорциональна квадрату расстояния, [29]
где F — мощность облучения, r — расстояние, α — активность источника, а Γ — константа мощности облучения, которая зависит от конкретного радионуклида, используемого в качестве источника гамма-излучения.
Ниже приведена таблица констант мощности экспозиции для различных радионуклидов. Они дают мощность экспозиции в рентгенах в час для заданной активности в милликюри на расстоянии в сантиметрах . [30]
В следующей таблице приведены величины излучения в единицах СИ и вне системы СИ:
Хотя Комиссия по ядерному регулированию США разрешает использовать единицы кюри , рад и бэр наряду с единицами СИ [32] , директивы Европейского союза о европейских единицах измерения требуют, чтобы их использование в «целях общественного здравоохранения...» было прекращено к 31 декабря 1985 года. [33]