
SDS-PAGE ( электрофорез в полиакриламидном геле с додецилсульфатом натрия ) представляет собой прерывистую электрофоретическую систему , разработанную Ульрихом К. Леммли, которая обычно используется в качестве метода разделения белков с молекулярной массой от 5 до 250 кДа . [1] [2] Совместное использование додецилсульфата натрия (SDS, также известного как лаурилсульфат натрия) и полиакриламидного геля устраняет влияние структуры и заряда, а белки разделяются за счет различий в их размерах. По крайней мере, до 2012 года публикация с ее описанием была наиболее часто цитируемой статьей одного автора и второй по цитируемости в целом. [3]
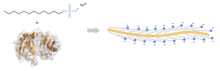

SDS-PAGE — это метод электрофореза , который позволяет разделять белки по массе. Среда (также называемая «матрицей») представляет собой дисперсный гель на основе полиакриламида. Полиакриламидный гель обычно помещается между двумя стеклянными пластинами в пластинчатом геле. Хотя тюбиковые гели (в стеклянных цилиндрах) использовались исторически, они быстро устарели с изобретением более удобных пластинчатых гелей. [4] Кроме того, используется ДСН ( додецилсульфат натрия ). Около 1,4 грамма ДСН связывается с граммом белка, [5] [6] [7] что соответствует одной молекуле ДСН на две аминокислоты . SDS действует как поверхностно-активное вещество , маскируя собственный заряд белка и придавая ему очень похожее соотношение заряда к массе. Собственные заряды белков незначительны по сравнению с нагрузкой SDS, а положительные заряды также значительно уменьшаются в основном диапазоне pH разделительного геля. При приложении постоянного электрического поля белки мигрируют к аноду, каждый с разной скоростью, в зависимости от их массы. Эта простая процедура позволяет точно разделить белки по массе.
ДСН имеет тенденцию образовывать сферические мицеллы в водных растворах при концентрации выше определенной, называемой критической мицеллярной концентрацией (ККМ). Выше критической концентрации мицелл от 7 до 10 миллимолярных в растворах ДСН встречается одновременно в виде одиночных молекул ( мономеров ) и мицелл, ниже КМЦ ДСН встречается только в виде мономеров в водных растворах. При критической концентрации мицелл мицелла состоит примерно из 62 молекул ДСН. [8] Однако только мономеры ДСН связываются с белками посредством гидрофобных взаимодействий, тогда как мицеллы ДСН являются анионными снаружи и не адсорбируют никаких белков. [5] SDS имеет амфипатическую природу, что позволяет ему разворачивать как полярные, так и неполярные участки белковой структуры. [9] При концентрациях ДСН выше 0,1 миллимолярного начинается разворачивание белков, [5] и выше 1 мМ большинство белков денатурируется. [5] Из-за сильного денатурирующего эффекта ДСН и последующей диссоциации белковых комплексов четвертичные структуры обычно не могут быть определены с помощью ДСН. Исключением являются белки, стабилизированные ковалентной сшивкой (например, -SS-сшивками), и устойчивые к ДСН белковые комплексы, которые стабильны даже в присутствии ДСН (последний, однако, только при комнатной температуре). Для денатурации SDS-устойчивых комплексов необходима высокая энергия активации, которая достигается за счет нагревания. Устойчивость к SDS основана на метастабильности складки белка. Хотя нативный, полностью свернутый, устойчивый к ДСН белок не обладает достаточной стабильностью в присутствии ДСН, химическое равновесие денатурации при комнатной температуре наступает медленно. Стабильные белковые комплексы характеризуются не только устойчивостью к SDS, но также устойчивостью к протеазам и увеличенным биологическим периодом полураспада . [10]
Альтернативно, электрофорез в полиакриламидном геле также можно проводить с катионными поверхностно-активными веществами CTAB в CTAB-PAGE, [11] [12] [13] или 16-BAC в BAC-PAGE. [14]
Метод SDS-PAGE состоит из подготовки геля, подготовки проб, электрофореза, окрашивания белков или вестерн-блоттинга и анализа полученного рисунка полос.


При использовании в геле разных буферов (прерывистый гель-электрофорез) гели готовят за сутки до электрофореза, чтобы диффузия не приводила к смешиванию буферов. Гель получают методом свободнорадикальной полимеризации в форме, состоящей из двух герметично закрытых стеклянных пластин с прокладками между стеклянными пластинами. В типичном варианте мини-геля прокладки имеют толщину 0,75 мм или 1,5 мм, что определяет нагрузочную способность геля. Для разливания раствора геля планшеты обычно закрепляют на подставке, которая временно герметизирует открытую в противном случае нижнюю сторону стеклянных пластин двумя прокладками. Для гелевого раствора смешивают акриламид в качестве гелеобразователя (обычно 4% по объему в укладочном геле и 10-12% в разделяющем геле), метиленбисакриламид в качестве сшивающего агента, укладочный или разделительный гель-буфер, воду и ДСН. . При добавлении катализатора TEMED и радикального инициатора персульфата аммония (APS) начинается полимеризация. Затем раствор разливают между стеклянными пластинами, не создавая пузырьков. В зависимости от количества катализатора и радикального стартера, а также от температуры полимеризация длится от четверти часа до нескольких часов. Нижний гель (разделительный гель) наливают первым и покрывают несколькими каплями труднорастворимого в воде спирта (обычно буферно-насыщенного бутанола или изопропанола), который удаляет пузырьки из мениска и защищает раствор геля от радикалов-поглотителей кислорода. После полимеризации разделительного геля спирт выбрасывают, а остатки спирта удаляют фильтровальной бумагой . После добавления APS и TEMED к раствору штабелирующего геля его выливают поверх твердого разделительного геля. После этого между стеклянными пластинами вставляют подходящую гребенку для образцов, не создавая пузырьков. После полимеризации гребешок для образцов осторожно вынимают, оставляя карманы для нанесения образца. Для последующего использования белков для секвенирования белков гели часто готовят за день до электрофореза, чтобы уменьшить реакции неполимеризованного акриламида с цистеинами в белках.
С помощью градиентного смесителя можно отливать градиентные гели с градиентом акриламида (обычно от 4 до 12%), которые имеют больший диапазон разделения молекулярных масс. [15] Коммерческие гелевые системы (так называемые готовые гели ) обычно используют буферное вещество бис-трис метан со значением pH от 6,4 до 7,2 как в накопительном, так и в разделяющем геле. [16] [17] Эти гели поставляются в виде отлитых и готовых к использованию. Поскольку они используют только один буфер (непрерывный гель-электрофорез) и имеют почти нейтральный pH, их можно хранить в течение нескольких недель. Более нейтральный pH замедляет гидролиз и, следовательно, разложение полиакриламида. Кроме того, в белках меньше цистеинов, модифицированных акриламидом. [16] Из-за постоянного pH в собирающем и разделяющем геле эффект суммирования отсутствует. Белки в гелях БисТрис не окрашиваются комплексами рутения. [18] Эта гелевая система имеет сравнительно большой диапазон разделения, который можно варьировать, используя MES или MOPS в рабочем буфере. [16]

Во время подготовки пробы к белкам в избытке добавляют буфер для пробы и, следовательно, ДСН, а затем пробу нагревают до 95°C в течение пяти минут или, альтернативно, до 70°C в течение десяти минут. Нагревание разрушает вторичную и третичную структуру белка, разрушая водородные связи и растягивая молекулы. Необязательно дисульфидные мостики можно расщепить путем восстановления. Для этой цели в буфер для образца добавляют восстанавливающие тиолы , такие как β-меркаптоэтанол (β-ME, 5% по объему), дитиотреитол (DTT, 10 миллимолярный) или дитиоэритрит (DTE, 10 миллимолярный). После охлаждения до комнатной температуры каждый образец пипеткой вносят в собственную лунку в геле, предварительно погруженном в электрофорезный буфер в аппарате для электрофореза.
Помимо образцов в гель обычно наносят маркер размера молекулярной массы . Он состоит из белков известных размеров и тем самым позволяет оценить (с погрешностью ± 10%) размеры белков в реальных образцах, которые мигрируют параллельно по разным дорожкам геля. [19] Маркер размера часто вводится пипеткой в первый или последний карман геля.


Для разделения денатурированные образцы загружают в гель полиакриламида, который помещают в буфер для электрофореза с подходящими электролитами. После этого подается напряжение (обычно около 100 В, 10-20 В на см длины геля), которое вызывает миграцию отрицательно заряженных молекул через гель в направлении положительно заряженного анода . Гель действует как сито. Небольшие белки относительно легко мигрируют через сетку геля, в то время как более крупные белки с большей вероятностью задерживаются и, следовательно, медленнее мигрируют через гель, что позволяет разделить белки по размеру молекул. Электрофорез длится от получаса до нескольких часов в зависимости от напряжения и длины используемого геля.
Наиболее быстро мигрирующие белки (с молекулярной массой менее 5 кДа) образуют буферный фронт вместе с анионными компонентами буфера для электрофореза, которые также мигрируют через гель. Область фронта буфера становится видимой путем добавления в буфер для образца сравнительно небольшого количества анионного красителя бромфенолового синего . Из-за относительно небольшого размера молекулы бромфенолового синего он мигрирует быстрее, чем белки. Путем оптического контроля мигрирующей цветной полосы электрофорез можно остановить до того, как краситель, а также образцы полностью пройдут через гель и покинут его.
Наиболее часто используемым методом является прерывистый SDS-PAGE. В этом методе белки сначала мигрируют в собирающий гель с нейтральным pH, в котором они концентрируются, а затем мигрируют в разделительный гель с основным pH, в котором происходит фактическое разделение. Укладочные и разделительные гели различаются разным размером пор (4-6 % Т и 10-20 % Т), ионной силой и значениями pH (pH 6,8 или pH 8,8). Наиболее часто используемым электролитом является SDS-содержащая трис - глицин - хлоридная буферная система. При нейтральном pH глицин образует преимущественно цвиттер-ионную форму, при высоком pH глицины теряют положительные заряды и становятся преимущественно анионных. В собирающем геле более мелкие отрицательно заряженные ионы хлорида мигрируют перед белками (как ведущие ионы), а несколько более крупные отрицательно и частично положительно заряженные ионы глицината мигрируют позади белков (как начальные замыкающие ионы), тогда как в сравнительно В основном разделяющем геле оба иона мигрируют перед белками. Градиент pH между буферами накопительного и разделительного геля приводит к эффекту накопления на границе накопительного геля и разделительного геля, поскольку глицинат частично теряет свои замедляющие положительные заряды по мере увеличения pH, а затем, по мере того, как бывший отстающий ион, догоняет его. белков и становится ведущим ионом, в результате чего полосы различных белков (видимые после окрашивания) становятся уже и острее – эффект суммирования. Для разделения более мелких белков и пептидов используется буферная система TRIS- Tricine Шеггера и фон Ягова из-за более высокого распределения белков в диапазоне от 0,5 до 50 кДа. [20]

В конце электрофоретического разделения все белки сортируются по размеру и затем могут быть проанализированы другими методами, например, окрашиванием белков, таким как окрашивание Кумасси (наиболее распространенное и простое в использовании), [21] [22] окрашивание серебром (самая высокая чувствительность). ), [23] [24] [25] [26] [27] [28] окрашивает все виды окрашивания, окрашивание амидо-черным 10B , [22] окрашивание быстрым зеленым FCF , [22] флуоресцентные окрашивания, такие как окрашивание эпикоккононом [29] и Оранжевое окрашивание SYPRO [30] и иммунологическое обнаружение, такое как вестерн-блоттинг . [31] [32] Флуоресцентные красители имеют сравнительно более высокую линейность между количеством белка и интенсивностью цвета, примерно на три порядка выше предела обнаружения (количество белка, которое можно оценить по интенсивности цвета). При использовании флуоресцентного белкового красителя трихлорэтанола последующее окрашивание белка не требуется, если он был добавлен в раствор геля и гель был облучен УФ-светом после электрофореза. [33] [34]
При окрашивании Кумасси гель фиксируют в 50% растворе этанола и 10% ледяной уксусной кислоты в течение 1 часа. Затем раствор меняют на свежий и через 1-12 часов гель заменяют на красящий раствор (50% метанол, 10% ледяная уксусная кислота, 0,1% кумасси бриллиантовый синий) с последующей заменой окрашивающего раствора несколько раз на 40% раствор. метанол, 10% ледяная уксусная кислота.
Окрашивание белков в геле создает документируемый рисунок полос различных белков.
Документирование рисунка полос обычно выполняется путем фотографирования или сканирования. Для последующего восстановления молекул в отдельных полосах можно провести гель-экстракцию .

После окрашивания белка и документирования рисунка полос полиакриламидный гель можно высушить для архивного хранения. Белки из него можно извлечь позднее. Гель помещают либо в сушильную камеру (с использованием тепла или без него), либо в вакуумную сушилку. Сушильный каркас состоит из двух частей, одна из которых служит основой для влажной целлофановой пленки, к которой добавляется гель и однопроцентный раствор глицерина . Затем накладывают вторую влажную целлофановую пленку без пузырьков, сверху надевают вторую часть рамки и закрепляют раму зажимами. Удаление пузырьков воздуха позволяет избежать фрагментации геля во время высыхания. Вода испаряется через целлофановую пленку. В отличие от сушильной установки, вакуумная сушилка создает вакуум и нагревает гель примерно до 50 °C.

Для более точного определения молекулярной массы в разделяющем геле измеряют относительные расстояния миграции отдельных полос белка. [37] [38] Измерения обычно выполняются в трех экземплярах для повышения точности. Относительная подвижность (называемая значением Rf или значением Rm) определяется как расстояние, пройденное полосой белка, деленное на расстояние, пройденное фронтом буфера. Каждое расстояние измеряется от начала разделительного геля. Миграция фронта буфера примерно соответствует миграции красителя, содержащегося в буфере образца. Rf маркера размера нанесены на график в полулогарифмическом графике в зависимости от их известных молекулярных масс. Путем сравнения с линейной частью построенного графика или с помощью регрессионного анализа молекулярную массу неизвестного белка можно определить по его относительной подвижности. [37] [39]
Полосы белков с гликозилированием могут быть размытыми [35] , поскольку гликозилирование часто бывает гетерогенным. [40] Белки со многими основными аминокислотами (например, гистонами ) [41] могут приводить к завышению молекулярной массы или даже вообще не мигрировать в гель, поскольку при электрофорезе они движутся медленнее из-за положительных зарядов или даже из-за противоположное направление. С другой стороны, многие кислые аминокислоты могут привести к ускоренной миграции белка и недооценке его молекулярной массы. [42]
SDS-PAGE в сочетании с красителем белков широко используется в биохимии для быстрого и точного разделения и последующего анализа белков. Он имеет сравнительно низкие затраты на инструменты и реагенты и является простым в использовании методом. Из-за низкой масштабируемости его чаще всего используют в аналитических целях, а не в препаративных целях, особенно когда необходимо выделить большие количества белка.
Кроме того, SDS-PAGE используется в сочетании с вестерн-блоттингом для определения присутствия конкретного белка в смеси белков или для анализа посттрансляционных модификаций . Посттрансляционные модификации белков могут привести к различной относительной подвижности (т.е. сдвигу полосы ) или к изменению связывания детектирующего антитела, используемого в вестерн-блоттинге (т.е. полоса исчезает или появляется).
В масс-спектрометрии белков SDS-PAGE является широко используемым методом подготовки проб перед спектрометрией, в основном с использованием расщепления в геле . Что касается определения молекулярной массы белка, SDS-PAGE немного более точен, чем аналитическое ультрацентрифугирование , но менее точен, чем масс-спектрометрия или - без учета посттрансляционных модификаций - расчет молекулярной массы белка по ДНК. последовательность .
В медицинской диагностике SDS-PAGE используется как часть теста на ВИЧ и для оценки протеинурии . В тесте на ВИЧ белки ВИЧ разделяются с помощью SDS-PAGE и впоследствии выявляются методом вестерн-блоттинга с ВИЧ-специфичными антителами пациента, если они присутствуют в его сыворотке крови . SDS-PAGE при протеинурии оценивает уровни различных сывороточных белков в моче, например, альбумина , альфа-2-макроглобулина и IgG .
SDS-PAGE является наиболее широко используемым методом гель-электрофоретического разделения белков. Двумерный гель-электрофорез последовательно сочетает изоэлектрическое фокусирование или BAC-PAGE с SDS-PAGE. Нативный PAGE используется, если необходимо сохранить нативную укладку белка. Для разделения мембранных белков в качестве альтернативы SDS-PAGE можно использовать BAC-PAGE или CTAB-PAGE. Для электрофоретического разделения более крупных белковых комплексов можно использовать электрофорез в агарозном геле , например, SDD-AGE . Некоторые ферменты можно обнаружить по их ферментативной активности с помощью зимографии .
Являясь одним из наиболее точных и недорогих методов разделения и анализа белков, SDS-PAGE денатурирует белки. Если необходимы неденатурирующие условия, белки разделяют с помощью нативного PAGE или различных хроматографических методов с последующей фотометрической количественной оценкой , например аффинной хроматографией (или даже тандемной аффинной очисткой ), эксклюзионной хроматографией , ионообменной хроматографией . [43] Белки также можно разделить по размеру с помощью тангенциальной проточной фильтрации [44] или ультрафильтрации . [45] Отдельные белки можно выделить из смеси с помощью аффинной хроматографии или анализа с понижением концентрации . Некоторые исторически ранние и экономически эффективные, но грубые методы разделения обычно основаны на серии экстракций и осаждений с использованием коссмотропных молекул, например осаждение сульфатом аммония и осаждение полиэтиленгликолем .
В 1948 году Арне Тиселиус был удостоен Нобелевской премии по химии за открытие принципа электрофореза, заключающегося в миграции заряженных и растворенных атомов или молекул в электрическом поле. [46] Использование твердой матрицы (первоначально бумажных дисков) в зонном электрофорезе улучшило разделение. Прерывистый электрофорез 1964 г., проведенный Л. Орнштейном и Б. Дж. Дэвисом, позволил улучшить разделение за счет эффекта суммирования. [47] Использование сшитых полиакриламидных гидрогелей, в отличие от ранее использовавшихся бумажных дисков или крахмальных гелей, обеспечило более высокую стабильность геля и отсутствие микробного разложения. Денатурирующий эффект SDS в непрерывных полиакриламидных гелях и последующее улучшение разрешения были впервые описаны в 1965 году Дэвидом Ф. Саммерсом в рабочей группе Джеймса Э. Дарнелла по разделению белков полиовируса. [48] Текущий вариант SDS-PAGE был описан в 1970 году Ульрихом К. Леммли и первоначально использовался для характеристики белков в головке бактериофага Т4 . [1]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{citation}}: CS1 maint: несколько имен: список авторов ( ссылка )